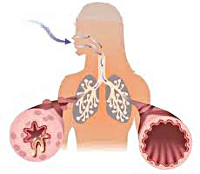
Бронхиальная астма фармакологический подход

Основной принцип лечения бронхиальной астмы — назначение базисной терапии (противовоспалительной терапии) и симптоматических средств с бронхорасширяющим эффектом. Стратегия лечения основана на пятиступенчатом подходе; первые четыре ступени отражают нарастание медикаментозной терапии в зависимости от степени тяжести заболевания, а пятая ступень (step down) — возможность снижения поддерживающих доз противоастматических препаратов после 3-месячного стабильного состояния больного.
Оптимальным путем введения лекарственных средств при бронхиальной астме является ингаляционный, что обеспечивает усиление местного лечебного эффекта препаратов и уменьшает системные (как правило, неблагоприятные) действия.
Препараты для лечения больных бронхиальной астмой разделяют:
- • на препараты для контроля за течением бронхиальной астмы — глюкокортикостероиды (см. подробно «Клиническая фармакология противовоспалительных лекарственных средств»), (32- адреностимуляторы длительного действия, стабилизаторы мембран тучных клеток, антагонисты лейкотриеновых рецепторов, теофиллин продленного действия;
- • препараты для купирования симптомов бронхиальной астмы — (32- адреностимуляторы короткого действия, комбинированные препараты ((32-адреностимуляторы короткого действия + ингаляционный М-холиноблокатор).
Препараты для контроля за течением бронхиальной астмы назначают всем больным, кроме пациентов с легким интермиттирующим течением болезни (несколько приступов в год). При этом предпочтительны ингаляционные глюкокортикостероиды (см. подробно «Клиническая фармакология противовоспалительных лекарственных средств»).
У больных с легким течением бронхиальной астмы целесообразно использовать стабилизаторы мембран тучных клеток для кальция или низкие дозы ингаляционных глюкокортикостероидов (ГКС), более тяжелое течение заболевания предусматривает применение средних и высокихдоз ингаляционных ГКС всочетании с Р2-адреностимуляторами длительного действия. Если на фоне приема высоких доз ингаляционных ГКС сохраняются приступы удушья, наряду с ингаляционными ГКС и Р2-адреностимуляторами длительного действия, назначают препараты теофиллина пролонгированного действия, модификаторы лейкотриенов, а при наиболее тяжелых формах бронхиальной астмы — ГКС внутрь, антииммуноглобулиновые препараты.
Для купирования симптомов бронхиальной астмы (на фоне проведения базисной терапии) назначают |32-адреностимуляторы короткого действия в режиме «по требованию».
При лечении обострений бронхиальной астмы применяют ингаляции Р2-адреностимуляторов короткого действия, М-холиноблокато- ры (в сочетании с Р2-адреностимуляторами), инъекции эуфиллина. Тяжелое обострение бронхиальной астмы является показанием к назначению короткого (10—14 дней) курса лечения ГКС внутрь (пред- низолон 40-60 мг/сутки).
Контроль эффективности лечения бронхиальной астмы
Контроль течения заболевания подразумевает достижение основных целей лечения — минимальные клинические проявления (в том числе ночью); минимальный прием р2-адреностимуляторов; восстановление физической активности в полном объеме; сведение вариабельности (утро—вечер) пиковой скорости выдоха до 20% и менее, доведение пиковой скорости выдоха до пределов физиологической нормы (самоконтроль больным с помощью пикфлоуметра).
Эффективность ингаляционных бронхолитиков для лечения приступа бронхиальной астмы можно оценить уже через 15—30 мин после их применения по увеличению показателей спирометрии. Эффективность ГКС можно оценить только через 1 —7 суток, а стабилизаторов тучных клеток — не ранее, чем через один месяц после начала лечения.
Источник
Рустем Салахович Фассахов
Оксана Евгеньевна Богоутдинова
Дарья Ивановна Владимирова
Кафедра аллергологии и клинической иммунологии Казанской государственной медицинской академии
Несмотря на то что термин “гормонально_зависимая бронхиальная астма” (или дополнение “гормональнозависимое течение” к диагнозу “бронхиальная астма”) в классификациях бронхиальной астмы (БА) отсутствует, его часто можно встретить как в амбулаторных картах и историях болезни, так и в научных публикациях. В современной научной литературе принято употреблять термин “стероидозависимая БА”. Большинство больных БА постоянно пользуются ингаляционными симпатомиметиками – аналогами адреналина – также гормона надпочечников, но этих больных “гормонально-зависимыми” не называют.
К сожалению, отсутствуют рекомендации по ведению этой категории больных БА в международных руководствах по диагностике и лечению БА (GINA, EPR-2), да и в отечественной литературе после исследований А.Г. Чучалина и Б.И. Шмушковича [1, 2] клинических работ по этой проблеме явно недостаточно. Что понимают под определением “стероидозависимая”? Сколько больных БА получают системные глюкокортикостероиды (ГКС) на постоянной основе? Каковы причины, заставляющие назначать больным БА системные ГКС? Что можно сделать, чтобы не допустить зависимости больных от системных ГКС? Как “снять” больного с таблеток? Именно эти вопросы встают перед врачом при ведении больных со стероидозависимой БА.
Определение стероидозависимой БА
Что же понимают под термином “стероидозависимая астма”? Это тяжелая форма БА, характеризующаяся упорным, постоянно рецидивирующим течением, для предупреждения симптомов которой больной вынужден принимать системные ГКС в виде таблеток или инъекций длительными (в течение месяцев) курсами или постоянно.
Постоянное применение системных препаратов ГКС – наименее желательный вариант терапии БА в связи с высоким риском развития серьезных осложнений. Через 1–2 года такого лечения побочные эффекты по ущербу здоровью больного зачастую превосходят само заболевание. Речь идет прежде всего о развитии стероидного диабета, васкулита, язвенных поражений желудочно-кишечного тракта, катаракты, а также остеопороза. В связи с этим врач должен сделать все, чтобы больной БА либо вовсе не получал системные ГКС на постоянной основе, либо в крайнем случае принимал их в минимально необходимой дозе.
Число больных БА, постоянно получающих системные ГКС, достаточно велико. Так, из 1552 больных БА, состоящих на учете в поликлиниках одного из крупных городов Республики Татарстан (население около 500 тыс. человек), получают ГКС на постоянной основе 466 больных (30%). Аналогичные данные получены нами и по г. Казани. Такой высокий процент стероидозависимых больных связан, на наш взгляд, с двумя причинами. Первая из них – особенности национальной статистики. На учете в поликлиниках стоят, как правило, только больные с тяжелым течением БА [1]. Об этом говорит и тот факт, что 20–25% стоящих на учете больных БА имеют инвалидность. Вторая причина – ошибки в диагностике и лечении БА.
Причины стероидозависимости
Прежде чем говорить о том, как “снять” больного с гормонов, необходимо выяснить причины, обусловившие необходимость такой терапии. В подавляющем большинстве случаев в качестве обоснования для назначения системных ГКС указывают на безуспешность остальных методов лечения. Однако проведенный нами анализ позволил выявить следующие причины стероидозависимости, расположив их в порядке значимости.
1. Ошибки в диагностике
Ошибочный диагноз БА. У взрослых ошибочный диагноз БА часто выставляют больным с хронической обструктивной болезнью легких, синдромом Чарджа–Стросса, астматическим вариантом узелкового периартериита; опухолями бронхов; бронхоэктазами; при дисфункции голосовых связок.
Следует также проводить дифференциальную диагностику с реже встречающимися заболеваниями: трахеобронхомаляцией, обструктивным бронхиолитом, муковисцидозом.
У детей к этим диагнозам следует добавить врожденные аномалии верхних дыхательных путей, дисфункцию ресничек и аспирацию инородных тел [1]. За исключением синдрома Чарджа–Стросса и узелкового периартериита, у больных с указанными выше заболеваниями применение системных ГКС по ежедневной схеме не обосновано.
Ошибки в этиологической диагностике БА. Наиболее часто приходится встречаться с ошибками в этиологической диагностике БА. Зачастую больного БА вообще не консультирует аллерголог, и диагноз “инфекционноаллергическая” или “инфекционно-зависимая” БА ставится врачом только на основании данных анамнеза о связи обострений с некими “простудными заболеваниями”. Каждый больной с впервые выставленным диагнозом БА должен получить консультацию аллерголога или другого специалиста, который может проводить аллергологическое обследование. Только аллерголог сможет квалифицированно подтвердить (или исключить) аллергическую природу заболевания. Не менее чем у 50% всех взрослых больных БА причиной заболевания является аллергия (у детей – до 90%). Нами проведен анализ этиологического диагноза БА в поликлиниках г. Казани. Оказалось, что атопическая форма зафиксирована лишь у 15% из стоящих на учете взрослых больных БА. Это значит, что у 35–40% всех больных БА этиологический диагноз – ошибочный. Если сопоставить эту цифру с количеством получающих системные ГКС (35–50%), комментарии становятся излишними.
Вторая по частоте ошибка в этиологической диагностике БА относится к больным с так называемой аспириновой астмой. Непереносимость нестероидных противовоспалительных препаратов встречается у 10–30% взрослых больных БА, однако диагностируют эту форму заболевания редко.
2. Ошибки в лечении
Исходящие из ошибок в диагностике БА. Ошибки в диагностике ведут к неадекватной терапии заболевания. Основным методом лечения аллергических заболеваний, в том числе атопической БА, является специфическая терапия, связанная с воздействием на конкретную причину заболевания – аллерген.
При выявлении последнего ведущим методом лечения служат элиминационные мероприятия, направленные на полное устранение аллергена или максимально возможное уменьшение контакта с ним.
Зачастую одних этих мероприятий (при аллергии на домашнюю пыль – удаления “пылесборников”: перьевых подушек, перин, ковров и т.д.) бывает достаточно для существенного улучшения течения заболевания, уменьшения дозы принимаемых противовоспалительных и симптоматических препаратов.
И напротив, невыполнение этих мероприятий приводит к тяжелому течению заболевания, вплоть до стероидозависимости. Растет количество публикаций о тяжелом течении БА у больных с аллергией на споры плесневых грибов, аллергены тараканов.
И если больной с аллергией на плесень живет в квартире с повышенной влажностью (например, в полуподвальном помещении) – стероидозависимость ему обеспечена. Особая тема – аллергия на домашних животных. Сенсибилизация к аллергенам кошек и собак встречается все чаще. К сожалению, выпускаемые отечественной промышленностью аллергены домашних животных для диагностики изготовлены из шерсти, в то время как основным источником аллергенов кошки является слюна. По нашим данным, кожные пробы с выпускаемыми в России аллергенами кошки и собаки выявляют сенсибилизацию лишь у 20–25% больных с аллергией на этих животных. Аллергенов для кожных проб на аллергию к тараканам в России вообще нет; в последние 5 лет не производятся и грибковые аллергены. С высокой степенью остоверности выявляют аллергию к животным (а также к тараканам) лабораторные тесты на основе определения специфических IgE_антител. Несвоевременная аллергологическая диагностика и невыполнение элиминационных мероприятий являются, по нашим наблюдениям, причиной применения системных ГКС у 25% стероидозависимых больных БА.
Неадекватная фармакотерапия БА. Нередко к стероидозависимости приводит неадекватная фармакотерапия заболевания.
Речь идет прежде всего о необоснованном назначении системных ГКС. С сожалением приходится констатировать, что до сих пор больным БА назначают депо-препараты – масляные растворы триамцинолона (кеналог_40), метилпреднизолона (метипред_40, депо_медрол) и бетаметазона (дипроспан). При инъекции этих препаратов создается депо, постепенно в течение 0,5–1 мес высвобождающее ГКС в кровоток.
В качестве оправдания такого метода терапии указывают на его “удобство для больных”: 1 инъекция в 3–4 нед улучшает состояние пациентов. Весьма опасное заблуждение! Депонированные препараты ГКС представляют наибольшую опасность в плане развития побочных эффектов, прежде всего стероидозависимости. Постоянная концентрация ГКС в крови через 4–5 инъекций приводит к угнетению функции коры надпочечников, часто необратимому, – больные уже не смогут обходиться без введения этих препаратов.
Наряду с развитием стероидного васкулита, диабета, миопатии, исподволь формируется одно из наиболее неблагоприятных осложнений – остеопороз, возрастает риск переломов. У больных с тяжелой стероидозависимой БА высок риск осложнений оперативного лечения переломов, обусловленный плохим заживлением ран, сниженным иммунитетом, стероидным диабетом. Именно с этими обстоятельствами связаны катастрофические цифры: при остеопорозе летальность в течение года после перелома шейки бедра составляет 50%!
В мировой практике пролонгированными препаратами ГКС лечат:
1) некоторых страдающих БА психических больных, которые не могут самостоятельно принимать необходимые препараты;
2) асоциальных лиц (алкоголиков, наркоманов) с тяжелой угрожающей жизни БА, отказывающихся правильно лечиться.
Назначая пациентам с БА пролонгированные ГКС, мы ставим их наравне с указанными категориями больных.
3. Крайне тяжелое, нестабильное течение БА, не поддающееся другим методам лечения
Среди наблюдавшихся нами стероидозависимых больных БА этих пациентов – меньшинство. Необходимость постоянного приема системных ГКС может быть обусловлена второй формой так называемой нестабильной БА [1], относительно благоприятное течение которой неожиданно, без видимых причин, может “взрываться” тяжелыми обострениями, развитием астматического статуса с высоким риском неблагоприятного исхода. Эту форму БА называют потенциально смертельной БА.
Одной из причин тяжелого постоянно рецидивирующего течения БА может быть сопутствующее заболевание: бронхолегочный аспергиллез, тиреотоксикоз, хронический гнойный синусит, рефлюкс_эзофагит. У этой категории больных лечение сопутствующего заболевания и адекватная базисная терапия БА в большинстве случаев позволяет отменить или существенно уменьшить дозу системных ГКС.
Как “снять” больного БА с системных ГКС
Универсального подхода к отмене системных ГКС у больных со стероидозависимой БА не существует. Принципиальное значение имеет причина назначения системных ГКС (см. выше). Если основной фактор тяжелого течения БА – выявленный и остающийся в окружении больного аллерген, наиболее существенными для отмены системных ГКС являются элиминационные мероприятия. Нельзя рассчитывать на отмену системных ГКС у больных БА с аллергией к животным, если семейный любимец остается в квартире. На сегодня альтернативы удалению животного из дому у этих пациентов не существует.
В последнее время существенно расширились возможности для снижения концентрации аллергенов домашней пыли. Наряду с традиционными способами (замена подушек и одеял на синтепоновые, удаление из спальни ковров, мягких игрушек и т.д.), появились новые возможности: защитные чехлы на подушки, матрацы и одеяла, специальный материал которых не пропускает аллергены клещей домашней пыли, а также воздухоочистители с фильтрами НЕРА. Кроме этого, к применению в России разрешены некоторые акарицидные (убивающие аллергенных клещей и разрушающие их аллергены) препараты – акаросан (пена для нанесения на мягкую мебель и ковры) и акарил (добавка к стиральному порошку).
Соблюдение “беспылевого” режима – первое и обязательное условие в лечении рассматриваемой категории больных. Среди подходов к снижению дозы и отмене системных ГКС следует отметить применение цитостатиков (метотрексата), некоторых макролидов (тролеандомицина), препаратов золота, а также нефармакологические методы (плазмаферез и др.). Однако критический анализ стероидозамещающего эффекта, проведенный институтом Соchrane [5], не подтвердил их эффективности.
На сегодня основным фармакологическим подходом к снижению и отмене системных ГКС при БА является замещение их ингаляционными препаратами ГКС (ИГКС) в комбинации с ингаляционными бета2-адреномиметиками пролонгированного действия.
В своей клинической практике мы используем при снижении дозы системных ГКС флютиказона пропионат – фликсотид (ФЛ), выбор которого был обусловлен следующими обстоятельствами. ФЛ обладает очень высокой местной противовоспалительной активностью. Этот момент принципиально важен, потому что при снятии больного с системных ГКС назначаются максимальные дозы ИГКС. Для получения аналогичного эффекта применяют дозировки ФЛ в 2 раза ниже, чем остальных ИГКС. ФЛ выпускается в широком диапазоне дозировок – 50, 125, 250 и 500 мкг в 1 ингаляционной дозе, что позволяет назначать в начальный период высокие дозы за 1–2 ингаляции, а при снижении осуществлять максимально плавное уменьшение дозы ИГКС.
Разнообразие систем доставки ФЛ позволяет использовать его на разных этапах снятия больных с системных ГКС – если в начальный период предпочтение отдается стандартному карманному ингалятору (тяжесть течения БА может обусловить необходимость использования спейсера), то в последующем можно использовать дискхалер, а также дискус – одну из наиболее эффективных систем доставки порошковых форм.
Обязательным условием является также назначение ингаляционных форм пролонгированных симпатомиметиков.
На первом этапе к получаемому больным лечению (системные ГКС, обычно в таблетках) добавляют ИГКС и пролонгированный симпатомиметик.
И если дозировка сальметерола стандартная (2 ингаляции 2 раза в день), то дозировка ФЛ подбирается индивидуально. Обычно стартовая доза ФЛ составляет 500 мкг в сутки, разделенные на 2 приема. Вначале ингалируют пролонгированный бронхолитик, а через 15 мин – ИГКС. После ингаляции обязательно следует прополоскать рот. Если доза получаемого ежедневно системного ГКС высока (это может быть 3 и даже 6 таблеток в день), начальная доза ФЛ повышается. В течение как минимум 2 нед больной принимает комбинацию ИГКС + пролонгированный симпатомиметик, продолжая получать системные ГКС. Связано это с тем, что, несмотря на постоянный прием системных ГКС, БА у этих больных находится вне контроля. Проведенный нами анализ симптомов у больных стероидозависимой БА показал, что 43 пациента из 55 обследованных (80%) пользуются карманным ингалятором более 6 раз в сутки, просыпаются каждую ночь от приступов удушья 26 больных (47%).
На втором этапе через 2–3 нед такой терапии оценивают состояние больного. При отсутствии приступов удушья и нормальных (или оптимальных для пациента) показателях ОФВ1 или ПСВ начинают постепенно снижать суточную дозу системных ГКС, обязательно под контролем (оптимально – пикфлоуметрия), продолжая прием ИГКС и пролонгированного бронхолитика. Темп снижения – индивидуальный. Он зависит от получаемой больным дозы системных ГКС, длительности их приема, особенностей течения БА. До уровня 1,5 таблеток в сутки обычно дозу уменьшают по 0,5 таблетки в 2 нед, затем до уровня 1 таблетки в сутки дозу уменьшают по 0,25 таблетки в 2–3 нед. Все это требует строгого клинического и пикфлоуметрического контроля, любое уменьшение дозы проводится только после визита к врачу, оценки функции внешнего дыхания и при отсутствии клинических и пикфлоуметрических признаков ухудшения состояния больного.
Особенно осторожно следует снижать дозу ниже 1 таблетки в сутки. У пациентов, получавших высокие суточные дозы (или средние суточные дозы, но в течение длительного времени), могут появиться признаки “синдрома отмены” в виде общей слабости, субфебрилитета и других симптомов – помимо обострения БА.
Как правило, с таким явлением нам приходилось сталкиваться при “снятии” больного БА с депонированных инъекционных форм ГКС. В таких случаях мы оставляем пациента на дозе 0,5–1 таблетка в сутки по альтернирующей схеме (через день) и подключаем терапевтические мероприятия, направленные на стимуляцию надпочечников. В этих случаях для полной отмены системных ГКС требуется более длительное время. После полной отмены системных ГКС приступают к постепенному уменьшению дозы ИГКС, не снижая на этих этапах дозу пролонгированного бета2-адреномиметика.
Надо быть готовым к тому, что у больных со стероидозависимой БА после перевода их с таблеток на ИГКС рецидивирует ринит, в том числе полипозная форма. Из 26 пациентов, у которых удалось добиться полной отмены системных ГКС, 20 пациентов испытывают серьезный дискомфорт, связанный с ухудшением носового дыхания. Высокая клиническая эффективность сочетания ИГКС с пролонгированными бета2-агонистами привела к появлению комбинированных препаратов. Один из них – Серетид, содержащий флютиказон и сальметерол одновременно, в 2001 г. зарегистрирован и в России. Опыт его применения за рубежом и в России принес весьма обнадеживающие результаты. Зарегистрированы и другие комбинации ИГКС и пролонгированных бета2-адреномиметиков, в частности Симбикорт (будесонид + формотерол).
Среди перспективных подходов к ведению больных со стероидозависимой БА следует отметить использование гуманизированных мышиных моноклональных анти_IgE_антител – препарата Omalisumab (Xolair) [3]. Хорошие результаты были получены и при использовании небулизируемого лидокаина. Находят подтверждение и данные о роли инфекции Chlamydia pneumoniae у стероидозависимых больных [6].
Таким образом, в настоящее время имеются возможности добиться контроля над тяжелой БА, не прибегая к постоянному приему системных ГКС, а у больных, уже получающих эти препараты, можно существенно снизить их дозу либо отменить полностью.
Комплексный подход, основанный на выяснении и устранении причин стероидной зависимости и адекватной базисной терапии с помощью ИГКС и пролонгированных бета2-адреномиметиков, позволяет добиться желаемого результата у подавляющего большинства стероидозависимых больных БА.
Cписок литературы
1. Чучалин А.Г. и др. // Пульмонология. 1998. Т. 8. № 3. С. 41.
2. Шмушкович Б.И. Клиническая эффективность и механизмы противовоспалительного действия глюкокортикоидных гормонов в лечении бронхиальной астмы // Бронхиальная астма / Под ред. Чучалина А.Г. М., 1997. Т. 2. С. 224.
3. Busse W. et al. // J. Allergy Clin. Immunol. 2000. V. 108. № 2. P. 184.
4. Evans D.J. et al. // Cochrane Database Syst. Rev. 2001. V. 2. CD002985.
5. Evans D.J. et al. // Cochrane Database Syst. Rev. 2001. V. 2. CD0029933.
6. Hahn D.L. et al. // Ann. Allergy Asthma Immunol. 1998. V. 80. № 1. P. 45.
Источник