Диагностические критерии бронхиальной астмы у детей
Бронхиальная астма (БА) детского возраста является серьезной медицинской и социальной проблемой. По распространенности, тяжести течения, сложности диагностики, терапии и реабилитации, социальным и экономическим проблемам БА занимает ведущее место среди «заболеваний века» и недаром названа «парадоксом ХХ столетия» [1, 2, 5].
В.Ф. Лапшин, д.м.н., профессор, заведующий отделом проблем аллергии и иммунореабилитации детей, Т.Р. Уманец, к.м.н., ведущий научный сотрудник, Институт педиатрии, акушерства и гинекологии АМН Украины, г. Киев
тематический номер: ПЕДИАТРИЯ, АКУШЕРСТВО, ГИНЕКОЛОГИЯ
 Это определяется рядом обстоятельств, среди которых можно выделить наиболее важные.
Это определяется рядом обстоятельств, среди которых можно выделить наиболее важные.
Неуклонный рост заболеваемости и смертности. Эпидемиологические исследования в Европе и других регионах мира свидетельствуют, что в течение последних 2-3 десятилетий распространенность БА стремительно прогрессирует. В Украине, по данным официальной статистики, распространенность астмы за последние десятилетия увеличилась в 1,6 раза. В Киеве этот показатель ежегодно возрастает на 5-8%.
Результаты исследований, касающихся БА, указывают на рост частоты смертности, в т. ч. у детей. Группу риска по неблагоприятному исходу БА составляют главным образом пациенты с тяжелой формой заболевания и подростки.
Раннее начало заболевания и сложность диагностики (дифференциальной диагностики). Детская астма может возникнуть в любой период, однако дебют заболевания чаще отмечается в раннем возрасте и в 50-80% случаев – у детей до 5 лет. Именно этот период наиболее трудный в плане верификации диагноза БА. С одной стороны, возникновению бронхиальной обструкции способствуют анатомо-физиологические особенности респираторного тракта ребенка, среди которых наиболее важными являются узость дыхательных путей, преобладание вазосекреторного компонента в развитии воспалительного процесса. С другой стороны, огромный перечень патологических состояний и заболеваний, сопровождающихся синдромом бронхообструкции, кашлем и свистящим дыханием у детей раннего возраста, усложняет дифференциальную диагностику [3].
Поздняя диагностика БА. Остается открытым вопрос запоздалой диагностики БА у детей, в среднем на 4-5 лет, на уровне первичного звена амбулаторной помощи (рис. 1). До сих пор участковые педиатры редко диагностируют БА, диагноз, как правило, устанавливают аллерголог или пульмонолог зачастую тогда, когда заболевание приобретает уже среднетяжелое и тяжелое течение (рис. 2), что существенно влияет на прогноз и исход БА.
Анализ развития и течения болезни, сопоставление диагнозов при поступлении в наши клиники и к моменту выписки позволил нам сгруппировать типичные ошибки. По данным консультативной поликлиники института, они отмечаются более чем в 60% случаев, имеет место как гипо-, так и гипердиагностика БА. Более чем у 50% больных при направлении на консультацию диагноз БА подменяется таким диагнозом, как бронхит – обструктивный, рецидивирующий, хронический или астматический. Следует отметить, что астматический бронхит – это вариант клинического течения БА у детей раннего возраста. Подмена диагноза БА на смягченный «астматический бронхит» успокаивает родителей больного ребенка и дезориентирует врача.
Гиподиагностика БА, по нашему мнению, связана с тем, что не учитываются характерные для аллергических заболеваний анамнестические данные, указания на отягощенную наследственность, имеющиеся у ребенка иные проявления аллергии. Необходимо помнить, что БА – многофакторная патология, поэтому множество факторов риска имеют важное значение в манифестации и прогрессировании заболевания.
БА в детском возрасте отличается многообразием клинических и функциональных проявлений, связанных с возрастом ребенка, тяжестью течения и возможным сочетанием с другими бронхолегочными заболеваниями. Основными клиническими проявлениями БА является триада характерных симптомов: экспираторная одышка, свистящие хрипы, кашель.
Таблица. Факторы риска БА (predictive index) у детей
У детей старшего возраста приступ удушья – кардинальный симптом БА, который чаще возникает в ночное время и выражается экспираторной одышкой с участием вспомогательных мышц. Нередко приступу предшествуют раздражительность, ринорея, зуд, сухое покашливание, боль в животе.
Эквивалентами приступа могут выступать такие симптомы, как эпизоды затрудненного свистящего дыхания с удлиненным выдохом (wheezing); приступообразный сухой кашель, сопровождающийся острым вздутием легких и/или затрудненным выдохом; эпизодические свистящие хрипы в груди; рецидивирующее ощущение сдавливания в грудной клетке. Как атипичный вариант течения БА рассматривается «кашлевой» со спазматическим коклюшеподобным кашлем, который также возникает в ночное время или утром, в ответ на физическую нагрузку, при контакте с аллергеном, при изменении температуры окружающей среды. При этом варианте БА не сопровождается wheezing и приступами удушья.
Астматический статус рассматривается как тяжелое затянувшееся состояние удушья у больного БА, которое характеризуется резистентностью к бронхолитикам, резкой дыхательной недостаточностью, гипоксемией и гиперкапнией, развитием «немого легкого» и отмечается у детей раннего возраста не реже, чем у старших.
Как уже отмечалось, клиническим вариантом течения БА у детей, особенно раннего возраста, является астматический бронхит. Его определяющим симптомом следует признать наличие свистящего удлиненного выдоха – wheezing, который в этом возрасте является таким же кардинальным признаком БА, как удушье у старших детей. Рецидивирование – одна из клинических особенностей данного варианта БА. Критическим периодом для астматического бронхита является возраст до 7 лет. В дальнейшем, особенно у мальчиков, может наступить длительная ремиссия, у части пациентов происходит трансформация в типичные приступы удушья либо обострения могут проходить так же, как и ранее, по типу бронхита.
Наиболее трудно определить диагностические критерии БА у детей раннего возраста [3, 5]. Разнообразные клинические проявления, с которых дебютирует БА у таких детей, значительно усложняют верификацию диагноза. С клинической точки зрения информативными симптомами являются wheezing, экспираторная одышка и повышение воздушности легких. Эти симптомы свидетельствуют о наличии обструкции, но мало специфичны. Афоризм клинических аллергологов звучит так: «Не все то астма, что проявляется свистящими хрипами», но все свистящие хрипы вызваны обструкцией.
Следует отметить, что один из основных критериев БА – рецидивирующий бронхообструктивный синдром (БОС) – в раннем возрасте клинически не различим, независимо от того, развивается ли он на фоне атопии (БА) или в результате воспалительного отека слизистой оболочки, вызванного вирусной инфекцией (обструктивный бронхит). Обструктивные состояния на фоне респираторной вирусной инфекции регистрируют у 10-30% младенцев, и только у 1/3 они являются манифестацией БА [3]. Влияние, которое вирусная инфекция оказывает на астму, зависит от возраста ребенка и, возможно, от вируса. У детей до 2 лет респираторные инфекции, вызванные респираторно-синцитиальным вирусом, являются наиболее частой причиной появления свистящих хрипов и потенциальным фактором, способствующим развитию астмы. У детей старше 2 лет преобладающим возбудителем являются риновирусы, а основным фактором риска появления свистящих хрипов при ОРЗ – аллергические заболевания. Существует большое количество различных состояний, имеющих разную анатомическую локализацию, которые могут приводить к обструкции дыхательных путей и появлению свистящих хрипов [3, 5].
Основными причинами БОС являются:
- обструкция верхних дыхательных путей – постназальный синдром (postnasal drip syndrom), дисфункция голосовых связок, стеноз гортани, эпиглотит, новообразования, риносклерома, обусловленная клебсиеллой, синдром подвижных мягких тканей глотки, рецидивирующий полихондрит, ларинготрахеомаляция, патологическое движение черпаловидного хряща, паралич голосовых связок, артрит перстнечерпаловидного хряща, гранулематоз Вегенера;
- обструкция нижних экстраторакальных дыхательных путей – стеноз трахеи вследствие интубации, аспирация инородного тела, новообразования трахеи и бронхов, загрудинный зоб, трахеобронхомаляция, аномалии сосудистого кольца;
- обструкция нижних дыхательных путей – БА, хроническая обструктивная болезнь легких, отек легких, аспирация (инородное тело, трахеопищеводный свищ, ахалазия кардии, гастроэзофагеальный рефлюкс), воспалительные заболевания бронхолегочной системы, муковисцидоз, паразитарные инвазии, наследственные и врожденные аномалии развития, бронхоэктатическая болезнь.
 Тщательно изученный анамнез может позволить различить состояния, при которых отмечаются свистящие хрипы. Диагноз астмы должен обсуждаться в качестве наиболее вероятного в случаях, когда у ребенка отмечаются эпизодические свистящие хрипы и другие симптомы, выраженность которых уменьшается после обычной противоастматической терапии (главным образом, ингаляционными бронходилататорами).
Тщательно изученный анамнез может позволить различить состояния, при которых отмечаются свистящие хрипы. Диагноз астмы должен обсуждаться в качестве наиболее вероятного в случаях, когда у ребенка отмечаются эпизодические свистящие хрипы и другие симптомы, выраженность которых уменьшается после обычной противоастматической терапии (главным образом, ингаляционными бронходилататорами).
Следует отметить, что БА у детей раннего возраста может дебютировать не только с БОС, но и рецидивов псевдокрупа, рецидивирующего wheezing, немотивированного приступообразного кашля и наиболее редко – с клинически оформленного приступа удушья. Особенностями клинической манифестации БА у данной возрастной группы являются наличие смешанной одышки с преобладанием экспираторного компонента и физикальные данные в виде сочетания диффузных сухих свистящих и разнокалиберных влажных незвучных хрипов.
Несмотря на то что в настоящее время не существует валидных диагностических критериев для установления диагноза БА у детей раннего возраста, зарубежные авторы (Castro-Rodriuer J.A., 2000; Martinez F., 2001; Silverman M., 2001) предлагают ранние большие и малые факторы риска БА, сочетание которых с некоторой вероятностью определяет риск формирования данной патологии у детей [6-9].
Дети с рецидивирующим wheezing, наличием полиорганных проявлений атопии (атопического дерматита и/или аллергического ринита), наличием семейного аллергоанамнеза имеют высокий риск формирования БА. Вероятность диагноза повышается при наличии повышенного содержания IgE и специфических IgE к разным аэроаллергенам, периодичности возникновения признаков, наличии ночной симптоматики, сезонных обострений и симптомов, возникающих после контакта с аллергенами или физического напряжения, эффективности противоастматической терапии.
В исследованиях с участием детей первых 6 лет жизни [7], в которых оценивали прогностическое значение таких симптомов, как кашель, наличие свистящих хрипов на фоне и без ОРВИ, приступы тахипноэ с wheezing, а также комбинацию этих симптомов, установлено, что всех детей, имеющих свистящие хрипы и астмоподобные симптомы в раннем детском возрасте, можно разделить на 2 группы. Первую группу составляют дети с эпизодическими симптомами, обычно связанными с ОРВИ, и имеющие исходно низкие показатели легочной функции по сравнению с аналогичными у их сверстников. У 60% из этих детей wheezing обусловлен малым диаметром дыхательных путей, и в дальнейшем к 6-летнему возрасту они не имеют каких-либо симптомов. К другой группе относятся дети с более поздним началом и персистирующим характером симптомов, с признаками атопии, астмой в семейном анамнезе, в дальнейшем у них развивается БА.
У детей с продуктивным кашлем, рецидивирующей инфекцией дыхательных путей, началом симптомов в неонатальном возрасте и задержкой развития, наличием периодической рвоты, локальной легочной симптоматикой необходимо проводить дифференциальную диагностику с альтернативным диагнозом. Возможности проведения диагностического поиска определяются возрастом ребенка.
Необходимый объем диагностических процедур у детей до 5-летнего возраста включает: исследования хлоридов пота, рентгенографию органов грудной клетки и придаточных пазух носа, эзофагографию, рН-метрию, иммунологическое обследование на наличие первичного иммунодефицита, исследование реснитчатого эпителия, бронхоскопическое обследование. У детей старше 5 лет возможно проведение аллергологического обследования (прик-тесты с аллергенами, уровень специфических IgE), определение функции внешнего дыхания (спирометрия с проведением бронхолитического теста и бронхопровокационных проб).
Среди дополнительных диагностических критериев БА у детей выделяют [4]:
- рентгенологические – во время обострений выявляют признаки острой эмфиземы, иногда так называемый среднедолевой синдром, исчезающий после купирования острого приступа и лечения; в период ремиссии – признаки хронического бронхита, при тяжелом течении астмы – признаки хронической эмфиземы;
- функциональные – наличие признаков бронхиальной обструкции: снижение пиковой объемной скорости выдоха (ПОСВ) и объема форсированного выдоха за 1-ю с (ОФВ1) <80% от должных, суточная вариабельность ПОСВ >20%, обратимость бронхиальной обструкции (ОФВ1) при проведении бронхолитического теста – >12% (150 мл) после ингаляции 200-400 мкг сальбутамола; наличие гиперреактивности бронхов по данным спирометрии с использованием бронхопровокационных фармакологических проб с метахолином, гистамином, гипертоническим раствором натрия хлорида и нефармакологических (с физической нагрузкой). Стандартизированными, наиболее высокочувствительными считаются пробы с гистамином (чувствительность – 81-89%) и метахолином (91-97%). Тест с физической нагрузкой недостаточно стандартизирован, но более специфичен. Противопоказаниями для проведения бронхопровокационных проб являются: ОФВ1 <67%, наличие обструкции, 2-недельный срок после перенесенной ОРВИ, эпилепсия, аневризма, обострение астмы;
- лабораторные критерии (маркеры аллергического воспаления): эозинофилия (системная и секреторная – рис. 3), определение NO, H2O2 в выдыхаемом воздухе. В настоящее время широко используют неинвазивные методики определения маркеров воспаления, что особенно важно в детском возрасте. При этом материалом для исследования служит индуцированная мокрота и конденсат выдыхаемого воздуха;
- алергологические: положительные результаты кожных тестов, повышенный уровень IgE (свидетельствует о наличии атопического статуса, 30% популяции атопики, не является специфичным показателем). При невозможности проведения кожной диагностики определяют специфические IgE, отражающие наличие и уровень сенсибилизации к аллергенам (по информативности уступает кожным тестам).
Таким образом, тщательно изученный анамнез заболевания, учет указанных особенностей клинического течения БА в детском возрасте, исключение альтернативного диагноза, наличие дополнительных критериев позволит своевременно верифицировать диагноз БА у детей. Сложности диагностики БА в детском возрасте определяются ее клинической вариабельностью, с одной стороны, и клинической схожестью с многими заболеваниями, невозможностью в определенном возрасте провести дополнительные диагностические процедуры, недооценкой педиатрами эквивалентов симптомов БА – с другой.
Специфика врачебной деятельности, ее непосредственная связь со здоровьем и жизнью человека побуждают анализировать заболевание, не допускать ошибок в диагностике и своевременно проводить адекватную терапию.
Литература
- Ласица О.И., Ласица Т.С. Бронхиальная астма в практике семейного врача. – К. :ЗАО «Атлант UMS», 2001. – 263 с.
- Огородова Л.М., Астафьева Н.Г. Факторы риска астмы // Consilium medicum. – 2001 (прил.). – С. 4-8.
- Смоленов И.В., Смирнов Н.А. Подходы к диагностике заболеваний, сопровождающихся свистящими хрипами // Consilium medicum. – 2001 (прил.). – С. 21-24.
- Протокол діагностики та лікування бронхіальної астми у дітей / Наказ МОЗ України від 27.12.2005, № 767.
- From atopic dermatitis to asthma / J. Bousquet, G. Dutau, A. Grimfeld, Y. Prost, 2002. – 163 p.
- Martinez F.D. Definition of pediatric asthma and associated risk factors. Pediatr. Pulmonol., 1997; Suppl. 15: 9-12.
- Мartinez F.D., Wright A.L., Tausig L.M. et al. Asthma and wheezing in the first six years of life. N. Engl. J. Med. 1995; 332: 133-138.
- Silverman M. Markers of early asthma. Parallel session «Asthma and allergy – early markers and predictors» in Paediatric Respiratory and Allergy Congress. – April 1-4, 2001; Praque.
- Castro-Rodriquer et al. A clinical index to define risk of asthma in young children with recurrent wheezing. Am. Respir. Crit. Care Med. 2000; 162 (4Pt 1): 1403-1406.
Источник
- Авторы
- Резюме
- Файлы
- Ключевые слова
- Литература
Федоров И.А.
1
Рыбакова О.Г.
1
1 ФГБОУ ВО «Южно-Уральский государственный медицинский университет» Министерства здравоохранения Российской Федерации
Диагностика бронхиальной астмы у детей раннего возраста остается сложной задачей для врачей первичного звена здравоохранения. Когортное исследование уровня эозинофилов индуцированной мокроты проводилось в течение 10 лет, под наблюдением находилась группа 75 детей в возрасте от 1 года до 5 лет (средний возраст 2,8±1,2 года) с острым обструктивным бронхитом в анамнезе. Исследование проводили поэтапно. Повторное обследование детей проведено через 18 месяцев и через 10 лет от начала исследования. По окончании наблюдения пациенты были разделены на две группы. Первая группа (n=46) – дети, у которых бронхиальная астма не сформировалась за время исследования. Вторая группа (n=29) – дети со сформировавшейся бронхиальной астмой. На втором этапе работы проводилось сравнение лабораторных показателей, из алгоритма диагностики БА у детей: уровень эозинофилов общего анализа крови, уровень общего иммуноглобулина Е крови и уровень эозинофилов индуцированной мокроты по таким показателям, как чувствительность и специфичность. Было доказано, что уровень эозинофилов индуцированной мокроты ≥5% является специфичным, чувствительным и воспроизводимым маркером бронхиальной астмы и может быть использован для дифференциальной диагностики бронхиальной астмы и острого обструктивного бронхита.
эозинофилы
индуцированная мокрота
дети
острый обструктивный бронхит
бронхиальная астма
1. Национальная программа «Бронхиальная астма у детей. Стратегия лечения и профилактика». – 5-е изд., перераб. и доп. – М.: Оригинал-макет, 2017. – 160 с.
2. Горлова Н.В. Диагностические возможности компьютерного комплекса «Паттерн» в оценке функции внешнего дыхания у детей / Н.В. Горлова, А.Н. Узунова, М.Л. Зайцева // Человек. Спорт. Медицина. – 2006. – № 3. — C. 215-217.
3. Гиниатуллин Р.У. Морфологические аспекты патогенеза атопической бронхиальной астмы тяжелого течения у детей / Р.У. Гиниатуллин, Я.И. Жаков, И.А. Федоров // Педиатрия. – 1997. — Т. 76, № 5. — С. 4-8.
4. Global Initiative for Asthma. Global Strategy for asthma management and prevention. – URL: https:// www.ginasthma.com. (дата обращения: 14.01.2018).
5. Жаков Я.И. Клинико-анамнестические и лабораторные особенности у детей групп риска по формированию бронхиальной астмы / Я.И. Жаков, О.Г. Рыбакова, Е.Е. Минина и др. // Сибирский мед. журн. (Иркутск). – 2015. — № 5. – С. 31-34.
6. Мизерницкий Ю.Л. Дифференциальная диагностика и дифференцированная терапия острой бронхиальной обструкции при ОРВИ у детей раннего возраста // Практическая медицина. – 2014. — № 9 (85). – С. 82-88.
7. Федоров И.А. Диагностика бронхиальной астмы у детей, перенесших эпизоды острого обструктивного бронхита в дошкольном возрасте, по результатам десятилетнего наблюдения / И.А. Федоров, О.Г. Рыбакова, О.Г. Степанов // Человек. Спорт. Медицина. – 2017. – Т. 17, № 1. – С. 28-35.
8. Brozek G. Childhood asthma prevalence and risk factors in three Eastern European countries — the Belarus, Ukraine, Poland Asthma Study (BUPAS): an international prevalence study / G. Brozek, J. Lawson, A. Shpakou [et al.] // BMC Pulm Med. – 2016. – Vol. 16, № 1. – P. 11-16.
9. Жаков Я.И. Клиническая информативность метода индуцированной мокроты при бронхиальной астме у детей / Я.И. Жаков, Ю.Л. Мизерницкий, Е.Е. Минина и др. // Пульмонология детского возраста: проблемы и решения. — 2009. — № 9. – С. 120-124.
10. Wenzel S.E. Asthma phenotypes: the evolution from clinical to molecular approaches // NatMed. – 2012. – Vol. 18. – P. 716-725.
11. Staticescu S. The value of induced sputum in the diagnosis and management of children with bronchial asthma / S. Staticescu, P. Chereches-Panta, G. Ichim et al. // Clujul Medical. — 2014. — Vol. 87 (3). — Р. 171-176.
12. Wang F. Different inflammatory phenotypes in adults and children with acute asthma / F. Wang, X.Y. He, K.J. Baines [et al.] // Eur. Respir. J. – 2011. – Vol. 38, № 3. – P. 567-574.
13. Vijverberg S. Clinical utility of asthma biomarkers: from bench to bedside / S.Vijverberg, B.Hilvering, Jan AM. Raaijmakers et al. // Biologics. — 2013. – Vol. 7. – P. 199–210.
14. Walford H.H. Diagnosis and management of eosinophilic asthma: a US perspective / H.H. Walford, A.T. Doherty // J. Asthma Allergy. – 2014. – Vol. 7. – P. 53-65.
Диагноз «бронхиальная астма» (БА) у детей раннего возраста является клинико-анамнестическим, так как не все существующие методы лабораторной и функциональной диагностики могут использоваться в практике врача-педиатра либо в связи с их дороговизной и трудоемкостью, либо вследствие возрастных ограничений [1-3]. Особенности течения БА у детей дошкольного возраста и отсутствие специфических методов диагностики приводят к определенным трудностям у врачей первичного звена здравоохранения при постановке диагноза [1; 4; 5]. Популяционные исследования, которые регулярно проводятся в мире, демонстрируют, что, несмотря на существующий прогресс в изучении и ведении бронхиальной астмы, все еще сохраняется гиподиагностика этого заболевания у детей раннего возраста [1; 4; 6]. Основные трудности возникают при дифференциальной диагностике острого обструктивного бронхита (ООБ) и БА, особенно при первых их проявлениях [1; 7]. Вирусная инфекция является как этиологическим фактором ООБ, так и самым частым триггером БА у детей дошкольного возраста. И в том и в другом случае развивается синдром бронхиальной обструкции, который у детей этой возрастной группы имеет схожие клинические проявления, одинаковые рентгенологические, функциональные и лабораторные изменения [1; 7; 8]. Также обращает на себя внимание субъективность оценки ряда клинических параметров (тяжесть течения обструктивного синдрома, ответ на терапию), отданных на откуп врачу, который на своем рабочем месте, ограниченный временем приема, должен решать как «более» или «менее» выражен тот или иной симптом. В результате практически ни один из этих показателей не может служить достоверным дифференциально-диагностическим критерием ООБ и БА. Заболевание не диагностируется, больные не получают своевременно базисную терапию, что приводит к снижению качества жизни, образования и может приводить к росту инвалидизации от БА. Необходимость разработки новых диагностических критериев позволила нам более десяти лет назад модифицировать и внедрить в алгоритм диагностики бронхиальной астмы у детей раннего возраста метод индуцированной мокроты (ИМ) [9]. В детской практике методы оценки воспаления слизистой оболочки дыхательных путей должны быть простыми, неинвазивными, дающими возможность многократного проведения с отсутствием противопоказаний, ограничений и возможных осложнений. Многие методы являются трудоемкими, устаревшими, не информативными, сложными, инвазивными, очень дорогостоящими и не могут претендовать на роль релевантных. Метод индуцированной мокроты, «пришедший» в педиатрию из взрослой службы, является безопасной процедурой, которая обеспечивает многофункциональной информацией о воспалительном процессе на уровне слизистой оболочки бронхиального дерева, в частности по эозинофильному воспалению, его динамике на фоне лечения, т.е. может являться средством лабораторной диагностики и мониторирования БА во время лечения [9-11].
Цель исследования. Оценить эффективность определения уровня эозинофилов индуцированной мокроты как дополнительного диагностического критерия бронхиальной астмы.
Материалы и методы. Когортное исследование уровня эозинофилов индуцированной мокроты проводилось в течение 10 лет, под наблюдением находилась группа 75 детей в возрасте от 1 года до 5 лет (средний возраст 2,8±1,2 года.) с ООБ в анамнезе, сформированная методом случайной выборки из детей, перенесших один и более эпизодов острого обструктивного бронхита, обратившихся на прием к врачу-аллергологу с целью обследования для исключения бронхиальной астмы. На всех детей была заполнена персональная анкета, содержащая данные анамнеза, объективного осмотра и результаты проведенных исследований. Всем респондентам в декретированные сроки был проведен цитологический анализ назального секрета, индуцированной мокроты, исследование уровня общего IgE крови, уровня эозинофилов крови. Для получения мокроты с целью ее цитологического анализа проводили процедуру индукции мокроты [9; 11; 12]. В данном исследовании за диагностически значимый уровень эозинофилов индуцированной мокроты принят показатель ≥ 5%. Из исследования исключались пациенты с подтвержденной паразитарной инфекцией.
Исследование проводили поэтапно. Повторное обследование детей проведено через 18 месяцев и через 10 лет от начала исследования. По окончании наблюдения пациенты были разделены на две группы. Первая группа (n=46) – дети, у которых бронхиальная астма не сформировалась за время исследования. Вторая группа (n=29) – дети со сформировавшейся бронхиальной астмой.
Статистический анализ полученных результатов проводился при помощи пакетов статистических программ STATISTICA 6.0 (StatSoft, 2001) и SPSS 12.0. Для описания количественных признаков в выборке рассчитывались медиана и квартили (Ме; 25-75%). Для сравнительного анализа данных в двух зависимых группах при распределении количественных признаков, отличных от нормального, использовался критерий Вилкоксона. С целью оценки клинической информативности диагностических тестов проводился ROC-анализ и анализ четырехпольной таблицы для оценки чувствительности и специфичности диагностического критерия. Для всех видов анализа статистически достоверными считались значения p<0,05.
Результаты и обсуждения. За первый год наблюдения детей с эпизодами ООБ в анамнезе БА сформировалась примерно у каждого пятого ребенка (17% детей). Через 2 года диагноз БА имел уже каждый третий ребенок (33% детей), через 3,5 года БА была диагностирована в общей сложности у 36% детей, через десять лет — у 39% детей, что соответствует статистическим данным других исследователей [1; 6].
При сравнении детей 2 группы с детьми 1 группы по уровню эозинофилов ИМ и его динамике за первые 18 месяцев наблюдения было выявлено, что у детей первой группы уровень эозинофилов ИМ в начале исследования был диагностически не значимым (Ме; 25-75%) — 1,0 (0,0-4,0) и в динамике, через 18 месяцев наблюдения, статистически значимо не изменился – 2,0 (1,0-3,0) (рwilc.>0,05). У детей второй группы уровень эозинофилов ИМ был изначально высоким — 6,0 (2,4-17,0), и отмечался его статистически значимый рост в динамике через 18 месяцев наблюдения – 12,0 (4,0 — 22,0) (рwilc.<0,05). Также наблюдали следующую закономерность: у детей, имевших через 18 месяцев наблюдения уровень эозинофилов ИМ ≥5%, независимо от исходного уровня эозинофилов ИМ (<2,5% или ≥2,5%) сформировалась БА в 95,2% случаев. У детей с исходным уровнем эозинофилов ИМ <2,5%, имевших через 18 месяцев уровень эозинофилов ИМ <5%, в 80,8% случаях не сформировалась БА в отдаленные сроки наблюдения. Связь между уровнем эозинофилов ИМ и наличием БА также была отмечена в работах иностранных исследователей [10; 11; 13].
На втором этапе работы проводилось сравнение лабораторных показателей, из алгоритма диагностики БА у детей: уровень эозинофилов общего анализа крови, уровень общего иммуноглобулина Е крови и изучаемого показателя — уровня эозинофилов индуцированной мокроты по таким критериям, как чувствительность и специфичность. Для этого мы сопоставили результаты лабораторных методов исследования у детей двух групп. Полученные результаты представлены в таблице. Следует отметить, что в этом случае нами использованы не исходные результаты обследования, а данные, полученные при исследовании, проведенном через 18 месяцев, то есть когда БА у детей сформировалась.
Анализ основных лабораторных показателей у детей в зависимости от наличия/отсутствия бронхиальной астмы
Показатели | Бронхиальная астма есть (n=46) | Бронхиальной астмы нет (n=29) | Всего |
Уровень эозинофилов ОАК (n=46) | |||
Эозинофилы ОАК ≥5 % | 17-77,3% | 5-22,7% | 22 |
Эозинофилы ОАК <5 % | 15-62,5% | 9-37,5% | 24 |
Уровень общего IgE крови (n=74) | |||
≥100 МЕ/мл | 25-86,2% | 4-13,8 | 29 |
<100 МЕ/мл | 21-46,7% | 24-53,3% | 45 |
Уровень эозинофилов индуцированной мокроты (n=75) | |||
Эозинофилы ИМ ≥5 % | 44-95,6% | 2-4,4% | 46 |
Эозинофилы ИМ < 5% | 2-6,9% | 27-93,1% | 29 |
При оценке диагностической ценности такого параметра, как уровень эозинофилов ОАК, было выявлено отсутствие статистически значимых различий в вероятности наличия БА у детей из групп риска (эпизоды ООБ в анамнезе) при уровне эозинофилов ОАК ≥5% (77,3%) и вероятности таковой при уровне эозинофилов ОАК < 5% (62,5%). В отношении повышенного уровня общего IgE крови и уровня эозинофилов ИМ различия были статистически значимыми (р<0,001), однако наиболее высокие чувствительность, специфичность и соответственно прогностическая ценность положительного результата и прогностическая ценность отрицательного результата были у уровня эозинофилов ИМ. Так, чувствительность, то есть доля лиц с положительным результатом теста (уровень эозинофилов ИМ ≥ 5%) среди лиц с изучаемым заболеванием, составила в данном случае, так же как и прогностическая ценность положительного результата, 95,6%. Специфичность, то есть доля лиц с отрицательным результатом теста, среди лиц без изучаемого заболевания составила, так же как и прогностическая ценность отрицательного результата, 93,1%. Диагностическая эффективность уровня эозинофилов ИМ ≥5% составила 94,4%, что оценивается как высокая [9; 11].
Повышенный уровень общего IgE крови (≥ 100 МЕ/мл) свидетельствовал о вероятности БА в 86,2% случаев, что статистически значимо меньше (р<0,05), чем при наличии уровня эозинофилов ИМ ≥5%. У детей из группы риска по развитию БА при уровне общего IgE крови < 100 МЕ/мл вероятность наличия БА — 46,7%, то есть достаточно высокая, что не позволяет считать данный признак диагностическим критерием БА у детей групп риска. Комплексный учет всех трех лабораторных методов (эозинофилы ИМ, эозинофилы ОАК, общий IgE крови) не повышает предсказательной способности изолированного определения уровня эозинофилов ИМ.
Для наглядного выражения соотношения между чувствительностью и специфичностью теста по определению уровня эозинофилов в ИМ с целью диагностики БА у детей раннего возраста было проведено построение ROC-кривой (ROC – Receiver operating characteristic curve) (рис. 1). Для получения численного значения клинической значимости теста используется показатель AUC (Area Under Curve). Судить о качестве теста можно по экспертной шкале для значений AUC. Характеристика качества метода диагностики может быть представлена в виде площади под ROC-кривой — AUC-ROC: >1,0-0,9 – отличное, 0,9-0,8 – очень хорошее, 0,8-0,7 – хорошее, 0,7-0,6 – среднее, 0,6-0,5 – метод неинформативен. Таким образом, чем больше эта площадь, тем эффективнее метод диагностики. В данном исследовании AUC-ROC (рис. 1) площадь под кривой равна 0,944, что говорит о высокой диагностической эффективности этого метода – 94,4%. В аналогичных исследованиях с участием детей старше 5 лет и взрослых было продемонстрировано, что процент эозинофилов в мокроте является наиболее чувствительным и специфичным маркером в сравнении с эозинофилией крови и уровнем общего IgE крови при БА [12-14].
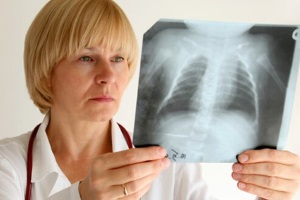
Для того чтобы была возможность сравнить чувствительность и специфичность использующихся в настоящее время показателей для диагностики БА, было проведено построение ROC-кривой по другим диагностическим тестам. Построены ROC-кривые диагностики по уровню эозинофилов ОАК (%) и общему IgE крови (МЕ/мл). Эти показатели были использованы, так как они являются лабораторными критериями, отражающими наличие аллергии и/или атопии, и используются врачами педиатрами и аллергологами при постановке диагноза БА (рис. 2, 3).
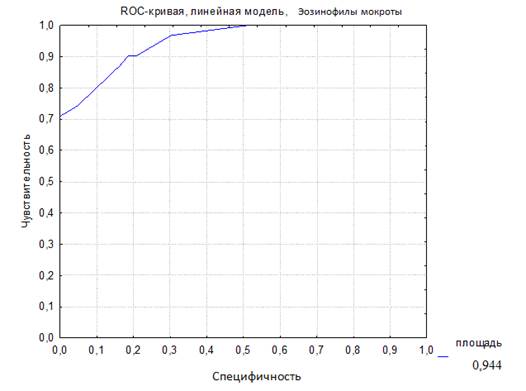
Рис. 1. ROC-кривая диагностической эффективности уровня эозинофилов индуцированной мокроты (AUC-ROC 0,944)

Рис. 2. ROC-кривая диагностической эффективности уровня эозинофилов в общем анализе крови (AUC-ROC 0,61)
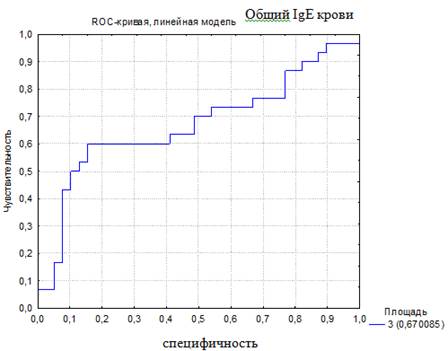
Рис. 3. ROC-кривая диагностической эффективности уровня общего IgE крови
(AUC-ROC 0,67)
Таким образом, полученные результаты помогут врачу определиться с количественной оценкой такого критерия, как уровень эозинофилов мокроты, так как даже в пятом пересмотре Национальной программы «Бронхиальная астма у детей. Стратегия лечения и профилактика» (2017) говорится о качественной оценке этого показателя: «у детей с БА средний уровень эозинофилов в индуцированной мокроте достоверно выше и превышает показатели у здоровых». В то же время что такое средний уровень и его количественное отображение не приводится. По данным этого исследования установлено, что уровень эозинофилов ИМ ≥5% является чувствительным и специфичным маркером и поэтому рекомендован для диагностики БА у детей.
Библиографическая ссылка
Федоров И.А., Рыбакова О.Г. РАННЯЯ ДИАГНОСТИКА БРОНХИАЛЬНОЙ АСТМЫ У ДЕТЕЙ МЛАДШЕ 5 ЛЕТ // Современные проблемы науки и образования. – 2018. – № 2.;
URL: https://science-education.ru/ru/article/view?id=27492 (дата обращения: 12.07.2020).

Предлагаем вашему вниманию журналы, издающиеся в издательстве «Академия Естествознания»
(Высокий импакт-фактор РИНЦ, тематика журналов охватывает все научные направления)
Источник