Глюкокортикоиды при бронхиальной астме механизм


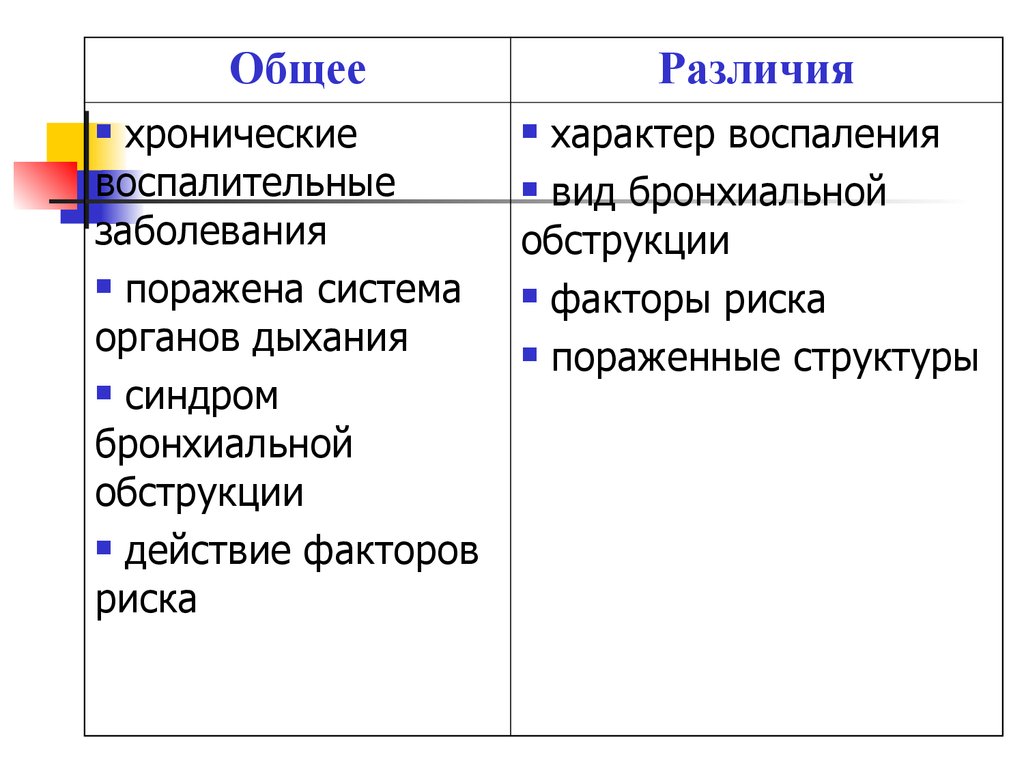
Бронхиальной астмой называют хроническое заболевание дыхательной системы, при котором отмечается сильное сужение бронхов. Гормоны при астме нужны для оказания противовоспалительного и антиаллергического эффекта.
В базисную терапию астмы включены глюкокортикостероиды. Если их не применять для лечения заболевания, сильно возрастает зависимость от симптоматических бронходилататоров. Это является признаком неконтролируемого течения астмы.
Что такое глюкокортикостероиды

Глюкокортикостероиды — это гормоны, производимые корой надпочечников. В организме человека вырабатывается кортизол, кортикостерон.
Разностороннее воздействие на организм этих биологически активных веществ позволило активно использовать их в лечении различных заболеваний, в том числе астмы.
Сейчас существует ряд фторированных и нефторированных синтетических глюкокортикоидов. В отличие от природных, они обладают большей активностью, поэтому действуют более эффективно.
Механизм действия ГКС
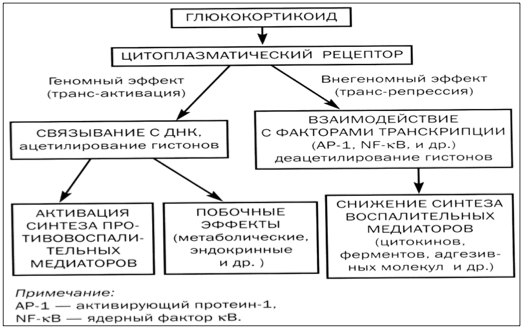
Для полного понимания, почему так активно используют гормоны от астмы, важно знать их механизм действия. В клетках человеческого организма существуют специальные рецепторы, с которыми глюкокортикостероиды связываются, проникая в цитоплазму.
Полученный в результате этого взаимодействия комплекс проникает внутрь ядра, где воздействует непосредственно на ДНК. Это позволяет активировать процесс образования различных белков:
- липокортин-1. Его действие направлено на торможение продукции арахидоновой кислоты, из которой синтезируются медиаторы воспаления;
- нейтральная эндопептидаза. Нужна для разрушения кининовых комплексов, принимающих участие в развитии воспалительного процесса;
- интерлейкин-10, оказывающий противовоспалительное действие;
- ингибитор ядерного фактора. Играет важную роль в торможении воспалительного процесса бронхов.
За счет действия комплекса гормон-рецептор наблюдается выраженное торможение образования активизирующих воспалительный процесс белков.
Глюкокортикоиды благодаря своим свойствам отлично помогают при бронхиальной астме, давая выраженный противовоспалительный эффект.
Использование глюкокортикостероидов при лечении астмы
Применение глюкокортикоидов при бронхиальной астме является традиционным методом лечения данного заболевания. Их использование началось еще в середине 40-х годов ХХ века, после того, как Ф. Хенч и Э. Кендэлл смогли искусственно синтезировать ГКС.
Поняв, что глюкокортикостероиды помогают в контроле воспалительного процесса при гормональной астме, они начали активно тестировать их при лечении заболевания, однако отметили большое количество побочных эффектов и временно прекратили их использование.
В современной медицине астматикам назначается два типа гормональных препаратов: ингаляционные и системные ГКС.
Ингаляционные ГКС

Главные преимущества, объясняющие широкое применение ингаляционных глюкокортикостероидов (ИГКС) для лечения бронхиальной астмы, — высокая липофильность, малый период полувыведения, а также быстрая инактивация.
В клинической практике используются следующие ИГКС:
- беклометазона дипропионат;
- будесонид;
- мометазона фуроат;
- флутиказона пропионат;
- циклесонид.
Механизм действия ИГКС при бронхиальной астме основан на их высокой липофильности. Эпителий человеческих бронхов покрыт незначительным слоем жидкости.
Поэтому не все вещества могут быстро проникнуть сквозь этот барьер. Липофильность позволяет препарату быстро достичь слизистой оболочки бронхов и проникнуть в кровеносную систему.
Эффект от применения ингаляционных глюкокортикоидов напрямую зависит от того, каким методом они были доставлены в организм.
Так, при использовании ингаляторов с аэрозолями большая часть препарата оседает в ротовой полости либо проглатывается. Лишь 10% достигает непосредственно слизистой оболочки бронха.
При вдыхании препарата через спейсер — около 5%. В системный кровоток ИГКС попадают в виде неактивных продуктов обмена, за исключением беклометазона. Также применяется введение препаратов через небулайзер для определенных групп пациентов, а именно:
- дети;
- пожилые люди;
- люди с нарушениями сознания;
- больные с сильной бронхиальной обструкцией.
Согласно ряду клинических испытаний, ингаляционные глюкокортикостероиды крайне эффективны при бронхиальной астме.
Системные глюкокортикоиды

Системные глюкокортикостероиды (СГКС) не являются препаратами экстренной помощи при бронхиальной астме, однако они крайне важны для проведения терапевтических мероприятий во время обострений. В целом они нужны для повышения качества жизни пациента и не обладают быстрым эффектом.
Согласно глобальной стратегии ВОЗ, крайне важно применять СГКС при всех обострениях астмы, за исключением самых легких. Особенно это касается следующих случаев:
- после введения ИГКС не отмечается улучшения состояния пациента;
- приступ начался, несмотря на прием ИГКС;
- требуется увеличение дозы ИГКС;
- состояние пациента постоянно ухудшается;
- снижение реакции организма на действие ИГКС;
- снижение пикфлоуметрических показателей (ПСВ ниже 60%)
Отмечается, что для длительной терапии лучше применять СГКС в форме таблеток, внутривенное введение чаще используется при приступе. Основные глюкокортикостероиды, использующиеся для системной терапии при бронхиальной астме, — это преднизолон и гидрокортизон.
При пероральном приеме отмечается крайне высокая биодоступность. Максимальная концентрация препаратов в крови при внутривенном введении достигается менее чем через час после попадания в организм.
В печени данные лекарственные средства метаболизируются, а затем выводятся вместе с мочой.
Побочные действия глюкокортикостероидов

При лечении больных гормонозависимой бронхиальной астмой важно помнить, что ГКС обладают рядом побочных эффектов, которые можно разделить на две группы:
- Развивающиеся во время терапии заболевания.
- Развивающиеся после прекращения лечения (синдром отмены).
К первой группе можно отнести следующие последствия:
- метаболические нарушения;
- повышение артериального давления;
- снижение иммунного статуса;
- язвенная болезнь;
- миопатия;
- расстройства психики;
- нарушения роста у детей;
- кушингоид.
Метаболические нарушения проявляются в виде гипергликемии, нарушении жирового, а также водно-электролитного обмена. Повышение уровня сахара в крови связано с тем, что на фоне приема ГКС отмечается увеличение устойчивости тканей к действию инсулина.
При этом данное состояние наблюдается достаточно редко, и к нему более склонны люди, которые, помимо гормональной астмы, болеют сахарным диабетом.
Нарушение обмена жиров проявляется в том, что на лице и туловище наблюдается чрезмерное развитие жировой ткани. Развивается так называемый кушингоидный хабитус.
Нарушения водного и минерального обмена проявляются в виде задержки воды в организме и потери кальция и калия.
Артериальная гипертензия при приеме ГКС связана с их воздействием на стенки сосудов. Развивается при длительном лечении большими дозами препаратов.
Еще реже возникает язвенная болезнь. Именно поэтому, все больные, которые применяют в лечении астмы СГКС, должны проходить обследования на предмет наличия язв в желудке.
У некоторых больных, применяющих ГКС, может возникнуть мышечная слабость, вплоть до полной атрофии. Это напрямую связано с влиянием препаратов на минеральный обмен. Также миопатия может наблюдаться при кушингоиде, поэтому ее нельзя называть специфичным побочным эффектом.
Легкие нарушения психического состояния могут наблюдаться в самом раннем начале терапии ГКС. Так, у больных отмечаются нервозность, частая смена настроения, а также нарушения сна. Стероидные психозы развиваются крайне редко.
У детей при использовании СГКС может отмечаться нарушение роста. В особенности этому подвержены мальчики. Считается, что патология связана с нарушением продукции половых гормонов.
При синдроме отмены наблюдается повышенная утомляемость, отсутствие аппетита, лихорадка, тошнота, а также сильные головные боли. В некоторых случаях может проявиться недостаточность надпочечников. Крайне редко наблюдается клиника псевдоопухоли мозга.
Возможно ли лечение астмы без применения гормонов

Первое, что должны понимать люди, больные гормонозависимой бронхиальной астмой, — нельзя самостоятельно отказываться от применения ГКС. Лечение должно быть системным и проходить под контролем специалиста.
Если говорить о лечении астмы без гормональных препаратов, то нужно вспомнить о такой группе лекарств, как кромоны. Нужно понимать, что данные лекарственные средства в большей мере обладают профилактическим, а не лечебным эффектом.
Их рекомендуется применять в период ремиссии. Существует много форм кромонов, однако лучший эффект достигается при применении при помощи ингаляторов. Они обладают рядом преимуществ:
- простота применения;
- отсутствие привыкания;
- минимальный риск побочных эффектов.
Благодаря своим свойствам препараты кромоглициевой кислоты отлично подходят для профилактики приступов астмы у детей, страдающих легкой формой заболевания. В соответствии с глобальной стратегией ВОЗ, они являются препаратом выбора.
Согласно проведенным исследованиям, если при средней тяжести и тяжелом течении астмы применение ИГКС не вызывает вопросов, то на начальных стадиях их употребление не оправдано.
Лечение астмы без гормонов у взрослого человека, который уже длительное время применял стероиды, практически невозможно.
В заключение
Медикаментозные средства, такие как ИГКС и СГКС, при лечении бронхиальной астмы важно применять под контролем лечащего врача. Препараты необходимо подбирать индивидуально, а само лечение должно носить системный характер.
При обострениях БА рекомендуется использовать ИГКС для снятия приступа, а затем, при необходимости подключать СГКС. Несмотря на риск развития побочных эффектов, данные средства являются оптимальным вариантом лечения астмы.
Источник
Медицинский эксперт статьи

х
Весь контент iLive проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
Для лечения больных бронхиальной астмой наиболее приемлемы препараты группы преднизолона и триамцинолона.
При очень тяжелом течении бронхиальной астмы и при отсутствии эффекта от остальных методов лечения рекомендуется применять препараты короткого действия (преднизон, преднизалон, метилпреднизолон).
Показания
Системная глюкокортикоидная терапия проводится только по строгим показаниям:
- очень тяжелое течение бронхиальной астмы при отсутствии эффекта от всех остальных методов лечения;
- кортикозависимая бронхиальная астма (т.е. когда больной уже длительно лечится глюкокортикоидами и в данный момент отменить их невозможно);
- астматический статус (глюкокортикоиды применяются парентерально);
- кома при бронхиальной астме (глюкокортикоиды применяются парентерально);
 [1], [2], [3], [4], [5], [6], [7], [8]
[1], [2], [3], [4], [5], [6], [7], [8]
Схема лечения
Системная глюкокортикоидная терапия обладает следующими механизмами действия:
- стабилизирует тучные клетки, предупреждает ихдегрануляцию и выход медиаторов аллергии и воспаления;
- блокируют образование IgE (реагинов);
- подавляют позднюю астматическую реакцию, что обусловлено подавлением клеточной воспалительной реакции вследствие перераспределения лимфоцитов и моноцитов, угнетением способности нейтрофи-лов к миграции из сосудистого русла, перераспределением эозинофилов. Поздняя астматическая рекция начинается через 3-4 ч после воздействия аллергена, максимум ее наблюдается через 12 ч, продолжается более 12 ч; она отражает механизмы прогрессирования бронхиальной астмы. Гиперреактивность бронхов, сохраняющаяся длительно (в течение недель и месяцев), связана с поздней астматической реакцией;
- стабилизируют лизосомальные мембраны и уменьшают выход лизосомальных ферментов, повреждающих бронхопульмональную систему;
- подавляют сосудорасширяющее действие гистамина;
- увеличивают количество и чувствительность бета-адренорецепторов бронхов к бронхорасширяющим воздействиям адреномиметаков;
- уменьшают отек слизистой оболочки бронхов;
- повышают активность эндогенных катехоламинов;
После проникновения в клетку глюкокортикоиды связываются со специфическими цитоплазматическими рецепторами, образуя комплекс гормон-рецептор, взаимодействующий в ядре клетки с хроматином. В результате активируется синтез белков, опосредующих эффекты глюкокортикоидов. Весь процесс занимает около 6 ч, поэтому глюкокортикоиды не купируют приступы удушья при обострении бронхиальной астмы, они действуют не ранее 6 ч после их введения.
Используются 3 группы глюкокортикоидов:
- группа преднизолона: преднизолон (таблетки по 0.005 г; ампулы по 1 мл с содержанием 30 мг препарата); метилпреднизолон (метипред, урбазон — таблетки по 0.004 г);
- группа триамцинолона: триамцинолон, кенакорт, полькортолон, берликорт (таблетки по 0.004 г);
- группа дексаметазона: дексаметазон, дексон, дексазон (таблетки по 0.0005 г; ампулы для внутривенного и внутримышечного введения по 1 и 2 мл 0.4%-раствора с содержанием препарата 4 и 8 мг соответственно).
Методика лечения по М. Э. Гершвину (1984):
- при обострении начинать с высоких доз (например, 40-80 мг преднизолона ежедневно);
- после уменьшения симптомов — медленно снижать дозу (в течение 5-7 дней) до поддерживающей, например, на 50% каждый день;
- для хронического (длительного) лечения применять ежедневную дозу преднизолона ниже 10 мг;
- принимать препарат в первой половине дня;
- в начале лечения дневную дозу разделить на 2-3 приема;
- если требуется прием более 7.5 мг преднизолона в день, предпринять попытку прерывистой терапии (например, 15 мг преднизолона через день вместо ежедневного приема 7.5 мг);
- для снижения суточной пероральной дозы преднизолона можно заменить часть принимаемого внутрь препарата ингаляцией бекотида, исходя из того, что 6 мг преднизолона равны по активности 400 мг бекотида.
В. И. Трофимов (1996) рекомендует начинать терапию таблетированными глюкокортиковдами с суточной дозы 20-40 мг преднизолона или 16-32 мг метипреда, триамцинолона 2/3 — 3/4 суточной дозы больной должен принимать утром после завтрака, остальную часть — после обеда (до 15.00) в соответствии с циркадными ритмами продукции глюкокортикоидов и чувствительности к ним тканей и клеток организма. После значительного улучшения состояния больного (отсутствие приступов удушья в течение 7-10 дней) можно снижать дозу глюкокортикоидов на 1/2 таблетки в 3 дня, а при достижении дозы 10 мгДуг преднизолона или эквивалентной дозы другого препарата — на 1/4 таблетки за 3 дня до полной отмены или сохранения поддерживающей дозы (обычно 1,1/2 таблетки). Если больной получал глюкокортикоиды длительно (более 6 месяцев), снижение дозы нужно производить более медленно: на 1/2 — 1/4 таблетки за 7-14 и более дней.
Рекомендуется сочетать прием глюкокортикоидов внутрь с использованием их ингаляционных форм, что позволяет значительно уменьшить лечебную и поддерживающую дозы пероральных препаратов.
При необходимости длительного применения глюкокортикоидов для контроля за астмой тяжелого течения целесообразно использование альтернирующей схемы приема (удвоенной суточной дозы через день 1 раз в сутки утром), что позволяет уменьшить риск угнетения надпочечников и развития системных побочных эффектов. Короткий период полураспада пероральных глюкокортикоидов группы преднизолона и триамцинолона позволяет применять альтернирующую схему. Следует подчеркнуть что альтернирующая схема приема глюкокортикоидов обычно приемлема тогда, когда с помощью ежедневного их приема уже удалось добиться улучшения течения астмы и снизить суточную дозу преднизолона до 5-7.5 мг/день; однако, если наступило ухудшение состояния, необходимо вернуться к ежедневному приему препарата. При очень тяжелом течении астмы альтернирующая схема неэффективна, приходится применять глюкокортикоиды ежедневно и даже 2 раза в день.
Согласно совместному докладу Национального института сердца, легких и крови (США) и ВОЗ «Бронхиальная астма. Глобальная стратегия» — короткий курс лечения пероральными глюкокортикоидами (5-7 дней) может быть использован как «максимальная терапия» для достижения контроля течения астмы у больного. Этот курс может применяться или в начале лечения больного с неконтролируемой астмой или в течение периода, когда больной отмечает постепенное ухудшение своего состояния. Побочные эффекты при коротких курсах (менее 10 дней), как правило, не наблюдаются, отменять глюкокортикоиды можно сразу после коротких курсов.
При наличии противопоказаний к приему глюкокортикоидных препаратов внутрь (эрозивный гастрит, язвенная болезнь желудка и двенадцатиперстной кишки) можно применить кенолог-40 (препарат триамцинолона продленного действия) внутримышечно в дозе 1-2 мл (40-80 мг) 1 раз в 4 недели.
Количество инъекций на курс лечения и интервалы между инъекциями определяются индивидуально, однако, к сожалению, при продолжительном лечении длительность эффекта уменьшается и возникает необходимость более частых введений. Некоторые больные, страдающие кортикозависимым вариантом бронхиальной астмы, вместо систематического перорального приема глюкокортикоидов применяют внутримышечное введение кеналога 1 раз в 3-4 недели.
При выраженных обострениях, тяжелых приступах бронхиальной астмы, угрожающих развитием астматического состояния, нередко приходится применять большие дозы глюкокортикоидов внутривенно через короткие интервалы времени. Считается, что оптимальная концентрация глюкокортикоидов в плазме достигается при введении гидрокортизона гемисукцината в дозе 4-8 мг/кг или преднизолона в дозе 1-2 мг/кг с интервалами 4-6 ч. Более эффективно внутривенное капельное введение глюкокортикоидов, которое может производиться 1-4 раза в сутки в зависимости от состояния больного. Обычно курс лечения внутривенными капельными вливаниями глюкокортикоидов до достижения оптимального эффекта составляет 3-7 дней, после чего глюкокортикоиды отменяют, постепенно снижая дозу на 1/4 начальной суточной дозы, добавляя ингаляционные глюкокортикоиды.
При глюкокортикозависимой бронхиальной астме отменить полностью глюкокортикоиды невозможно, достаточно активной оказывается суточная доза преднизолона 5-10 мг.
Лечение глюкокортикоидами беременных женщин, страдающих бронхиальной астмой
Большинство пульмонологов считает противопоказанной системную пероральную глюкокортакоидную терапию в первом триместре беременности из-за высокого риска развития уродств у плода. Ингаляционные глюкокортикоиды могут применяться для лечения бронхиальной астмы (в дозе не более 1000 мкг в сутки) в течение всего периода беременности, т.к. их системные побочные эффекты незначительны, а риск гибели плода вследствие гипоксии при приступах астмы велик.
Небольшие дозы глюкокортикоидов при необходимости можно назначать внутрь во II-III триместрах в комбинации с ингаляционными глюкокортикоидами. При тяжелом приступе астмы и астматическом статусе показано внутривенное введение глюкокортикоидов.
Осложнения
Побочные эффекты системного лечения глюкокортикоидами:
- ожирение, преимущественно в области груди, живота, шейного отдела позвоночника, появление лунообразного гиперемированного лица;
- психозы, эмоциональная лабильность;
- истончение, сухость кожи, багрово-фиолетовые стрии;
- акне, гирсутизм;
- атрофия мышц;
- остеопороз, в т.ч. позвоночника (возможны переломы позвоночника);
- гиперсекреция и повышение кислотности желудочного сока, развитие язв желудка и двенадцатиперстной кишки;
- гипергликемия (стероидный сахарный диабет);
- артериальная гипертензия;
- задержка натрия, отеки;
- задняя субкапсулярная катаракта;
- активизация туберкулезного процесса;
- угнетение функции надпочечников.
Внезапная отмена глюкокортикоидов после длительного их применения, особенно в больших дозах, приводит к быстрому появлению синдрома отмены, который проявляется:
- ухудшением течения бронхиальной астмы, возобновлением приступов удушья, возможным развитием астматического статуса;
- значительным падением артериального давления;
- резкой слабостью;
- тошнотой, рвотой;
- артралгией, миалгией;
- болями в животе;
- головной болью.
Для уменьшения развития побочных явлений глюкокортиковдной терапии и для уменьшения кортикозависимости рекомендуется:
- стараться обходиться меньшими дозами препарата;
- сочетать лечение с ингаляциями интала;
- назначать короткодействующие препараты (преднизолон, урбазон, полькортолон) и не применять длительно действующие глюкокортикоиды (кеналог, дексазон и др.);
- назначать глюкокортикоид в первой половине дня, наибольшую часть суточной дозы давать утром, чтобы концентрация препарата в крови совпадала с наибольшим выбросом эндогенного кортизола;
- поддерживающую дозу препарата (1.5-2 таблетки) целесообразно давать прерывистым способом (т.е. удвоенную поддерживающую дозу принимать однократно утром, но через день). При таком приеме уменьшается возможность угнетения надпочечников и развития побочных явлений;
- для уменьшения кортикозависимости в момент снижения дозы преднизолона и перехода на поддерживающие дозы принимать этимиол по 0.1 г 3 раза в день (под контролем артериального давления), глициррам по 0.05 г 2-3 раза в день внутрь. Эти средства стимулируют надпочечники. Для уменьшения кортикозависимости можно применять также настойку диоскореи кавказской по 30 капель 3 раза в день;
- применять РДТ с сочетании с иглорефлексотерапией;
- для предупреждения или уменьшения побочных явлений пероральной глюкокортикоидной терапии целесообразно часть дозы заменить ингаляциями глюкокортикоидов;
- применять плазмаферез, гемосорбцию.
Одним из наиболее тяжелых осложнений системной глюкокортикоидной терапии является остеопороз. Для его профилактики и лечения применяются препараты, содержащие гормон С-клеток щитовидной железы кальцитонин — кальцитрин, миакалъцик. Кальцитрин назначается по 1 ЕД подкожно или внутримышечно ежедневно в течение месяца с перерывами каждый 7-й день (курс 25 инъекций) или по 3 ЕД через день (курс 15 инъекций). Миакальцик (кальцитонин лосося) вводится подкожно или внутримышечно по 50 ЕД (курс 4 недели). Можно применять также миакальцик в виде спрея интраназально по 50 ЕД через день в течение 2 месяцев с последующим двухмесячным перерывом. Лечение препаратами кальцитонина нужно проводить в сочетании с приемом кальция глюконата внутрь по 3-4 г/сут. Препараты кальцитонина способствуют поступлению кальция в костную ткань, уменьшают явления остеопороза, обладают противовоспалительным действием, уменьшают дегрануляцию тучных клеток и кортикозависимость.
 [9], [10], [11], [12], [13], [14]
[9], [10], [11], [12], [13], [14]
Источник