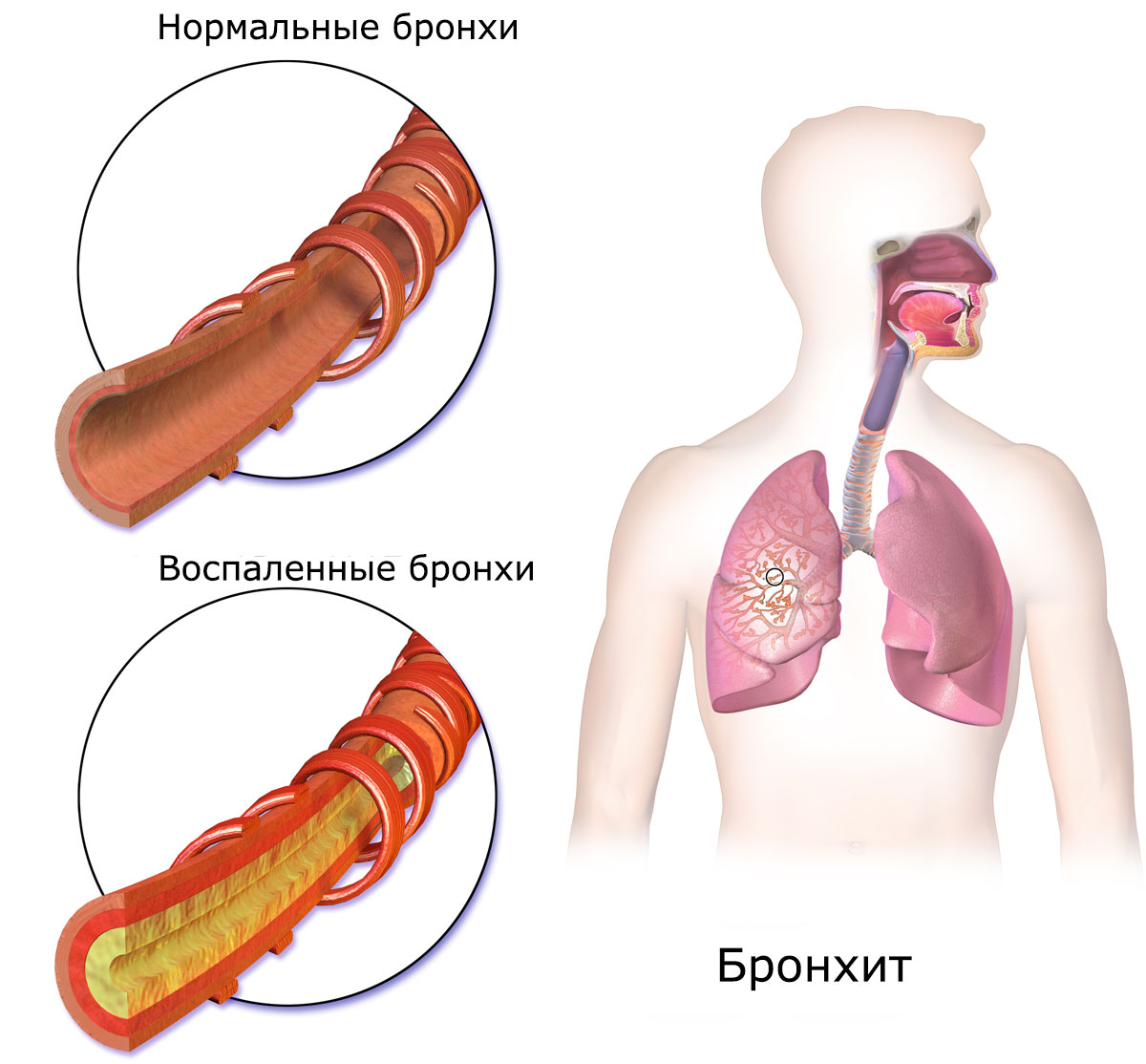
Иммунотерапия при бронхиальной астме

Предисловие
Бронхиальная астма — наиболее распространенное заболевание в структуре аллергических болезней.
По данным эпидемиологов, бронхиальная астма выявляется среди 8-10% взрослого населения и более 7% детей страдает этим заболеванием.
В последнее десятилетие отмечается тенденция роста показателей заболеваемости бронхиальной астмой.
В XX столетии зарегистрированы крупные «вспышки» бронхиальной астмы в ряде промышленных городов Европы, Азии, США, Англии и других стран.
Наличие указанной эпидемиологической ситуации требует разработки эффективных способов терапии и профилактики одной из наиболее тяжелых аллергопатологий.
В разные периоды развития астмологии предлагались различные определения болезни «бронхиальная астма». В 1995 г. в объединенном докладе ВОЗ и Национального института здоровья США дано следующее определение понятия бронхиальной астмы: «Астмой является хронический воспалительный процесс дыхательных путей, в котором задействованы многие клетки, особенно тучные, эозинофилы и Т-лимфоциты. У восприимчивых индивидов данное воспаление вызывает рецидивирующие приступы удушья, одышки, сдавливания в области грудной клетки и кашля, особенно в ночное время и ранним утром.
Данные симптомы обычно ассоциированы с распространяющимся затруднением дыхания, которое хотя бы частично снимается спонтанно или при лечении. Воспаление также является причиной ассоциированного повышения реактивности дыхательных путей на многие возбудители».
Этиология
Концепция болезни — основа для разработки стратегии ее лечения. Нозология бронхиальной астмы основана на специфической этиологии воздействующих на ткани бронхолегочного аппарата аэроаллергенов, патоморфологических изменениях, механизмах болезни (формирование аллергического воспаления) и клинических ее проявлениях.
Этиологические принципы, клинические признаки заболевания, степень выраженности и характер бронхиальной обструкции (легкая, средняя и тяжелая степень) положены в основу классификации этой болезни. В связи с этим всестороннее рассмотрение всех звеньев этиопатогенеза бронхиальной астмы и подходов к патогенетическим методам терапии является обязательным при выборе способов борьбы с этим тяжелым недугом.
Среди разнообразных методов лечения бронхиальной астмы можно выделить методы, направленные на устранение причины заболевания (этиологическое или элиминационное лечение) и на коррекцию патогенетических механизмов болезни (патогенетические методы терапии).
Аллерген-специфическая иммунотерапия
До настоящего времени единственным методом, так называемого, противоаллергического лечения, воздействующего на все патогенетически значимые звенья аллергического процесса и обладающего профилактическим эффектом после завершения лечебных курсов, является аллерген-специфическая иммунотерапия.
Этот метод (сокращенно СИТ) имеет преимущества перед фармакотерапевтическими методами, что позволяет получить длительную ремиссию заболевания, полное отсутствие симптомов болезни у пациента в период пыления растений, предотвращает переход более легких клинических проявлений бронхиальной астмы в тяжелые формы болезни, наконец, сохраняет трудоспособность пациента.
Ведущим звеном патогенеза бронхиальной астмы является повышенная чувствительность, гиперреактивность бронхов к аллергенам. Аллергическое воспаление, развивающееся в ответ на воздействие аэроаллергенов, чаще всего IgЕ-опосредованно. Воспалительная концепция ставит вопрос о необходимости проведения базисной противовоспалительной терапии. К этим методам относится и аллерген-специфическая иммунотерапия.
Метод СИТ, первоначально примененный при лечении пыльцевой аллергии, в настоящее время используется также для лечения болезней, обусловленных сенсибилизацией к инсектным, грибковым и другим аллергенам.
Комитетом Международного Союза иммунологических обществ и ВОЗ признана значимость метода СИТ в лечении аллергических заболеваний (69). Синонимами термина аллерген-специфическая иммунотерапия являются специфическая гипосенсибилизация, аллерговакцинация и др., обозначающие названия вариантов СИТ, с помощью которых достигается снижение чувствительности организма больного к причинно-значимому аллергену (или нескольким аллергенам) путем многократного введения в организм малых доз этого аллергена (или аллергенов). Анализ механизмов СИТ, рассмотрение критериев оценки эффективности метода является неотъемлемым условием ознакомления врача с методом гипосенсибилизирующей терапии.
К настоящему времени в аллергологической практике всего мира накоплен значительный опыт применения СИТ больным с бронхиальной астмой.
Существуют различные варианты осуществления гипосенсибилизирующей терапии, проведения аллерген-специфического лечения в сочетании (в комплексе) с другими методами терапии, в частности, в сочетании с базисной противовоспалительной терапией.
В предлагаемой вниманию читателей книге представлены в том числе результаты использования оздоровительного действия горного климата Приэльбрусья в лечении больных с бронхиальной астмой и его влияния на эффективность СИТ. Специальное внимание уделено вопросам бактериальной аллергии и опыту проведения СИТ бактериальными аллергенами у больных с инфекционно-аллергической (инфекционно-зависимой) бронхиальной астмой.
Отмечено, что наряду с высокой эффективностью метода (при правильном выборе больных для специфической терапии, отборе причинно-значимых аллергенов и др.) могут выявляться некоторые недостатки СИТ (риск провокации реакций анафилактического типа у больного, длительность курсов терапии и др.). Это требует усовершенствования метода через селекцию альтернативного контроля СИТ, а также путем разработки новых форм лечебных аллергенов на основе молекулярной модуляции IgЕ-связывающих эпитопов, введения в аллергологическую практику адьювантных форм аллергенов и др.
В связи с тем, что эффективность СИТ во многом определяется качеством лечебных форм аллергенов, в монографии рассмотрены вопросы взаимосвязи их структуры и функции, качества существующих коммерческих лечебных форм этих аллергенов (аллергоидов, депонированных форм, химически модифицированных вариантов), схем введения препаратов. Значительное внимание уделено анализу отдаленных результатов проведения СИТ. Обсуждается опыт 30-летних наблюдений авторов по изучению клинической эффективности аллерген-специфической иммунотерапии, проведенной больным с бронхиальной астмой.
Отдельный раздел посвящен вопросам инсектной аллергии и опыту применения СИТ при гиперчувствительности к внутрижилищным инсектным аллергенам и яду перепончатокрылых. Обсуждается возможность использования приемов СИТ в профилактике инсектной аллергии.
С целью широкого ознакомления читателя с методом СИТ представлены различные схемы проведения специфического лечения, которые были использованы разными исследователями, рассмотрены также преимущества и недостатки этих рекомендаций, даны характеристики коммерческих лечебных аллергенов, используемых при СИТ.
На Международной конференции «Достижения в лечении аллергических заболеваний дыхательного тракта» (1998, Paris) была изложена суть документа, подготовленного ВОЗ об отношении к аллерген-специфической иммунотерапии (СИТ), в котором иллюстрированы основные положения, касающиеся назначения этого вида лечения.
На основе анализа данных многочисленных исследований, положенных в основу оценки эффективности СИТ, было показано, что:
- СИТ является единственным методом лечения, который способен влиять на все патогенетические звенья аллергического процесса;
- СИТ при IgE-опосредованных формах аллергии является высокоэффективным методом лечения, проводимым в тех случаях, когда невозможно исключение контакта с «виновным» аллергеном;
- своевременно проведенная СИТ, осуществляемая на ранних стадиях формирования респираторной аллергии, предупреждает развитие бронхиальной астмы;
- СИТ особенно эффективна у пациентов с легкой формой бронхиальной астмы при наличии у них повышенной чувствительности к ограниченному числу аллергенов.
Указанные положения позволяют сделать вывод о том, что при наличии у больного бронхиальной астмой гиперчувствительности немедленного типа (IgЕ-опосредованной) к 2 — 3 причинно-значимым аллергенам (и при отсутствии противопоказаний) возможно проведение СИТ. В связи с этим необходимо рассмотреть основные механизмы аллергических реакций немедленного типа, которые играют важную роль в патогенезе бронхиальной астмы и которые задействованы в формировании противоаллергической защиты при проведении СИТ.
Хутуева С.X., Федосеева В.Н.
Опубликовал Константин Моканов
Источник
Специфическое лечение бронхиальной астмы может проводиться в нескольких направлениях: методы элиминации — устранение контакта с причинно-значимыми аллергенами; специфическая гипосенсибилизация или иммунотерапия, в основе которой лежит выработка у больного толерантности к специфическому аллергену.
Наиболее простым и радикальным методом лечения атопической астмы является полное прекращение контакта больного с аллергеном, ответственным за заболевание, т. е. элиминационная терапия.
Однако это не всегда возможно и зависит в основном от рода аллергена.
Элиминационная терапия возможна при пищевой и лекарственной аллергии (если речь идет о моносенсибилизации); при бытовой и эпидермальной аллергии постоянная влажная уборка квартиры, замена постельных принадлежностей, содержащих перо и пух, приводит к элиминации бытовых и пищевых аллергенов. При пыльцевой аллергии прекращение контакта с «виновным» аллергеном путем выезда в другую климато-географическую зону, где не растет аллергенная растительность.
При невозможности избежать контакта с «виновным» аллергеном показана специфическая иммунотерапия, в основе которой лежит выработка у больного толерантности к специфическому аллергену, которая достигается введением в организм возрастающих доз специфического аллергена.
При специфической иммунотерапии наиболее часто используется «классический» метод, предложенный Noon в 1911 г. При этом методе этиологический аллерген вводится подкожно в постоянно возрастающих концентрациях. Существует несколько схем лечения подкожными инъекциями — замедленная (классическая) и ускоренная схемы.
Эффективность лечения атопических заболеваний дыхательных путей составляет 60 — 80% (Ю. А. Порошина и соавторы, 1964, 1986; Л. А. Горячкина и соавторы, 1981).
Специфическая иммунотерапия больных атопической бытовой астмой с подключением аллергена клеща D.pteronyssinus позволила получить отличный и хороший эффекты в 79% случаев.
О. В. Полсачева и соавторы (1986) изучили результаты трех методов специфической иммунотерапии пыльцевой аллергии у больных, сенсибилизированных к пыльце злаковых трав водно-солевыми экстрактами по ускоренной схеме (водно-солевые экстракты, депонированные ex tempore в 0,1% геле гидрата окиси алюминия) — экспериментальными сериями очищенного пролонгированного препарата цинтала. Больным контрольной группы вводили плацебо. Лучший клинический эффект получен при проведении лечения цинтаналом, в сравнении в нативным ВСЭ.
Возникающие осложнения побуждают постоянно вести поиск новых методов специфической иммунотерапии. Среди них следует остановиться на пероральном методе СИТ. Несмотря на простоту методики проведения лечения, он не получил широкого распространения ввиду недостаточного терапевтического эффекта. У детей, однако, проводят лечение поллиноза и бронхиальной астмы пероральным методом.
Оральная специфическая иммунотерапия пыльцевыми аллергенами была несколько менее эффективной в исследованиях. J. Oppenheimer et al (1994) указывает на возможность получения (121) 67,4% отличных и хороших результатов при оральном методе СИТ, в сравнении с результатами классического инъекционного специфического лечения (76,9%).
Разработанный в Институте иммунологии новый ускоренный пероральный метод специфической иммунотерапии аллергенами «глицал» позволил получить больший процент отличных и хороших результатов, по сравнению с ускоренным парентеральным методом водно-солевыми экстрактами.
При проведении специфической иммунотерапии также используется интраназальный или ингаляционный метод введения бытовых и пыльцевых аллергенов, результаты которого оказались более эффективными, в сравнении с подкожным методом лечения. Преимуществом данного метода является нетравматичность, меньшее число осложнений и возможность проведения лечения на дому с помощью ингалятора.
Локальная интраназальная специфическая иммунотерапия аллергеном амброзии позволила улучшить состояние больных в 71,5% случаев, а в группе получавших плацебо значительно меньше (Nickelsen et al, 1981).
Специфическая иммунотерапия бытовыми аллергенами (домашней пыли, клещей, эпидермальными аллергенами)
Специфическая иммунотерапия больных атопической бронхиальной астмой проводилась в Республиканском аллергологическом центре. Больные, прошедшие специфическую иммунотерапию, были в возрасте от 10 до 60 лет. Средний возраст — 27,5 лет. Продолжительность наблюдения составила 5 -30 лет.
При обращении превалировали пациенты со средней степенью тяжести бронхиальной астмы (69%). В период с 1971 по 1985 гг. больные получили от 1 до 10 курсов специфической иммунотерапии (всего 726 курсов).
Специфическая иммунотерапия проводилась по классической замедленной схеме водно-солевыми экстрактами бытовых, эпидермальных и пыльцевых аллергенов. Инъекции делали 1 — 2 раза в неделю с постепенным повышением концентрации аллергена. Больные получали в среднем 30 — 40 инъекций. Продолжительность курса доставляла 5-8 месяцев, с переводом их в последующем на поддерживающую дозу 1:10-0,5 один раз в неделю от 2 — 6 инъекций.
Перерывы между курсами составляли не более 3-4 месяцев. За курс лечения больной получал в среднем от 5967 до 8967 PNU. Специфическая иммунотерапия начиналась осенью, когда отцветала амброзия, и завершалась в июне. После получения хорошего терапевтического эффекта больным рекомендовалось продолжение специфической иммунотерапии для закрепления результата лечения.
Эффективность специфической иммунотерапии оценивалась по клиническим и иммунологическим показателям.
Клинические показатели оценивались следующим образом: отличный эффект, хороший, удовлетворительный, неудовлетворительный (А. Д. Адо, Н. В. Адрианова, 1976) (табл. 28):
а) отличный эффект — после лечения исчезли все проявления заболевания (приступы удушья, кашель, ринорея). Бронхолитическими и антигистаминными препаратами больной не пользовался;
б) хороший — проявления болезни стали очень редкими и легкими, т. е. выраженных приступов удушья не стало, иногда беспокоили легкие затруднения дыхания, кашель, небольшой насморк. Все симптомы легко купировались малыми дозами бронхолитиков в ингаляциях;
в) удовлетворительный — приступы удушья стали протекать легче и реже. Число необходимых лекарств значительно уменьшилось;
г) неудовлетворительный — эффекта от лечения не наступило.
Результаты специфического лечения оценивались сразу же после окончания курса лечения, а за пациентами, прошедшими специфическую иммунотерапию, наблюдения продолжались в течение длительного времени (до 30 лет). В последующем больные осматривались один раз в году — осенью, в период наиболее вероятного обострения заболевания. При нестойком терапевтическом эффекте проводились повторные курсы иммунотерапии до получения стойкой клинической ремиссии, при стойкой клинической ремиссии через каждые 3-5 лет проводились профилактические, т. е. противорецидивные курсы иммунотерапии, что обозначено нами как вторичная иммунопрофилактика астмы. Если курсы иммунотерапии не повторялись, возможными становились рецидивы астмы.
При проведении специфической иммунотерапии больные выдерживали элиминационные мероприятия, по мере необходимости принимали медикаментозное лечение (бронхолитики, антигистаминные препараты, интал, за исключением кортикостероидов).
Таблица 28. Результаты специфической иммунотерапии больных бронхиальной астмой бытовыми и эпидермальными аллергенами

Специфическое лечение проводили стандартными бытовыми и эпидермальными аллергенами. Получено 67,5 ± 3,7% отличных и хороших результатов, у 20,0 ± 3,16% — эффект удовлетворительный, у 8,1 ± 2,14% — эффекта от лечения не было, а у 4,4 ± 0,38% — приступы удушья возобновились вновь после длительной клинической ремиссии.
Результаты иммунотерапии не всегда были устойчивы. Из 108 больных с отличным и хорошим эффектом в период клинической ремиссии у некоторых отмечали насморк, кашель, одышку при контакте с неспецифическими раздражителями (запахом краски, при переохлаждении, респираторном заболевании). Все это расценивалось нами как нестойкий терапевтический эффект.
Последующий анализ показал, что подобные обострения чаще возникали у больных, которые нарушали последовательность и ритмичность лечения, т. е. пройдя один курс специфического лечения, почувствовав облегчение или исчезновение приступов удушья, они самовольно прекращали лечение. Через несколько лет, когда состояние их ухудшалось, они вновь являлись к аллергологу, получали следующий курс иммунотерапии и прекращали его до очередного ухудшения состояния.
70 больных имели стойкий терапевтический эффект, в связи с чем в дальнейшем специфическое лечение им было прекращено, а наблюдение за ними продолжалось. Большинство из них лечилось регулярно, подряд 2-3 курса и более с небольшими перерывами между курсами.
Выписка из истории болезни №567
Больной С. М., 20 лет, обратился к аллергологу. Страдает бронхиальной астмой. Первый приступ удушья связывает с фактором переохлаждения. В последующем приступы удушья приняли характер атопической астмы, дома, в селе, приступы удушья были каждую ночь, вне дома, в стационаре был здоров. Больному провели два курса специфического лечения бытовыми аллергенами.
Состояние несколько улучшилось, но приступы удушья еще беспокоили, в связи с чем больному начали третий курс специфической иммунотерапии в условиях стационара, затем продолжили его в условиях высокогорья. После проведения еще трех курсов бытовыми аллергенами был получен отличный терапевтический эффект, стойкая клиническая ремиссия. Больной служил в рядах Советской Армии, и приступы удушья не возобновились. Отдаленные результаты лечения с отличным эффектом — 20 лет.
Из данных аллергологического анамнеза: у матери и у дяди по линии матери бронхиальная астма.
У двух сестер тоже появились приступы удушья. Обе сестры обследованы, диагноз атопической астмы подтвержден, проведено специфическое лечение. Одна из сестер провела подряд два курса специфической иммунотерапии с отличным эффектом. Отдаленные результаты с отличным эффектом — 6 лет. Другая сестра по семейным обстоятельствам сумела провести только один курс специфической иммунотерапии, чувствовала себя хорошо в течение двух лет, однако спустя год у больной — рецидив астмы, развился приступ удушья.
Таким образом, при регулярном проведении специфической иммунотерапии не менее двух курсов получена стойкая клиническая ремиссия, в то время как у одной из сестер получена нестойкая клиническая ремиссия с последующим рецидивом астмы, что явилось основанием для продолжения специфической иммунотерапии.
Возобновление приступов удушья у больной после длительной клинической ремиссии навело нас на мысль о необходимости проведения профилактических, т. е. противорецидивных курсов иммунотерапии с целью продлить клиническую ремиссию.
Поскольку результаты специфической иммунотерапии были относительно невысокими (67,5 ± 3,74% отличных и хороших результатов), специфическая иммунотерапия продолжена у части из них с целью улучшить терапевтический эффект или закрепить уже полученный хороший терапевтический эффект.
С целью улучшения терапевтического эффекта продолжено специфическое лечение краевыми аллергенами — клещом, амброзией и аллергеном домашней пыли, а при отсутствии эффекта специфическое лечение проводилось в условиях горного климата Приэльбрусья. При сочетании с пищевой аллергией назначали элиминационные диеты.
При проведении специфической иммунотерапии больным с сочетанной полиаллергией выдерживалась определенная последовательность: сначала лечение проводилось бытовыми и эпидермальными аллергенами, а затем — пыльцевыми (табл. 29).
Учитывая наличие выраженной сенсибилизации к клещу у 210 (51,4 ± 2,46%) больных, при проведении специфической иммунотерапии к смеси домашней пыли и пера подушки подключали 0,1 мл аллергена клеща Dermatophagoides pteronyssinus с содержанием 10000 PNU в 1 мл и продолжали специфическую иммунотерапию по обычной методике и схеме.
Для проведения специфической иммунотерапии были взяты больные, у которых клинически явно превалировал выраженный клещевой компонент — приступы удушья дома, ночью, четкий фактор элиминации, к тому же эффект специфической иммунотерапии, полученный от предыдущих курсов, был недостаточным. В эту группу включены больные в возрасте от 15 до 64 лет.
При проведении специфической иммунотерапии бытовыми и эпидермальными аллергенами с подключением аллергена клеща получено отличных и хороших результатов 80,0 ± 6,7%.
Проведение специфического лечения бытовыми, эпидермальными аллергенами с подключением аллергена клеща оказалось значительно эффективнее, что свидетельствует об этиологической значимости его.
Специфическая иммунотерапия аллергенами домашней пыли
Учитывая данные литературы о том, что краевые и индивидуальные аллергены являются более специфичными, были приготовлены краевые и индивидуальные аллергены в Институте иммунологии МЗ РФ.
Специфическая иммунотерапия краевым аллергеном домашней пыли проведена 73 больным, ранее у которых при использовании стандартных аллергенов не удалось достигнуть желаемого эффекта (табл. 30).
Таблица 29. Сравнительная характеристика результатов специфической иммунотерапии бытовыми аллергенами с подключением аллергена клеща Dermatophagoides pteronyssinus и без него

Таблица 30. Результаты специфической иммунотерапии краевыми аллергенами домашней пыли

В результате проведенного лечения краевыми аллергенами удалось улучшить терапевтический эффект с 57,4 ± 5,83% хороших до 78,0 ± 4,8% отличных и хороших результатов (Р < 0,01). Таким образом, краевые аллергены оказались более эффективными, чем стандартные.
Хутуева С.X., Федосеева В.Н.
Опубликовал Константин Моканов
Источник