Обмен лактата в печени и мышцах цикл кори
Метаболическая регуляция мышечного сокращения
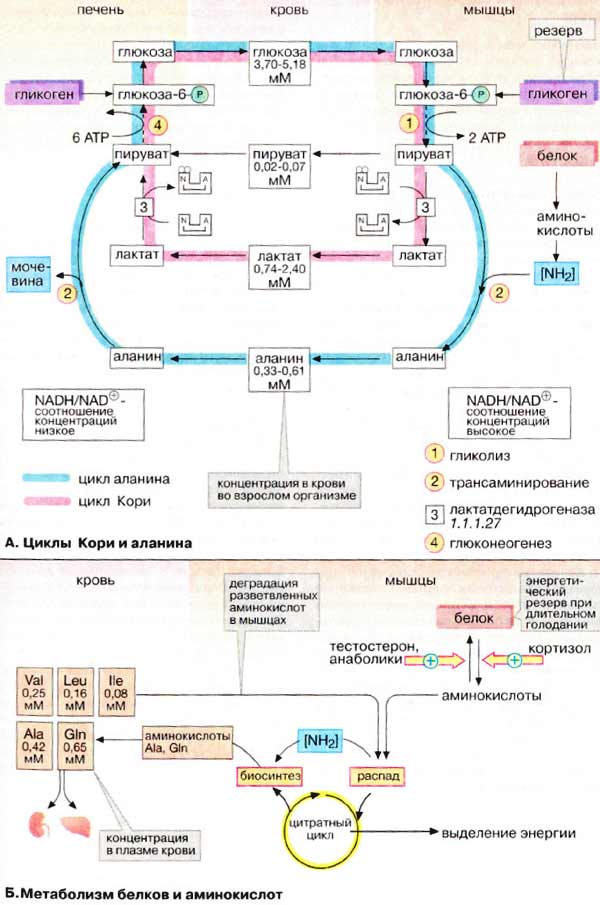
А. Циклы Кори и
аланина
В клетках, не содержащих митохондрий
(например, в эритроцитах), или в тканях при недостаточном снабжении кислородом
(например, в активно работающих мышцах) АТФ (АТР) синтезируется за счет процесса
превращений глюкозы в лактат, т. е. за счет процесса брожения (= анаэробного
гликолиза, см. рис. 153). Лактат переносится кровью в печень, где в
процессе глюконеогенеза с затратой АТФ (см. рис. 157) вновь конвертируется
в глюкозу (цикл Кори).
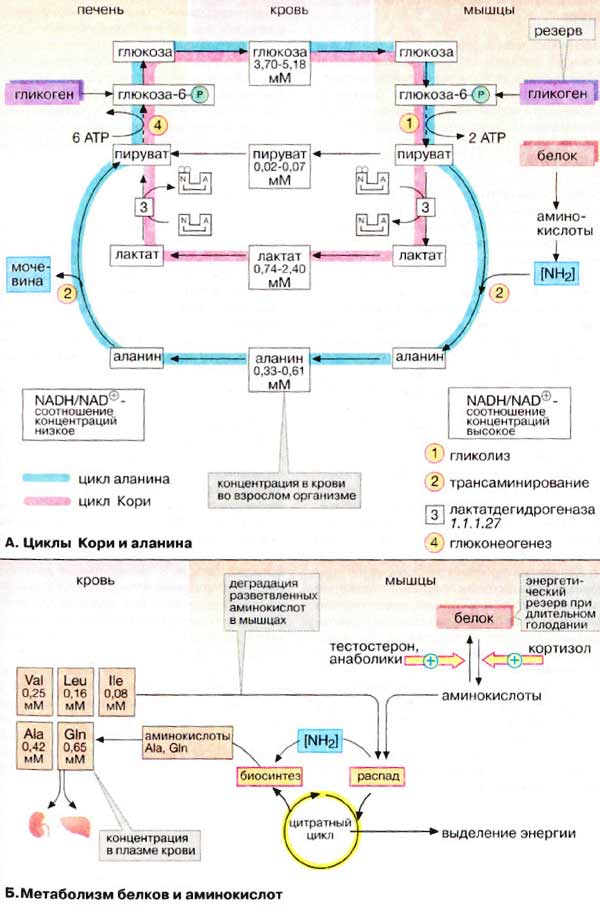
При интенсивной работе мышцы максимально
активируется гликолиз. Продукт гликолиза, пировиноградная кислота (пируват)
накапливается в цитоплазме и недостаточно быстро поступает в митохондрии, если
они из-за недостатка кислорода не готовы к окислению пирувата. В анаэробных
условиях пируват в реакции, катализируемой лактатдегидрогеназой (см. рис.
103) (заключительный этап гликолиза) восстанавливается до лактата.
Одновременно
НАДН (NADH), кофермент лактатдегидрогеназы, окисляется до НАД+
(NAD+), который вновь используется на окислительном этапе
гликолитического пути. Этой реакции способствует относительно высокое отношение
НАДН/НАД+ в мышечной ткани. Лактат диффундирует в кровь и поступает в
печень, где конвертируется в глюкозу. Таким образом, образование лактата
временно заменяет аэробный метаболизм глюкозы и частично переносит этот процесс
из мышц в печень.
Обратная связь, подобная циклу Кори,
существует в цикле аланина, в котором также участвует пируват.
Цикл аланина берет начало с протеолиза белков. Образующиеся аминокислоты
в результате трансаминирования в присутствии ферментов превращаются в
α-кетокислоты (на схеме не приведено, см. рис. 181), которые в основном включаются
в цикл трикарбоновых кислот (цитратный цикл) (см. рис. 183).Одновременно в
реакции, катализируемой аланинтрансаминазой, аминогруппы из разных аминокислот
переносятся на имеющийся субстрат, пируват. Образующийся аланин поступает
в кровь и переносится в печень. Таким образом, цикл аланина служит каналом
передачи азота и предшественников глюкозы в печень, которая является местом
синтеза конечных продуктов азотистого обмена, например мочевины (см. рис.
185).
Следует напомнить, что при анаэробном
гликолизе образуются кислоты, которые, не принимая участие в последующем обмене,
существуют в форме анионов. Поэтому при интенсивном анаэробном гликолизе рН
мышечной клетки может понизиться настолько, что сокращение станет невозможным.
Обычно этого не происходит благодаря быстрому выходу кислых метаболитов (лактата
и пирувата) в кровь, которая также может оказаться закисленной
(метаболический ацидоз).
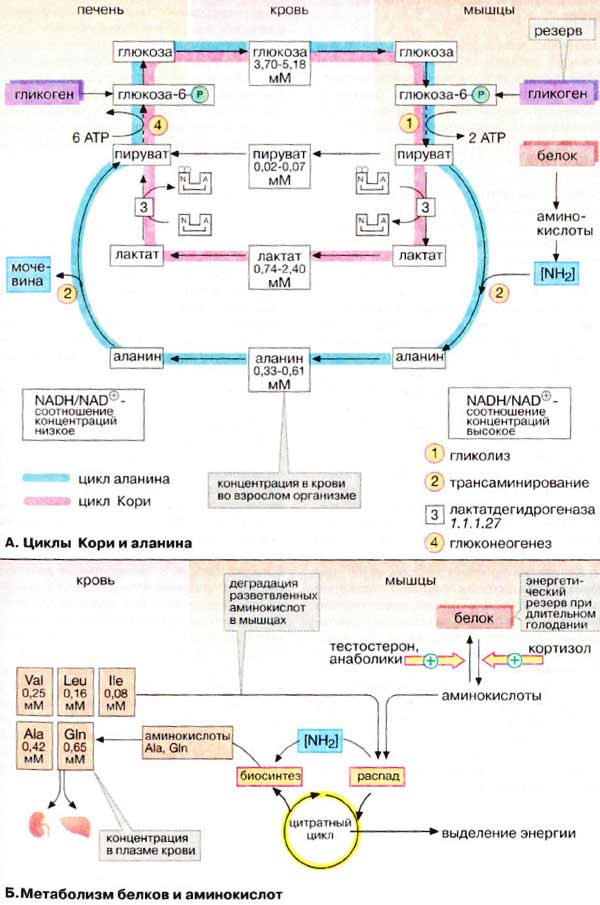
Б. Метаболизм белков и
аминокислот
Скелетные мышцы активно участвуют в
метаболизме аминокислот. Это наиболее важный участок деградации разветвленных
аминокислот (Val и Ile, см. с. 402). Ряд других аминокислот также
деградируются преимущественно в мышцах. Одновременно идет ресинтез и
высвобождение в кровь аланина и глутамина. Эти аминокислоты служат
переносчиками азота, образующегося при расщеплении белков, в печень (цикл
аланина) и почки (см. рис. 319).
При голодании мышечные белки
служат энергетическим резервом организма. Они гидролизуются до аминокислот,
которые поступают в печень. Здесь углеродный скелет аминокислот конвертируется в
промежуточные продукты цитратного цикла, в том числе в ацетоацетил-КоА и
ацетил-КоА (см. рис. 183). Эти амфиболические соединения окисляются в цикле
трикарбоновых кислот или включаются в процесс
глюконеогенеза.
Синтез и расщепление мышечных белков
контролируются гормонами. Тестостерон и синтетические анаболики
стимулируют биосинтез белка; напротив, кортизол подавляет образование
мышечных белков.
Белки актин и миозин содержат остатки
гистидина, метилированного на стадии посттрансляционной модификации. При
расщеплении этих белков образуется 3-метилгистидин, который дальше не
разрушается. Количество метилгистидина в моче служит мерой деградации мышечных
белков.

Источник
330-331
Òêàíè è îðãàíû. Ìûøöû
Ìåòàáîëè÷åñêàÿ ðåãóëÿöèÿ ìûøå÷íîãî ñîêðàùåíèÿ
 À. Öèêëû Êîðè è
À. Öèêëû Êîðè è
àëàíèíà
 êëåòêàõ, íå ñîäåðæàùèõ ìèòîõîíäðèé
(íàïðèìåð, â ýðèòðîöèòàõ), èëè â òêàíÿõ ïðè íåäîñòàòî÷íîì ñíàáæåíèè êèñëîðîäîì
(íàïðèìåð, â àêòèâíî ðàáîòàþùèõ ìûøöàõ) ÀÒÔ (ÀÒÐ) ñèíòåçèðóåòñÿ çà ñ÷åò ïðîöåññà
ïðåâðàùåíèé ãëþêîçû â ëàêòàò, ò. å. çà ñ÷åò ïðîöåññà áðîæåíèÿ (= àíàýðîáíîãî
ãëèêîëèçà, ñì. ðèñ. 153). Ëàêòàò ïåðåíîñèòñÿ êðîâüþ â ïå÷åíü, ãäå â
ïðîöåññå ãëþêîíåîãåíåçà ñ çàòðàòîé ÀÒÔ (ñì. ðèñ. 157) âíîâü êîíâåðòèðóåòñÿ
â ãëþêîçó (öèêë Êîðè).
Ïðè èíòåíñèâíîé ðàáîòå ìûøöû ìàêñèìàëüíî
àêòèâèðóåòñÿ ãëèêîëèç. Ïðîäóêò ãëèêîëèçà, ïèðîâèíîãðàäíàÿ êèñëîòà (ïèðóâàò)
íàêàïëèâàåòñÿ â öèòîïëàçìå è íåäîñòàòî÷íî áûñòðî ïîñòóïàåò â ìèòîõîíäðèè, åñëè
îíè èç-çà íåäîñòàòêà êèñëîðîäà íå ãîòîâû ê îêèñëåíèþ ïèðóâàòà. Â àíàýðîáíûõ
óñëîâèÿõ ïèðóâàò â ðåàêöèè, êàòàëèçèðóåìîé ëàêòàòäåãèäðîãåíàçîé (ñì. ðèñ.
103) (çàêëþ÷èòåëüíûé ýòàï ãëèêîëèçà) âîññòàíàâëèâàåòñÿ äî ëàêòàòà.
Îäíîâðåìåííî
ÍÀÄÍ (NADH), êîôåðìåíò ëàêòàòäåãèäðîãåíàçû, îêèñëÿåòñÿ äî ÍÀÄ+
(NAD+), êîòîðûé âíîâü èñïîëüçóåòñÿ íà îêèñëèòåëüíîì ýòàïå
ãëèêîëèòè÷åñêîãî ïóòè. Ýòîé ðåàêöèè ñïîñîáñòâóåò îòíîñèòåëüíî âûñîêîå îòíîøåíèå
ÍÀÄÍ/ÍÀÄ+ â ìûøå÷íîé òêàíè. Ëàêòàò äèôôóíäèðóåò â êðîâü è ïîñòóïàåò â
ïå÷åíü, ãäå êîíâåðòèðóåòñÿ â ãëþêîçó. Òàêèì îáðàçîì, îáðàçîâàíèå ëàêòàòà
âðåìåííî çàìåíÿåò àýðîáíûé ìåòàáîëèçì ãëþêîçû è ÷àñòè÷íî ïåðåíîñèò ýòîò ïðîöåññ
èç ìûøö â ïå÷åíü.
Îáðàòíàÿ ñâÿçü, ïîäîáíàÿ öèêëó Êîðè,
ñóùåñòâóåò â öèêëå àëàíèíà, â êîòîðîì òàêæå ó÷àñòâóåò ïèðóâàò.
Öèêë àëàíèíà áåðåò íà÷àëî ñ ïðîòåîëèçà áåëêîâ. Îáðàçóþùèåñÿ àìèíîêèñëîòû
â ðåçóëüòàòå òðàíñàìèíèðîâàíèÿ â ïðèñóòñòâèè ôåðìåíòîâ ïðåâðàùàþòñÿ â
α-êåòîêèñëîòû (íà ñõåìå íå ïðèâåäåíî, ñì. ðèñ. 181), êîòîðûå â îñíîâíîì âêëþ÷àþòñÿ
â öèêë òðèêàðáîíîâûõ êèñëîò (öèòðàòíûé öèêë) (ñì. ðèñ. 183).Îäíîâðåìåííî â
ðåàêöèè, êàòàëèçèðóåìîé àëàíèíòðàíñàìèíàçîé, àìèíîãðóïïû èç ðàçíûõ àìèíîêèñëîò
ïåðåíîñÿòñÿ íà èìåþùèéñÿ ñóáñòðàò, ïèðóâàò. Îáðàçóþùèéñÿ àëàíèí ïîñòóïàåò
â êðîâü è ïåðåíîñèòñÿ â ïå÷åíü. Òàêèì îáðàçîì, öèêë àëàíèíà ñëóæèò êàíàëîì
ïåðåäà÷è àçîòà è ïðåäøåñòâåííèêîâ ãëþêîçû â ïå÷åíü, êîòîðàÿ ÿâëÿåòñÿ ìåñòîì
ñèíòåçà êîíå÷íûõ ïðîäóêòîâ àçîòèñòîãî îáìåíà, íàïðèìåð ìî÷åâèíû (ñì. ðèñ.
185).
Ñëåäóåò íàïîìíèòü, ÷òî ïðè àíàýðîáíîì
ãëèêîëèçå îáðàçóþòñÿ êèñëîòû, êîòîðûå, íå ïðèíèìàÿ ó÷àñòèå â ïîñëåäóþùåì îáìåíå,
ñóùåñòâóþò â ôîðìå àíèîíîâ. Ïîýòîìó ïðè èíòåíñèâíîì àíàýðîáíîì ãëèêîëèçå ðÍ
ìûøå÷íîé êëåòêè ìîæåò ïîíèçèòüñÿ íàñòîëüêî, ÷òî ñîêðàùåíèå ñòàíåò íåâîçìîæíûì.
Îáû÷íî ýòîãî íå ïðîèñõîäèò áëàãîäàðÿ áûñòðîìó âûõîäó êèñëûõ ìåòàáîëèòîâ (ëàêòàòà
è ïèðóâàòà) â êðîâü, êîòîðàÿ òàêæå ìîæåò îêàçàòüñÿ çàêèñëåííîé
(ìåòàáîëè÷åñêèé àöèäîç).
Á. Ìåòàáîëèçì áåëêîâ è
àìèíîêèñëîò
Ñêåëåòíûå ìûøöû àêòèâíî ó÷àñòâóþò â
ìåòàáîëèçìå àìèíîêèñëîò. Ýòî íàèáîëåå âàæíûé ó÷àñòîê äåãðàäàöèè ðàçâåòâëåííûõ
àìèíîêèñëîò (Val è Ile, ñì. ñ. 402). Ðÿä äðóãèõ àìèíîêèñëîò òàêæå
äåãðàäèðóþòñÿ ïðåèìóùåñòâåííî â ìûøöàõ. Îäíîâðåìåííî èäåò ðåñèíòåç è
âûñâîáîæäåíèå â êðîâü àëàíèíà è ãëóòàìèíà. Ýòè àìèíîêèñëîòû ñëóæàò
ïåðåíîñ÷èêàìè àçîòà, îáðàçóþùåãîñÿ ïðè ðàñùåïëåíèè áåëêîâ, â ïå÷åíü (öèêë
àëàíèíà) è ïî÷êè (ñì. ðèñ. 319).
Ïðè ãîëîäàíèè ìûøå÷íûå áåëêè
ñëóæàò ýíåðãåòè÷åñêèì ðåçåðâîì îðãàíèçìà. Îíè ãèäðîëèçóþòñÿ äî àìèíîêèñëîò,
êîòîðûå ïîñòóïàþò â ïå÷åíü. Çäåñü óãëåðîäíûé ñêåëåò àìèíîêèñëîò êîíâåðòèðóåòñÿ â
ïðîìåæóòî÷íûå ïðîäóêòû öèòðàòíîãî öèêëà, â òîì ÷èñëå â àöåòîàöåòèë-ÊîÀ è
àöåòèë-ÊîÀ (ñì. ðèñ. 183). Ýòè àìôèáîëè÷åñêèå ñîåäèíåíèÿ îêèñëÿþòñÿ â öèêëå
òðèêàðáîíîâûõ êèñëîò èëè âêëþ÷àþòñÿ â ïðîöåññ
ãëþêîíåîãåíåçà.
Ñèíòåç è ðàñùåïëåíèå ìûøå÷íûõ áåëêîâ
êîíòðîëèðóþòñÿ ãîðìîíàìè. Òåñòîñòåðîí è ñèíòåòè÷åñêèå àíàáîëèêè
ñòèìóëèðóþò áèîñèíòåç áåëêà; íàïðîòèâ, êîðòèçîë ïîäàâëÿåò îáðàçîâàíèå
ìûøå÷íûõ áåëêîâ.
Áåëêè àêòèí è ìèîçèí ñîäåðæàò îñòàòêè
ãèñòèäèíà, ìåòèëèðîâàííîãî íà ñòàäèè ïîñòòðàíñëÿöèîííîé ìîäèôèêàöèè. Ïðè
ðàñùåïëåíèè ýòèõ áåëêîâ îáðàçóåòñÿ 3-ìåòèëãèñòèäèí, êîòîðûé äàëüøå íå
ðàçðóøàåòñÿ. Êîëè÷åñòâî ìåòèëãèñòèäèíà â ìî÷å ñëóæèò ìåðîé äåãðàäàöèè ìûøå÷íûõ
áåëêîâ.
Источник
330-331
Òêàíè è îðãàíû. Ìûøöû
Ìåòàáîëè÷åñêàÿ ðåãóëÿöèÿ ìûøå÷íîãî ñîêðàùåíèÿ
 À. Öèêëû Êîðè è
À. Öèêëû Êîðè è
àëàíèíà
 êëåòêàõ, íå ñîäåðæàùèõ ìèòîõîíäðèé
(íàïðèìåð, â ýðèòðîöèòàõ), èëè â òêàíÿõ ïðè íåäîñòàòî÷íîì ñíàáæåíèè êèñëîðîäîì
(íàïðèìåð, â àêòèâíî ðàáîòàþùèõ ìûøöàõ) ÀÒÔ (ÀÒÐ) ñèíòåçèðóåòñÿ çà ñ÷åò ïðîöåññà
ïðåâðàùåíèé ãëþêîçû â ëàêòàò, ò. å. çà ñ÷åò ïðîöåññà áðîæåíèÿ (= àíàýðîáíîãî
ãëèêîëèçà, ñì. ðèñ. 153). Ëàêòàò ïåðåíîñèòñÿ êðîâüþ â ïå÷åíü, ãäå â
ïðîöåññå ãëþêîíåîãåíåçà ñ çàòðàòîé ÀÒÔ (ñì. ðèñ. 157) âíîâü êîíâåðòèðóåòñÿ
â ãëþêîçó (öèêë Êîðè).
Ïðè èíòåíñèâíîé ðàáîòå ìûøöû ìàêñèìàëüíî
àêòèâèðóåòñÿ ãëèêîëèç. Ïðîäóêò ãëèêîëèçà, ïèðîâèíîãðàäíàÿ êèñëîòà (ïèðóâàò)
íàêàïëèâàåòñÿ â öèòîïëàçìå è íåäîñòàòî÷íî áûñòðî ïîñòóïàåò â ìèòîõîíäðèè, åñëè
îíè èç-çà íåäîñòàòêà êèñëîðîäà íå ãîòîâû ê îêèñëåíèþ ïèðóâàòà. Â àíàýðîáíûõ
óñëîâèÿõ ïèðóâàò â ðåàêöèè, êàòàëèçèðóåìîé ëàêòàòäåãèäðîãåíàçîé (ñì. ðèñ.
103) (çàêëþ÷èòåëüíûé ýòàï ãëèêîëèçà) âîññòàíàâëèâàåòñÿ äî ëàêòàòà.
Îäíîâðåìåííî
ÍÀÄÍ (NADH), êîôåðìåíò ëàêòàòäåãèäðîãåíàçû, îêèñëÿåòñÿ äî ÍÀÄ+
(NAD+), êîòîðûé âíîâü èñïîëüçóåòñÿ íà îêèñëèòåëüíîì ýòàïå
ãëèêîëèòè÷åñêîãî ïóòè. Ýòîé ðåàêöèè ñïîñîáñòâóåò îòíîñèòåëüíî âûñîêîå îòíîøåíèå
ÍÀÄÍ/ÍÀÄ+ â ìûøå÷íîé òêàíè. Ëàêòàò äèôôóíäèðóåò â êðîâü è ïîñòóïàåò â
ïå÷åíü, ãäå êîíâåðòèðóåòñÿ â ãëþêîçó. Òàêèì îáðàçîì, îáðàçîâàíèå ëàêòàòà
âðåìåííî çàìåíÿåò àýðîáíûé ìåòàáîëèçì ãëþêîçû è ÷àñòè÷íî ïåðåíîñèò ýòîò ïðîöåññ
èç ìûøö â ïå÷åíü.
Îáðàòíàÿ ñâÿçü, ïîäîáíàÿ öèêëó Êîðè,
ñóùåñòâóåò â öèêëå àëàíèíà, â êîòîðîì òàêæå ó÷àñòâóåò ïèðóâàò.
Öèêë àëàíèíà áåðåò íà÷àëî ñ ïðîòåîëèçà áåëêîâ. Îáðàçóþùèåñÿ àìèíîêèñëîòû
â ðåçóëüòàòå òðàíñàìèíèðîâàíèÿ â ïðèñóòñòâèè ôåðìåíòîâ ïðåâðàùàþòñÿ â
α-êåòîêèñëîòû (íà ñõåìå íå ïðèâåäåíî, ñì. ðèñ. 181), êîòîðûå â îñíîâíîì âêëþ÷àþòñÿ
â öèêë òðèêàðáîíîâûõ êèñëîò (öèòðàòíûé öèêë) (ñì. ðèñ. 183).Îäíîâðåìåííî â
ðåàêöèè, êàòàëèçèðóåìîé àëàíèíòðàíñàìèíàçîé, àìèíîãðóïïû èç ðàçíûõ àìèíîêèñëîò
ïåðåíîñÿòñÿ íà èìåþùèéñÿ ñóáñòðàò, ïèðóâàò. Îáðàçóþùèéñÿ àëàíèí ïîñòóïàåò
â êðîâü è ïåðåíîñèòñÿ â ïå÷åíü. Òàêèì îáðàçîì, öèêë àëàíèíà ñëóæèò êàíàëîì
ïåðåäà÷è àçîòà è ïðåäøåñòâåííèêîâ ãëþêîçû â ïå÷åíü, êîòîðàÿ ÿâëÿåòñÿ ìåñòîì
ñèíòåçà êîíå÷íûõ ïðîäóêòîâ àçîòèñòîãî îáìåíà, íàïðèìåð ìî÷åâèíû (ñì. ðèñ.
185).
Ñëåäóåò íàïîìíèòü, ÷òî ïðè àíàýðîáíîì
ãëèêîëèçå îáðàçóþòñÿ êèñëîòû, êîòîðûå, íå ïðèíèìàÿ ó÷àñòèå â ïîñëåäóþùåì îáìåíå,
ñóùåñòâóþò â ôîðìå àíèîíîâ. Ïîýòîìó ïðè èíòåíñèâíîì àíàýðîáíîì ãëèêîëèçå ðÍ
ìûøå÷íîé êëåòêè ìîæåò ïîíèçèòüñÿ íàñòîëüêî, ÷òî ñîêðàùåíèå ñòàíåò íåâîçìîæíûì.
Îáû÷íî ýòîãî íå ïðîèñõîäèò áëàãîäàðÿ áûñòðîìó âûõîäó êèñëûõ ìåòàáîëèòîâ (ëàêòàòà
è ïèðóâàòà) â êðîâü, êîòîðàÿ òàêæå ìîæåò îêàçàòüñÿ çàêèñëåííîé
(ìåòàáîëè÷åñêèé àöèäîç).
Á. Ìåòàáîëèçì áåëêîâ è
àìèíîêèñëîò
Ñêåëåòíûå ìûøöû àêòèâíî ó÷àñòâóþò â
ìåòàáîëèçìå àìèíîêèñëîò. Ýòî íàèáîëåå âàæíûé ó÷àñòîê äåãðàäàöèè ðàçâåòâëåííûõ
àìèíîêèñëîò (Val è Ile, ñì. ñ. 402). Ðÿä äðóãèõ àìèíîêèñëîò òàêæå
äåãðàäèðóþòñÿ ïðåèìóùåñòâåííî â ìûøöàõ. Îäíîâðåìåííî èäåò ðåñèíòåç è
âûñâîáîæäåíèå â êðîâü àëàíèíà è ãëóòàìèíà. Ýòè àìèíîêèñëîòû ñëóæàò
ïåðåíîñ÷èêàìè àçîòà, îáðàçóþùåãîñÿ ïðè ðàñùåïëåíèè áåëêîâ, â ïå÷åíü (öèêë
àëàíèíà) è ïî÷êè (ñì. ðèñ. 319).
Ïðè ãîëîäàíèè ìûøå÷íûå áåëêè
ñëóæàò ýíåðãåòè÷åñêèì ðåçåðâîì îðãàíèçìà. Îíè ãèäðîëèçóþòñÿ äî àìèíîêèñëîò,
êîòîðûå ïîñòóïàþò â ïå÷åíü. Çäåñü óãëåðîäíûé ñêåëåò àìèíîêèñëîò êîíâåðòèðóåòñÿ â
ïðîìåæóòî÷íûå ïðîäóêòû öèòðàòíîãî öèêëà, â òîì ÷èñëå â àöåòîàöåòèë-ÊîÀ è
àöåòèë-ÊîÀ (ñì. ðèñ. 183). Ýòè àìôèáîëè÷åñêèå ñîåäèíåíèÿ îêèñëÿþòñÿ â öèêëå
òðèêàðáîíîâûõ êèñëîò èëè âêëþ÷àþòñÿ â ïðîöåññ
ãëþêîíåîãåíåçà.
Ñèíòåç è ðàñùåïëåíèå ìûøå÷íûõ áåëêîâ
êîíòðîëèðóþòñÿ ãîðìîíàìè. Òåñòîñòåðîí è ñèíòåòè÷åñêèå àíàáîëèêè
ñòèìóëèðóþò áèîñèíòåç áåëêà; íàïðîòèâ, êîðòèçîë ïîäàâëÿåò îáðàçîâàíèå
ìûøå÷íûõ áåëêîâ.
Áåëêè àêòèí è ìèîçèí ñîäåðæàò îñòàòêè
ãèñòèäèíà, ìåòèëèðîâàííîãî íà ñòàäèè ïîñòòðàíñëÿöèîííîé ìîäèôèêàöèè. Ïðè
ðàñùåïëåíèè ýòèõ áåëêîâ îáðàçóåòñÿ 3-ìåòèëãèñòèäèí, êîòîðûé äàëüøå íå
ðàçðóøàåòñÿ. Êîëè÷åñòâî ìåòèëãèñòèäèíà â ìî÷å ñëóæèò ìåðîé äåãðàäàöèè ìûøå÷íûõ
áåëêîâ.
Источник
Дано определение молочной кислоты, описана история ее открытия и метаболизм ее превращения в организме при физических нагрузках (цикл Кори). Описывается концепция ацидоза, описывающая изменения в скелетных мышцах, которые приводят к их гипертрофии и увеличению силовых показателей.
Молочная кислота (лактат) и физические нагрузки
Определение
Молочная кислота (лактат) – конечный продукт анаэробного распада глюкозы и гликогена (гликолиза).
История открытия
1780 году шведский химик Карл Вильгельм Шилле выделил молочную кислоту из молока. А в 1808 году Йенс Якоб Берцелиус открыл, что молочная кислота образуется в скелетных мышцах при выполнении физических упражнений.
Молочная кислота и физические нагрузки
Практически при любой физической нагрузке для получения АТФ используется гликоген скелетных мышц. Его концентрация в скелетных мышцах при интенсивных физических нагрузках быстро снижается. Одновременно в скелетных мышцах образуется и накапливается молочная кислота.
Формула молочной кислоты (С3H6O3).
Цикл Кори
Циклический путь метаболизма молочной кислоты в скелетных мышцах открыт американским биохимиком, нобелевским лауреатом Герти Терезой Кори. По другим источникам открытие цикла Кори приписывается нобелевским лауреатом супругам Карлу и Герти Кори. Он описывает превращения молочной кислоты в организме человека. Большая часть молочной кислоты, которая образуется в организме во время физических нагрузок включается в метаболические процессы непосредственно в мышцах и под влиянием фермента лактатдегидрогеназы (ЛДГ) превращается в пировиноградную кислоту, которая затем в митохондриях окисляется до углекислого газа и воды. Другая часть молочной кислоты через кровеносные капилляры проникает в кровь и доставляется в печень, где включается в метаболические реакции, приводящие к синтезу гликогена. Незначительное количество молочной кислоты может выводиться из организма с мочой и потом. Гликоген печени используется организмом для восстановления энергетических источников скелетных мышц.
Концепция ацидоза
Одной из концепций, объясняющей возникновение острых болезненных ощущений, возникающих как во время, так и после тренировки, является предположение, что накопление молочной кислоты в мышечных волокнах является пусковым механизмом целого ряда биохимических реакций.
Во-первых, молочная кислота повышает кислотность внутри мышечных волокон. Изменение рН саркоплазмы мышечных волокон с 7,1 до 6,5 (то есть повышение кислотности) при сильном утомлении снижает активность ключевых ферментов гликолиза – фосфорилазы и фосфофруктокиназы. При значении рН саркоплазмы равном 6,4 расщепление гликогена прекращается. Это вызывает резкое снижение уровня АТФ и развитие утомления (Н.И. Волков с соавт., 2000).
Во-вторых, повышение концентрации молочной кислоты в мышечных волокнах приводит к увеличению проницаемости их мембраны, повышению осмотического давления, в результате чего в мышечные волокна поступает вода. Возникает отёк, мышечные волокна «разбухают» и сдавливают болевые рецепторы мышц. Это ощущается как «жжение» в мышцах (М.И. Калинский, В.А. Рогозкин, 1989). Спортсмены называют это явление «мышцы забиты».
Молочная кислота и лактат
Следует отметить, что молочная кислота и лактат — не одно и то же. Лактат — это соль молочной кислоты. Образовавшаяся в результате гликолиза в скелетных мышцах молочная кислота почти полностью диссоциирует на ионы водорода и соединение, которое соединяется с ионами натрия или калия и образует соль (лактат), рис. 1.
Рис. 1
Поэтому в литературе часто вместо понятия «молочная кислота» используется термин «лактат». Содержание молочной кислоты и лактата имеет взаимосвязь с кислотностью внутри мышечных волокон (то есть с pH саркоплазмы). При pH в интервале от 6.5 (полное утомление) до 7,1 (норма) в мышечных волокнах накапливается, выводится и перерабатывается именно лактат.
В течение нескольких часов лактат удаляется из мышечных волокон. Если после физической нагрузки выполнить 10-15 минутную аэробную работу (например, бег или педалирование на велосипеде), лактат из мышц выведется еще быстрее.
Новые исследования свидетельствуют о том, что основным повреждающим агентом являются ионы водорода (Н+). Утомление в скелетных мышцах вызывает ацидоз — накопление ионов водорода и смещение pH саркоплазмы в кислую сторону (R. A. Robergs et al., 2004).
Молочная кислота, гипертрофия и сила скелетных мышц
Предполагается, что накопление кислых продуктов в мышечных волокнах (ацидоз) лежит в основе их повреждения, что в последствии приводит к их гипертрофии по миофибриллярному типу и росту силы. Следовательно, удалять молочную кислоту из скелетных мышц после тренировки не следует, так как это основной фактор, повреждающий мышечные волокна. Это предположение подтверждается опытом тренировок чемпионки мира в беге на 400 м с барьерами Марины Степановой и ее тренера Вячеслава Владимировича Степанова. Стремясь увеличить силовые показатели мышц ног, М. Степанова и В. Степанов в цикле своих статей «Анаэробика» указывают, что «есть смысл ненадолго (на несколько часов) «повариться» в молочнокислой среде, а «разогнать» ее позже (к примеру, вечерними упражнениями)».
Литература
- Калинский, М.И. Биохимия мышечной деятельности / М.И. Калинский, В.А. Рогозкин. – Киев: Здоровья, 1989.– 144 с.
- Михайлов С.С. Спортивная биохимия. – М.: Советский спорт, 2009.– 348 с.
- Самсонова, А.В. Гипертрофия скелетных мышц человека: Учеб. пособие. 5-е изд. /А.В. Самсонова. – СПб: Кинетика, 2018.– 159 с.
- Самсонова, А. В. Гормоны и гипертрофия скелетных мышц человека: Учеб. пособие. – СПб: Кинетика, 2019.– 204 c.: ил.
- Степанова, М. Анаэробика /М. Степанова, В. Степанов // Легкая атлетика, 2011 № 7-8. С. 24-27.
С уважением, А.В. Самсонова
Источник
Глюконеогенез
— это образование глюкозы вновь
из неуглеводных компонентов: пирувата,
лактата,гликогенных аминокислот,
глицерина,любого соединения, которое
в процессе катаболизма может быть
превращено в пируват или один из
метаболитов цикла Кребса.
Глюконеогенез
протекает в: печени, корковом веществе
почек,слизистой кишечника.За счёт
глюконеогенеза в условиях углеводного
голодания образуется 80 г глюкозы.
Глюконеогенез–это
частично обращённый гликолиз.
Три
реакции гликолиза необратимы, поэтому
используются другие ферменты.
Пируваткиназная реакция заменяется
двумя:пируваткарбоксилазной реакцией
и фосфоенолпируваткарбоксикиназной
реакцией.
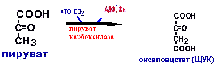

Между
этими реакциями существует челночный
механизм.ЩУК не может самостоятельно
выйти из митохондрий.ЩУК + НАДН+Н =
малат + НАД. В цитоплазме малат окисляется
цитоплазматической малатдегидрогеназой
до ЩУК

От
ФЕП до ФФК реакции все реакции идут в
обратной последовательности
гликолиза:Фосфофруктокиназная реакция
заменяется фруктозодифосфатазной
реакцией.
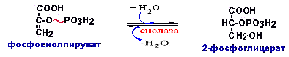
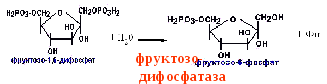
Биологическая
роль глюконеогенезаизбавление от
лактата (85% лактата идёт на глюконеогенез,
15% — окисляется до СО2, Н2О и энергии),
связь обменов, получение эндогенной
глюкозы.
Итоговое
уравнение глюконеогенеза
2
лактата + 6АТФ + 4Н2О + 2НАДН+Н глюкоза
+ 6АДФ + 6Фн + 2НАД
АТФ
используется в пируваткарбоксилазной,
фосфоенолпируваткарбоксикиназной,
фосфоглицераткиназной реакциях. НАДН+Н
необходим для ГАФДГ. 2Н20 участвуют в
енолазной реакции. 2Н20 – в фосфатазных
реакциях.
Регуляция
глюконеогенеза4 фермента определяют
скорость процесса. При уменьшении АТФ
и НАД тормозится глюконеогенез. Ключевые
ферменты стимулируются АТФ,ингибируются
– АДФ и АМФ. Инсулин – репрессор ферментов
глюконеогенеза.Процесс активируется:
глюкокортикоидами, жирными кислотами,
избытком лактата в крови, глюкагоном.
Цикл
Кори
осуществляет связь между
гликолизом в мышце при активной работе
и глюконеогенезом в печени. При работе
лактат поступает из мышц в кровь и
печень.

Мышца
Кровь
Печень
3)Больной 50 лет поступил в клинику с жалобами на резкие боли в области сердца, слабость. Активность каких ферментов следует определить в крови больного для исключения инфаркта миокарда?
МБ+КФК
ЛДГ
АСТ/АЛТ
Миоглобин
тропонин
Билет
23
1)Холестерин, его биологическая роль, биосинтез. Гиперхолестеринемии. Атеросклероз.
Холестерин:
циклический
ненасыщенный спирт,нерастворим
в воде,в
основе холестерина лежит кольцо
циклопентанпергидрофенантрена.
Содержится
в: коре надпочечников, мозге, нервной
ткани, мышцах, соединительной ткани,
жировой ткани.
Биороль:
синтез
желчных кислот,синтез
половых гормонов,синтез
кортикостероидов,синтез
витамина D3,входит
в состав клеточных мембран, миелиновых
оболочек,участвует
в образовании желчных камней, развитии
атеросклероза.
Пищевые
источники холестерина:
печень,
яйца,
мясо,
мозг,
икра.
Синтезируется
в:
эндоплазматическом
ретикулуме, цитозоле печени (80%),
коже,
стенке
тонкой кишки.
Синтез
холестерина:
включает
35 реакций,идёт
в 3 стадии:
образование
из ацетил-КоА мевалоновой кислоты,образование
из мевалоновой кислоты сквалена,циклизация
сквалена в холестерин.
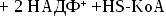
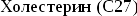
Холестеринемии:
1)Наследственная.
В
сыворотке крови увеличено содержание
холестерина, β-липопротеинов
Механизм
развития заболевания– отсутствие
или снижение количества рецепторов
клеток к ЛПНП, снижается захват и
катаболизм холестерина из ЛПНП,
увеличивается содержание холестерина
в плазме, оседание холестерина на стенки
сосудов, развитие атеросклеротических
бляшекОсложнения– ранний инфаркт миокарда, ксантоматоз,
инсульт
2)
Алиментарная гиперхолестеринемиявозникает от избытка в питании холестерина
3)Вторичная
гиперхолестеринемиявозникает
при гипотиреозе, сахарном диабете,
подагре, нефротическом синдроме
Атеросклероз:
Заболевание,
связанное с накоплением холестерина
в интиме сосудов с последующей
дегенерацией, отложением в очаг поражения
солей кальция, фиброзированием очага
и тромбозомДиагностические
критерии:гиперлипидемия,
гиперхолестеринемия
изменение
состава и соотношения транспортных
форм холестерина (увеличение ЛПНП и
уменьшение ЛПНП)Снижение
соотношения фосфолипиды
холестерин
Снижение
активности липопротеинлипазыУменьшение
в составе триацилглицеринов
полиненасыщенных жирных кислот и эфиров
холестерина
Способствуют
развитию атеросклероза:
наследственная
предрасположенность
гипертония
сахарный
диабет
ожирение
стрессы
гиподинамия
нарушение
равновесия свертывающей и противосвертывающей
системы крови.
Соседние файлы в предмете Биохимия
- #
- #
Источник


