Общество по бронхиальной астме сайты
Справочник болезней
«Не будь первым, кто испытывает новое, и последним, кто отстаивает старое»
ОПРЕДЕЛЕНИЕ
Гетерогенное заболевание, которое характеризуется хроническим воспалением дыхательных путей и диагностируется по респираторным симптомам свистящего дыхания, одышки, стеснения в груди или кашля, вариабельных по длительности и интенсивности, в сочетании с лабильной экспираторной обструкцией дыхательных путей (GINA).
Частота встречаемости триггеров при астме
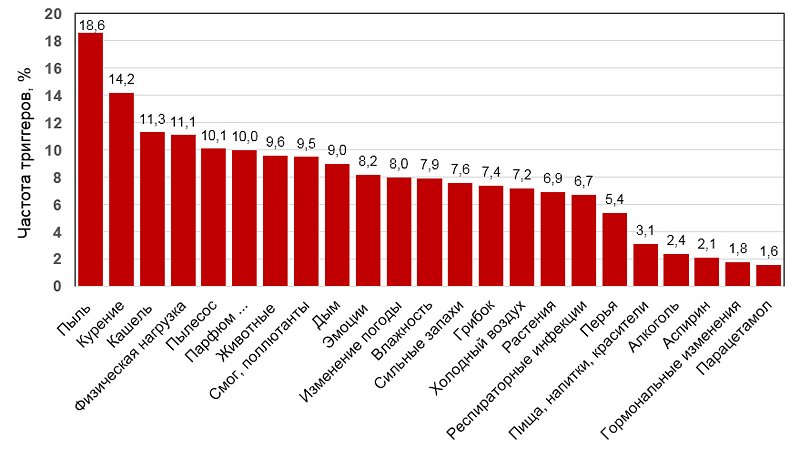
Price D, et al. J Asthma. 2014;51:127–35.
ТРИГГЕРЫ АСТМЫ
• Домашние аллергены: клещи, тараканы, животные, грибы.
• Средовые аллергены: пыльца растения.
• Профессиональные сенситизаторы: пищевая промышленность, медицина …
• Курение табака.
• Воздушные поллютанты: озон, нитрата оксид.
• Физическая нагрузка, смех, холодный воздух.
• Желудочно-пищеводный рефлюкс.
• Лекарства: бета-блокаторы, ингибиторы циклооксигеназы-1 (аспирин, нестероидные противовоспалительные препараты).
Пыльца растений
Dartmouth Electron Microscope Facility.
КЛИНИКА ВАРИАБЕЛЬНЫХ РЕСПИРАТОРНЫХ СИМПТОМОВ
• Эпизоды одышки, свистящего дыхания, стеснения в груди, кашля.
• Обычно более одного вида симптомов.
• Варьируют по времени и интенсивности.
• Ухудшение ночью, при пробуждении.
• Провокация физической нагрузкой, смехом, аллергенами, холодным воздухом, нестероидными противовоспалительными препаратами (НПВП).
• Появление или ухудшение симптомов при вирусной инфекции.
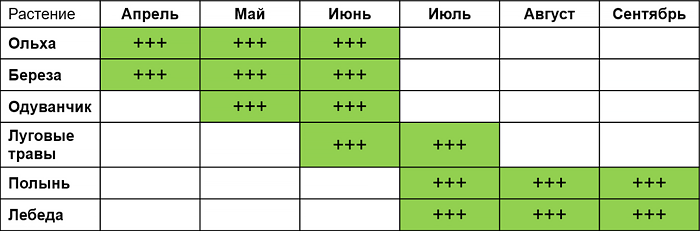
КАЛЕНДАРЬ ЦВЕТЕНИЯ РАСТЕНИЙ
ВОСПАЛЕНИЕ 2 ТИПА
• ~50% тяжелой астмы.
• Аллергическая астма.
• Аспирин-индуцированная респираторная болезнь.
• Интерлейкины IL-4, IL-5, IL-13.
• Эозинофилия крови ≥0.15•109/л.
• Эозинофилия мокроты ≥2%.
• Лечение: анти-IgE (омализумаб), анти-IL5 (бенрализумаб, меполизумаб, реслизумаб), анти-IL4 (дупилумаб).
Число обострений астмы и погода
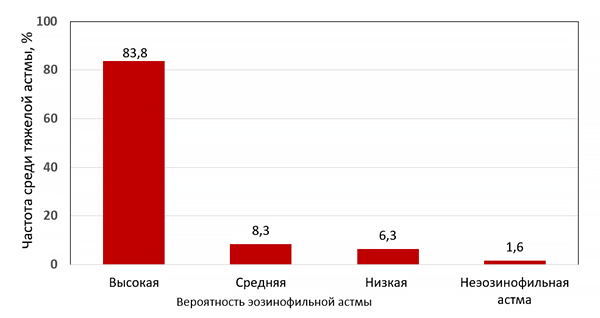
Andrew E, et al. BMJ. 2017;359.
ДИАГНОСТИКА ЛАБОРАТОРНАЯ
• Спирометрия.
• Рентгенография грудной клетки.
• Кожные аллергологические тесты (prick-test), IgE специфический.
• Эозинофилы мокроты (при тяжелой астме, ERS/ATS).
Спирометрия
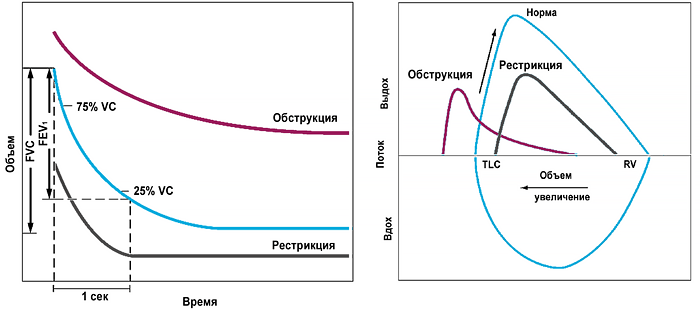
КЛАССИФИКАЦИЯ БРОНХИАЛЬНОЙ АСТМЫ
Этиология
• Алергическая.
• Неаллергическая.
• Аспирин-индуцированная респираторная болезнь.
• Профессиональная.
• Астма-ХОБЛ синдром.
Уровень контроля
• Критерии контроля: дневные симптомы >2/нед, сальбутамол >2/нед, ночные симптомы, ограничение активности.
• Контролируемая: нет критериев.
• Частично контролируемая: 1–2 критерия.
• Неконтролируемая: 3–4 критерия.
Обострение
• Легкое.
• Cредней тяжести.
• Тяжелоe.
ВАРИАБЕЛЬНАЯ БРОНХИАЛЬНАЯ ОБСТРУКЦИЯ (GINA)
• ОФВ1 (FEV1) <80% хотя бы однажды, подтвержденное снижением ОФВ1/ФЖЕЛ<75%.
• Прирост ОФВ1 >12% (+200 мл) через 10–15 мин после ингаляции 200–400 мкг сальбутамола (если прирост меньше рассмотреть альтернативный диагноз или тяжелая астма).
• Снижение ОФВ1 >20% на дозу метахолина <4 мг/мл (если ≥4 мг/мл рассмотреть альтернативный диагноз).
• Суточная вариативность ПСВ (PEF) >10% 2 раза в день в течение 2 нед. Расчет: среднее за неделю (ПСВmax – ПСВmin)/ ((ПСВmax – ПСВmin)/2).
• Вариации ОФВ1 >12% (+200 мл) между визитами вне респираторной инфекции (менее надежно).
• Прирост ОФВ1 >12% (+200 мл) или ПСВ >20% после 4 нед противовоспалительного лечения.
Ответ на бронходилататор
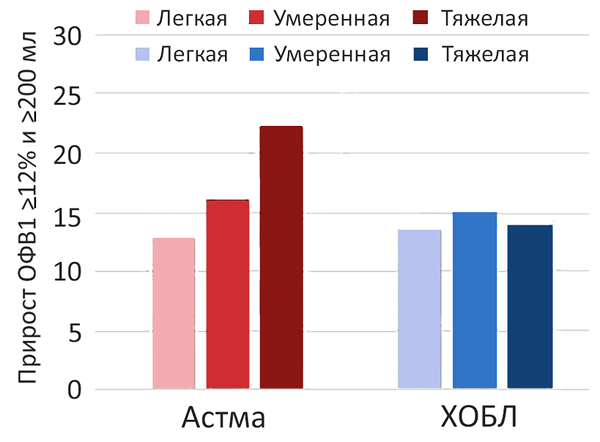
Janson C, et al. Eur Respir J. 2019;3:1900561.
ФОРМУЛИРОВКА ДИАГНОЗА
Ds: Бронхиальная астма аллергическая (полынь, береза), частично контролируемая, обострение. Аллергический ринит, конъюнктивит. [J45.0]
Ds: Бронхиальная астма, неконтролируемая, тяжелое обострение. [J46]
Фоновый Ds: Гастроэзофагеальная рефлюксная болезнь, неэрозивная форма.
Ds: Бронхиальная астма аспирин-индуцированная, частично контролируемая. [J45.1]
Сопутствующий Ds: ИБС: стабильная стенокардия III ФК. Пароксизмальная фибрилляция предсердий, EHRA 2б. ХСН II ФК.
Ds: Астма-ХОБЛ синдром. [J44.8]
ОБРАТИМЫЕ ФАКТОРЫ РИСКА ОБОСТРЕНИЯ АСТМЫ
• Неконтролируемые симптомы астмы.
• Высокие дозы сальбутамола (смертность повышена если >200 доз в мес).
• Неадекватная доза кортикостероидов: плохая приверженность, неадекватная техника ингаляции.
• Низкий ОФВ1: <60%.
• Выраженные психические расстройства или социоэкономические проблемы.
• Экспозиция курения, аллергенов.
• Коморбидность: ожирение, риносинусит, пищевая аллергия.
• Эозинофилия в мокроте или крови.
• Беременность.
Эффективность белья против клещей
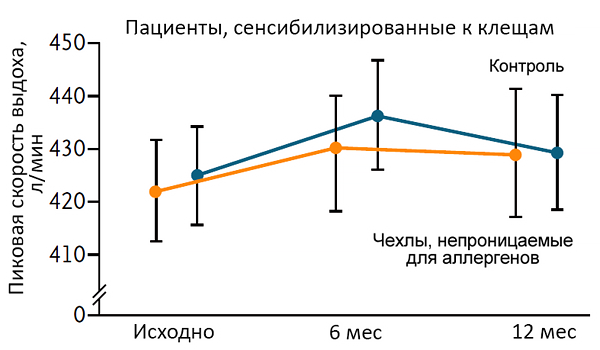
Woodcock A, et al. N Engl J Med. 2003;349:225–36.
ЛЕЧЕНИЕ АСТМЫ
• Устранение аллергенов, триггеров.
• Отказ от курения.
• Снижение массы тела.
• Дыхательные упражнения.
• Регулярные физические нагрузки.
• Контроль депрессии, тревоги, стресса.
• Сублингвальная иммунотерапия при аллергическом рините и сенсибилизации к клещам домашней пыли с персистирующей астмой, несмотря на ИКС.
• Десенсибилизацация аспирином.
• Вакцинация против гриппа (тяжелая астма, пожилые).
• Противовоспалительные препараты: кортикостероиды, модификаторы лейкотриенов (зафирлукаст, монтелукаст), анти-IgE, анти-IL5, анти-IL4.
• Бронходилататоры пролонгированные: бета2-агонисты (салметерол, формотерол), холинолитики.
• Бронхиальная термопластика.
Терапия астмы, основанная на контроле (GINA, 2019)
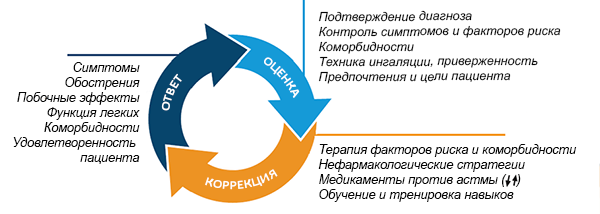
Global Strategy for Asthma Management and Prevention 2019.
ИНГАЛИРУЕМЫЕ КОНТРОЛЛЕРЫ
Кортикостероид
• Беклометазон: 100–200, 200–400, >400 мкг/сут в 2 приема.
• Будесонид [пульмикорт]: 200–400, 400–800, >800 мкг/сут в 2 приема.
• Флутиказона пропионат [фликсотид]: 100–250, 250–500, >500 мкг/сут в 2 приема.
Кортикостероид + бета2-агонист
• Будесонид/формотерол: 80–160/4.5, 320/9 [симбикорт], 200–400/12 [форадил комби] мкг 2 раза.
• Флутиказона флуорат/вилантерол [релвар]: 100–200/25–50 мкг однократно.
• Флутиказона пропионат/салметерол [серетид]: 50–125–250–500/25–50 мкг 2 раза.
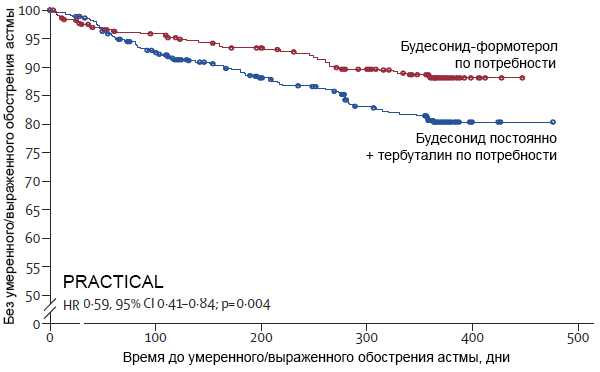
Терапия легкой/умеренной астмы (PRACTICAL)

Hardy J, et al. The Lancet. 2019;10202:919–28.
СТУПЕНЧАТЫЙ КОНТРОЛЬ СИМПТОМОВ (GINA, 2019)
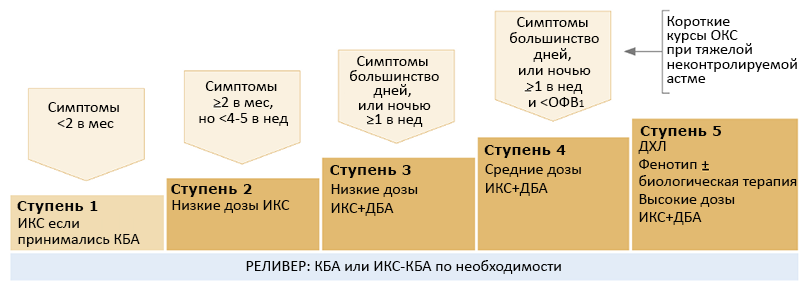
АЛР — антагонисты лейкотриеновых рецепторов, ДБА — длинные бета2-агонисты, ИКС — ингалируемые кортикостероиды, КБА — короткие бета2-агонисты, ОКС — оральные кортикостероиды.
СТУПЕНЧАТАЯ ПОДДЕРЖИВАЮЩАЯ ТЕРАПИЯ АСТМЫ (GINA)
1 ступень
• ИКС-формотерол в низких дозах.
2 ступень
• ИКС (беклометазон 50–100 мкг 2 раза) в низких дозах.
• ИКС-формотерол в низких дозах по необходимости.
3 ступень
• ИКС-пролонгированные бета2-агонисты в низких дозах (будесонид-формотерол 80–160/4.5 мкг, флутиказона пропионат-салметерол 50/25 мкг 2 раза).
• ИКС в средних дозах (беклометазон 100–200 2 раза).
4 ступень
• ИКС-пролонгированные бета2-агонисты в средних дозах (будесонид-формотерол 320/9 мкг, флутиказон-салметерол 125–250/25 мкг 2 раза).
• ИКС в высоких дозах (беклометазон >200 мкг 2 раза).
• ± Тиотропиум (5 мкг однократно [спирива респимат]).
5 ступень
• ИКС-пролонгированные бета2-агонисты в высоких дозах.
• + Тиотропиум, анти-IgE, анти-IL5, анти-IL4.
• + Преднизолон ≤7.5 мг/сут.
Плацебо эффект при астме
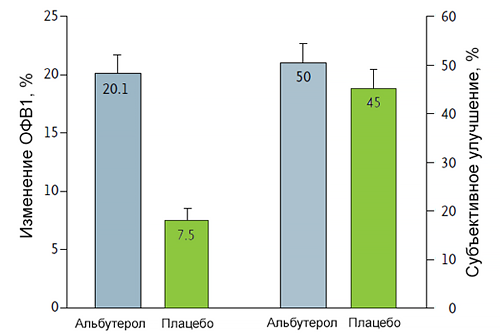
Wechsler M, et al. New Engl J Med. 2011;365:119–26.
САМОЛЕЧЕНИЕ УХУДШЕНИЯ БРОНХИАЛЬНОЙ АСТМЫ (GINA)
• Повышение частоты использования сальбутамола (+ спейсер).
• Учащение приема сальбутамола или снижение PEF >20% в течение >2 сут требует увеличение дозы контроллеров.
• Удвоение дозы ингалируемых кортикостероидов.
• Повышение дозы комбинированных препаратов (максимальная доза формотерола 72 мкг/сут).
• Преднизолон 50 мг/сут однократно 5–7 дней, отменять сразу.
Опасность монотерапии бета-агонистами
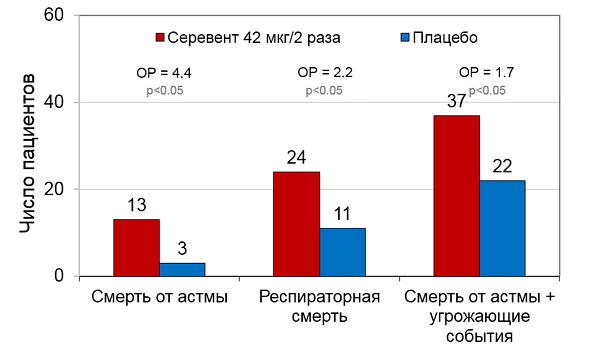
SMART. Chest 2006;129:15–26.
КРИТЕРИИ ТЯЖЕСТИ ОБОСТРЕНИЯ (GINA)
Легкое обострение
• Одышка при ходьбе, разговор предложениями, свистящее дыхание умеренное на выдохе, могут лежать.
• Пульс <100/мин, >20 дыханий в мин, PEF >80%, SpO2 >95%.
Умеренное обострение
• Одышка при разговоре, разговор фразами, свистящее дыхание громкое, предпочитают сидеть.
• Пульс 100–120/мин, >20 дыханий в мин, PEF 50–80%, SpO2 90–95%.
Тяжелое обострение
• Одышка в покое, разговор словами, свистящее дыхание громкое, ортопноэ, используют вспомогательные мышцы, возбуждение.
• Пульс >120/мин, >30 дыханий в мин, PEF <50% (<100 мл/мин), SpO2 <90%.
Угроза остановки дыхания
• Отсутствие свистов, слабые дыхательные усилия, цианоз, оглушенность, брадикардия, аритмии.
• PEF <33%, SpO2 <90%.
Бронхиальная термопластика при рефрактерной астме

До и после термопластики. d’Hooghe J, et al. Pharmacology&Therapeutics. 2017.
ЛЕЧЕНИЕ ОБОСТРЕНИЯ БРОНХИАЛЬНОЙ АСТМЫ (GINA)
Амбулаторное лечение
• Увеличить ингаляции реливера с низкодозовым будесонидом/формотеролом (80–160/4.5): общая доза формотерола до 72 мкг.
• Короткодействующий бета2-агонист: сальбутамол через ингалятор 4–10 вдохов каждые 20 мин первый час, далее от 4–10 вдохов каждые 1–4 ч (через спейсер экономнее небулайзера). Через небулайзер: 2.5–5 мг каждые 20 мин первый час, затем 2.5–10 мг через 1–4 ч по необходимости или 10–15 мг/ч постоянно.
• Увеличение в 4 раза дозы контроллера (кортикостероид или кортикостероид/формотерол).
• Преднизолон 40–50 мг/сут однократно 5–7 дней: нет эффекта 48 ч, ОФВ1/ПСВ <60%, внезапные тяжелые обострения в анамнезе.
• Кислород, поддерживая SpO2 93–95%.
Стационарное лечение
• Сальбутамбол + ипратропиум: через небулайзер 0.5 мг каждые 20 мин до 3 доз, далее по необходимости или через дозированный ингалятор 8 вдохов каждые 20 мин до 3 ч.
• Кортикостероид перорально или внутривенно.
• Магнезия внутривенно: 2 г за 20 мин.
• Искусственная вентиляция легких.
Источник
Post navigation
Вот тут как говорится на вкус и цвет…Я по началу тоже предполагал, что бронхиальная астма и климат могут быть каким то образом взаимосвязаны и взаимосвязаны как правило через «посредников» в виде бронхитов.
Что дело всё в климате и тому были доказательства в виде увеличения количества приступов во время непогоды. Как же, климат меняется, начинается дождь или снег, снижается температура (или наоборот повышается) или иная какая непогода наступает и начинаются приступы удушья, значит всё дело в нём. Но не всё так просто Continue reading →
Вы наверно хотите знать как при бронхиальной астме дают инвалидность?
Отвечу:
астма, её степень тяжести и инвалидность не имеют между собой ничего общего.Это мнение сложилось из моего личного опыта и опыта моих знакомых.
— Как так? – спросите Вы
— Да вот так!
Теперь подробнее.Будь у Вас хоть десять раз бронхиальная астма и показания на инвалидность, вам её не видать пока Continue reading →
Нет, с астмой в армию не берут. Процедура достаточно проста.
На комиссии в военкомате призывник проходит всех врачей и когда у него спрашивают, а это обязательно спросят:
– Есть ли жалобы на здоровье?
– Страдаете ли хроническими заболеваниями?
Тут скрывать нечего, а потому ответствовать нужно честно ибо не чего подводить ни себя, ни других. Так как в казарме спать всем разом, а приступы у астматика бывают и ночью, то нужно говорить правду и только правду. Continue reading →
Астма и алкоголь как к этому относиться?
По разному. Смотря какая астма и какой алкоголь и для чего собственно он.
Алкоголь можно использовать для лечения, а можно и для банальной выпивки. Подход разный. Я не хочу что бы данная статья служила оправданием тем, кто злоупотребляет алкоголем. Она не для них. Эти люди будут просто искать лазейку чтобы выпить.
Очень часто я слышал рецепты от астматиков и от здоровых людей по поводу применения спиртного. Большинство из них Continue reading →
Пишет пользователь Галина
Прошла все круги ада, пока получила бесплатные лекарства. Фишка врачей в этом случае заключалась в том, что диагноз только еще выставлен и чтобы получать лекарства бесплатно, нужно дождаться, пока меня внесут в реестр на получение бесплатных лекарств, а на это уходит 2-3 недели. Но, учитывая, что все происходит в конце года Continue reading →
Ага, работает сайт. Замечательно. Не закрыли еще. Тоже хорошо. Тогда продолжаю.
Да, сайт действительно нужен и вот почему. В нашем мире и в наше время почему то человеческая жизнь почти не ценится, в отличии скажем от советских времен.
Ну это понятно, хорошей жизни на всех не хватит, а чем больше людей будут уходить тем больше благ достанется верхушке. Continue reading →
Спрашивает Галина
Здравствуйте! Кто-нибудь знает, возможно ли полное избавление от астмы, если выявлен аллерген? Как вы относитесь к лечению такого типа астмы путем введения малых доз аллергенов в организм?
Спрашивает Ольга556
Здравствуйте , мой ребенок болеет с 1,5 лет — приступы частые до 2х раз в месяц с бронхоспазмами , стенозом. Отек происходит очень быстро 7-15 мин, температуры при этом никогда нет , течение болезни после купирования приступа протекает по разному. Можем раздышаться за день два и забыть Continue reading →
Пишет пользователь Лиа
Я очень хочу помочь людям избавиться от астмы. Я это сделала. Мне 52 года, их них них 20 лет потрачено на борьбу с астмой. По образованию я врач, поэтому традиционная медицина сразу была исключена, следуя которой ты приходишь к инвалидности. Я пошла путем голодания и уринотерапии, этот путь нелегкий, но я добивалась хорошего результата, астма отступала, придерживалась определенной диеты, но… Continue reading →
Пишет пользователь Fiore
Традиционная астма подразумевает бронхоспазм на уровне средних и крупных бронхов. Это везде описываемые и хорошо слышимые хрипы и свист во время приступа. Но есть ещё и мелкие бронхи. Не все врачи их слышат, а некоторые вообще не признают, что бронхоспазм мелких бронхов мешает жить.
При таком течении на первый план выходят одышка и ухудшение переносимости физической нагрузки, свист появляется при форсированном выдохе, когда включаются и мелкие бронхи.
Если есть астматики с таким же течением, хотелось бы узнать их опыт диагностики, лечения и жизни с этим диагнозом.
Источник
Для цитирования. А.А. Зайцев. Бронхиальная астма у взрослых: ключевые вопросы диагностики и фармакотерапии // РМЖ. 2015. № 18. С. 1096–1100.
«Астма – это когда ходишь в четверть шага, думаешь в четверть мысли,
работаешь в четверть возможности и только задыхаешься в полную мощь»
К.Г. Паустовский
Бронхиальная астма (БА) относится к числу наиболее распространенных и социально значимых заболеваний человека. Так, среди взрослого населения европейских стран распространенность БА составляет 6–9%, в США – 11% [1–5]. Согласно официальной статистике, распространенность астмы в России составляет около 3%. В то же время результаты отдельных эпидемиологических исследований позволяют уточнить истинную распространенность БА в Москве – 6,4%, Екатеринбурге – 6,2%, Иркутске – 5,6%. Экспертами Российского респираторного общества признается, что распространенность БА среди детей составляет от 5,6 до 12,1%, а среди взрослых – 5,6–7,3%. В абсолютных цифрах можно предположить, что в России общее число больных БА составляет как минимум 7 млн человек [6, 7].
Проблема усугубляется тем, что больные БА нуждаются в продолжительной медицинской помощи, что требует больших экономических затрат. В развитых странах затраты на ведение пациентов с БА составляют 1–2% от бюджетных средств, выделяемых на здравоохранение. Экономическое бремя БА связано не только с высокими расходами на лечение, но и с затратами, связанными с потерей работоспособности и снижением качества жизни больных [1]. Согласно российским данным, общие расходы на ведение больных БА в 2007 г. составили более 11 млрд руб. [8]. Из них порядка 6 млрд руб. составляют расходы на оказание неотложной помощи и стационарное лечение пациентов в связи с обострением заболевания или ухудшением состояния из-за недостаточно эффективной терапии. Очевидный рост затрат вследствие неадекватной базисной терапии подтверждается целым рядом исследований [9–11]. Таким образом, рациональный выбор терапии для достижения и поддержания контроля над клиническими проявлениями БА является чрезвычайно важной задачей [12–14].
Типичные симптомы БА, отмечаемые большинством пациентов, включают: экспираторную одышку, свистящее дыхание, кашель и заложенность в груди [12]. Наиболее часто симптомы БА проявляются ночью или сразу после пробуждения, а также после физической нагрузки, что зачастую приводит к ограничению физической активности пациентов. Важным этапом клинической оценки БА является оценка внелегочных проявлений аллергии – прежде всего аллергического ринита, конъюнктивита, атопического дерматита. Диагноз БА устанавливается на основании жалоб и анамнестических данных пациента, клинико-функционального обследования с оценкой обратимости бронхиальной обструкции, специфического аллергологического обследования (кожные тесты с аллергенами и/или специфический иммуноглобулин класса Е (IgЕ) в сыворотке крови) и исключения других заболеваний. Важнейшим фактором диагностики является тщательный сбор анамнеза, который укажет на причины возникновения, продолжительность и разрешение симптомов, наличие аллергических реакций у пациента и его кровных родственников, причинно-следственные особенности возникновения признаков болезни и ее обострений.
Начало заболевания БА в большинстве случаев приходится на детский и юношеский возраст. Однако дебют болезни может быть в любом возрасте, и начало болезни у взрослых и даже пожилых пациентов не является редкостью. Вместе с тем бронхообструктивный синдром, впервые развившийся в пожилом возрасте, требует проведения дифференциальной диагностики с целым рядом сходных по клиническому течению заболеваний (хроническая обструктивная болезнь, тромбоэмболия легочной артерии, острая левожелудочковая недостаточность, опухолевый процесс в легких и др.). Важно установить связь появления симптомов БА после контакта с аллергеном, сезонную вариабельность симптомов, сочетание с ринитом, наличие в семейном анамнезе атопии или БА. Иногда встречается кашлевой вариант БА, когда единственным проявлением заболевания является кашель, беспокоящий преимущественно в ночные часы.
Клинические признаки, повышающие вероятность наличия БА [12]:
1) наличие более одного из следующих симптомов: хрипы, удушье, чувство заложенности в грудной клетке и кашель, особенно в случаях ухудшения симптомов ночью и рано утром; возникновение симптомов при физической нагрузке, воздействии аллергенов и холодного воздуха; возникновение симптомов после приема ацетилсалициловой кислоты или β-блокаторов;
2) наличие атопических заболеваний в анамнезе;
3) наличие астмы и/или атопических заболеваний у родственников;
4) распространенные сухие свистящие хрипы при аускультации;
5) низкие показатели пиковой скорости выдоха (ПСВ) или объема форсированного выдоха за 1 с (ОФВ1) (ретроспективно или в серии исследований), необъяснимые другими причинами;
6) эозинофилия периферической крови, необъяснимая другими причинами.
Специальные методы диагностики БА включают исследование вентиляционной функции легких с оценкой обратимости бронхиальной обструкции, выявление бронхиальной гиперреактивности, проведение специфического аллергологического обследования. При проведении спирометрии важным параметром является ОФВ1, указывающий на степень бронхиальной обструкции. Бронходилатационный тест считается положительным, если после ингаляции бронходилататора величина прироста ОФВ1 составляет ≥12% от должного или абсолютный прирост составляет 200 мл и более (для заключения о положительном тесте обязательно достижение обоих критериев). У пациентов с показателями спирометрии в пределах нормы следует провести дополнительное исследование для выявления бронхиальной гиперреактивности – ингаляционный тест с метахолином. Тест является высокочувствительным, поэтому положительный результат является подтверждением БА. Мониторирование ПСВ используется для выявления повышенной суточной вариабельности показателей, характерных именно для БА (вариабельность показателей ПСВ или >30% в течение 1 сут). Характерным признаком БА является эозинофилия периферической крови (более 0,4х109/л), в анализах мокроты обнаруживаются также эозинофилы, кристаллы Шарко – Лейдена, спирали Куршмана. Среди дополнительных тестов стоит упомянуть аллергологическое обследование, позволяющее выявить чувствительность к различным аллергенам, определение общего и специфических IgE. Проба с физической нагрузкой используется для подтверждения БА у детей и подростков. После 7-минутных упражнений более чем у 90% детей с БА наблюдается снижение ОФВ1.
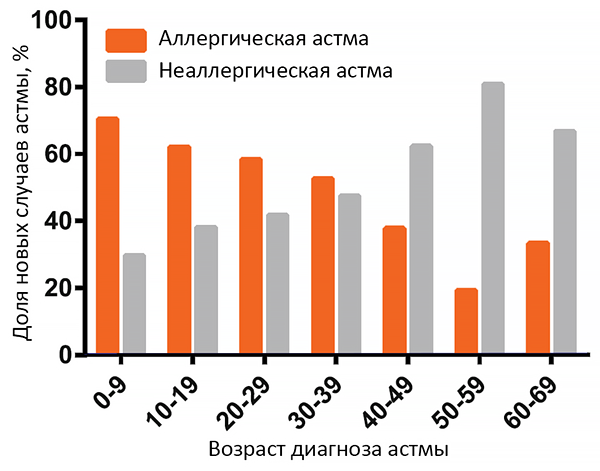
В зависимости от факторов, провоцирующих обострение, выделяют различные клинические формы БА: аллергическая (атопическая), аспириновая, астма физического усилия и др. Аллергические механизмы имеют преобладающее значение (~80% случаев) в развитии детской астмы и обнаруживаются более чем в 50% случаев у взрослых. Такая астма нередко сочетается с аллергическим ринитом, конъюнктивитом и дерматитом. Отмечается гиперчувствительность к различным аллергенам. Для аспириновой астмы характерна триада симптомов: БА, полипозный риносинусит и непереносимость нестероидных противовоспалительных препаратов. Астма физического усилия характерна для молодого и детского возраста (приступ бронхоспазма провоцируется физической активностью – ходьбой, бегом и т. д., причем симптомы возникают не во время действия фактора, а через 5–30 мин после него. Нередко провоцирующим фактором обострения БА является вирусная инфекция, поэтому говорят об инфекционно-зависимой астме. В ряде случаев выделить какой-либо механизм не представляется возможным, поэтому в клинических диагнозах встречается термин «смешанная форма БА».
По степени тяжести БА делится на интермиттирующую и персистирующую (легкой, средней и тяжелой степени тяжести) (табл. 1).
В руководстве GINA (The Global Initiative for Asthma) в настоящее время рекомендована 3-уровневая классификация БА по уровню контроля клинических признаков и характеристике внешнего дыхания (контролируемая, частично контролируемая и неконтролируемая БА) (табл. 2). Такой подход лучше описывает состояние болезни на фоне проводимых лечебных мероприятий, отражает понимание того, что тяжесть БА зависит не только от выраженности симптомов заболевания, но и от ответа на терапию.
Целями фармакотерапии БА являются достижение и поддержание клинического контроля над заболеванием в течение длительного периода времени с учетом безопасности терапии, потенциальных нежелательных реакций и стоимости лечения [12, 14–15]. Увеличение потребности в препаратах неотложной помощи, особенно ежедневное их использование, указывает на утрату контроля над БА и необходимость пересмотра терапии. Если текущая терапия не обеспечивает контроля над БА, необходимо увеличивать объем терапии до достижения контроля. В случае достижения частичного контроля над БА следует рассмотреть возможность увеличения объема терапии с учетом наличия более эффективных подходов к лечению, их безопасности, стоимости и удовлетворенности пациента достигнутым уровнем контроля. При сохранении контроля над БА в течение 3 мес. и более возможно уменьшение объема поддерживающей терапии с целью установления минимального объема терапии и наименьших доз препаратов, достаточных для поддержания контроля.
Фармакотерапия БА включает в себя 2 вида препаратов: препараты неотложной помощи (купирование бронхоспазма) и препараты для базисной («поддерживающей») терапии. К первым относятся β2-агонисты короткого и длительного действия (сальбутамол, фенотерол, формотерол), ингаляционные антихолинергические препараты (ипратропия бромид, тиотропия бромид). Препараты базисной терапии: ингаляционные глюкокортикостероиды (ИГКС) и системные кортикостероиды, комбинированные препараты (пролонгированные β2-агонисты + ИГКС), пролонгированные теофиллины, антагонисты лейкотриеновых рецепторов и антитела к IgE.
ИГКС являются препаратами первой линии в терапии БА, они показаны для лечения персистирующей БА любой степени тяжести [12–14]. ИГКС, составляющие основу базисной противовоспалительной терапии БА, предотвращают развитие симптомов и обострений болезни, улучшают функциональные показатели легких. Раннее назначение ИГКС может улучшить контроль БА и нормализовать функцию легких, а также предотвратить развитие необратимого поражения дыхательных путей. В клинической практике применяются следующие ИГКС: беклометазона дипропионат (БДП), будесонид, флютиказона пропионат, мометазона фуроат и циклесонид.
Отдельной строкой необходимо выделить, что в лечении среднетяжелой и тяжелой БА наиболее эффективной и перспективной является комбинация ИГКС и длительно действующего β2-агониста (ДДБА) [12–14]. В настоящее время в клинической практике применяются следующие фиксированные комбинации ИГКС+ДДБА: салметерол+флутиказон, формотерол+будесонид, формотерол+беклометазон. По результатам ряда исследований показано, что комбинация ДДБА+ИГКС эффективнее увеличенных доз ИГКС, быстрее позволяет достигнуть контроля над симптомами БА, и при использовании комбинированного препарата отмечается снижение количества обострений. Так, исследование GOAL [16] продемонстрировало преимущества комбинированной терапии ИГКС+ДДБА в достижении контроля над симптомами заболевания при среднетяжелой и тяжелой БА по сравнению с монотерапией ИГКС. В авторитетном исследовании N. Barnes et al. было показано, что при персистирующей БА терапия с использованием комбинации флутиказон/салметерол оказалась более эффективной по сравнению с монотерапией флутиказоном [17]. В метаанализе, включившем более 20 тыс. пациентов с персистирующей БА, применение комбинированного препарата салметерол/флутиказон сопровождалось снижением риска обострений заболевания, риска госпитализаций по сравнению с монотерапией ИГКС [18].
Таким образом, в целом ряде клинических исследований было доказано, что добавление ДДБА к низким и средним дозам ИГКС обеспечивает лучший клинический эффект, чем увеличение дозы ИГКС, что в конечном итоге легло в основу современной стратегии ведения больных с БА [12–14].
Очевидно, что большим преимуществом фиксированных комбинаций является не только их высокая эффективность в достижении контроля над симптомами БА, но и хорошая комплаентность за счет соединения 2-х лекарственных средств в одном ингаляторе. Стоит отметить, что представленные на российском фармацевтическом рынке оригинальные комбинированные препараты обладают достаточно высокой стоимостью, но появление в настоящее время дженерических форм, безусловно, расширяет возможности их применения в реальной клинической практике.
Так, в начале 2015 г. в России зарегистрирован препарат Сальмекорт – фиксированная комбинация салметерол+флутиказон в форме дозированного аэрозольного ингалятора (ДАИ) в дозировках 25/50, 25/125 и 25/250 мкг. Клиническая эффективность и безопасность Сальмекорта в сравнении с оригинальным препаратом в форме аэрозоля для ДАИ изучались в рамках клинического исследования, включившего 107 больных с персистирующей БА и нуждающихся в комбинированной терапии высокими дозами ИГКС+ДДБА [19, 20]. Препараты применялись в дозе 25/250 мкг по 2 ингаляции 2 р./сут, продолжительность наблюдения за больными составила 12 нед. В группу больных, получавших Сальмекорт, вошли 56 пациентов, группу сравнения (оригинальный препарат) составил 51 больной с БА. В ходе исследования Сальмекорт продемонстрировал сравнимые с оригинальным препаратом эффективность и безопасность. Так, количество пациентов с положительным ответом на лечение по данным спирометрии составило 35 (64,81%) в группе Сальмекорта и 25 (49,02%) – в группе больных, получавших оригинальный препарат (табл. 3).
При анализе контроля над симптомами БА с использованием опросника АСТ – теста по контролю над астмой (Asthma Control Test) в обеих группах был отмечен значимый прирост показателей на фоне лечения, при этом количество пациентов с приростом оценки как минимум на 1 балл составило 45 в группе Сальмекорта и 40 – в группе сравнения (табл. 4).
В ходе исследования пациенты указывали на уменьшение общего количества приступов БА. При сравнительном анализе оказалось, что статистически значимое уменьшение общего количества приступов астмы наблюдалось в группе больных, получавших Сальмекорт. Анализ частоты развития нежелательных явлений не выявил статистически значимой разницы между группами. Нежелательные явления были зарегистрированы у 9 (16,1%) пациентов, получавших Сальмекорт, и у 3 больных (5,88%) в группе сравнения.
Таким образом, практические врачи располагает теперь более широкими возможностями для базисной терапии БА.
Возвращаясь к принципам терапии, необходимо отметить, что системные глюкокортикостероиды не рекомендуются для поддерживающей терапии БА из-за развития побочных эффектов. Эти препараты применяются для лечения тяжелых обострений БА. Теофиллины длительного действия могут быть использованы в качестве препаратов второй линии у пациентов с персистирующей БА. Анти-IgE-препараты – новый класс лекарственных средств, используемых в настоящее время для улучшения контроля над тяжелой персистирующей атопической БА. В числе наиболее изученных препаратов стоит упомянуть омализумаб. Его применение наиболее оправданно у больных с высоким сывороточным уровнем IgE, нуждающихся в повторных госпитализациях, экстренной медицинской помощи, применяющих высокие дозы ингаляционных и/или системных глюкокортикостероидов.
Для достижения контроля над симптомами БА рекомендован принцип ступенчатой терапии [12]. Каждая ступень включает варианты лечения, которые могут служить альтернативой при выборе поддерживающей терапии БА. У большинства больных с симптомами персистирующей БА, не получавших терапии, следует начинать лечение со ступени 2. Если симптомы БА при первичном осмотре указывают на отсутствие контроля (табл. 5), то лечение необходимо начинать со ступени 3. Если лечение неэффективно или ответ на него недостаточен, проверьте технику ингаляции, соблюдение назначений, уточните диагноз и оцените сопутствующие заболевания. При принятии решения, дозу какого препарата снижать первой и с какой скоростью, должны быть приняты во внимание тяжесть астмы, побочные эффекты лечения, продолжительность приема текущей дозы, достигнутый положительный эффект и предпочтения пациента. Снижение дозы ингаляционных стероидов должно быть медленным в связи с возможностью развития обострения. При достаточном контроле возможно снижение дозы каждые 3 мес., примерно от 25 до 50%.
Литература
1. Глобальная стратегия лечения и профилактики бронхиальной астмы. Global initiative for asthma. Пересмотр 2006 г. / под ред. А.Г. Чучалина. М.: Атмосфера, 2007. 104 с.
2. Емельянов А.В., Черняк Б.А., Княжеская Н.П., Потапова М.О., Белевский А.С. Бронхиальная астма. Респираторная медицина / под ред. А.Г. Чучалина. М.: ГЭОТАР-Медиа, 2007. Т. 1. С. 665–692.
3. Asthma in America. Доступно на: www.asthmain-america.com.
4. Asthma insights reality in Europe. Доступно на: www.asthmaineurope.com.
5. Global Atlas of Asthma Published by the European Academy of Allergy and Clinical Immunology 2013. Available from: https:// www.eaaci.org.
6. Лещенко И.В. Бронхиальная астма: распространенность, диагностика, лечение и профилактика – региональная программа в Свердловской области: Автореф. дисс. … докт. мед. наук. М., 1999.
7. Чучалин А.Г. Тяжелая бронхиальная астма // Русский медицинский журнал. 2000. Т. 8. № 12. https://www.rmj.ru/articles_1636.htm.
8. Социально-экономическое бремя бронхиальной астмы и хронической обструктивной болезни легких в Российской Федерации. Cводный отчет. М., 2009.
9. Accordini S., Bugiani M., Arossa W. et al. Poor control increases the economic cost of asthma. A multicentre populationbased study // Int Arch Allergy Immunol. 2006. Vol. 141. Р. 189–198.
10. Briggs A., Bousquet J., Wallace M., et al. Cost-effectiveness of asthma control: an economic appraisal of the GOAL study // Allergy. 2006. Vol. 61. Р. 531–536.
11. Sullivan S., Rasouliyan L., Russo P., et al. Extent, patterns, and burden of uncontrolled disease in severe or difficult-totreat asthma // Allergy. 2007. Vol. 62. Р. 126–133.
12. Чучалин А.Г., Айсанов З.Р., Белевский А.С. и др. Федеральные клинические рекомендации по диагностике и лечению бронхиальной астмы // Пульмонология. 2014. № 2. С. 11–32.
13. British Thoracic Society. Diagnosis and management of asthma in preschoolers, children and adults. Guideline update 2012 // Can Respir J. 2012. Vol. 19. № 2. Р. 127–164.
14. Global Initiative for Asthma 2014 (GINA) https:// www.ginasthma.com (last accessed 2014).
15. Bateman E., Reddel H., Erikson G. et al. Overall asthma control and future risk // J Allergy Clin. Immunol. 2010. Vol. 125 (3). Р. 600–608.
16. Bateman E., Boushey H., Bousquet J., Busse W., Clark T., Pauwels R., Pedersen S.; GOAL Investigators Group. Can guideline-defined asthma control be achieved? The Gaining Optimal Asthma ControL study // Am J Respir Respir Crit Care Med. 2004. Vol. 170. Р. 836–844.
17. Barnes N., Jacques L., Goldfrad C., Bateman E.D. Initiation of maintenance treatment with salmeterol/fluticasone propionate 50/100 g bd versus fluticasone propionate 100 g bd alone in patients with persistent asthma: Integrated analysis of four randomised trials // Respiratory Medicine. 2007. Vol. 101. Р. 2358–2365.
18. Bateman E., Nelson H., Bousquet J., Kral K., Sutton L., Ortega H., Yancey S. Metaanalysis: Effects of Adding Salmeterol to Inhaled Corticosteroids on Serious Asthma-Related Events // Ann Intern Med. 2008. Vol. 149. Р. 33–42.
19. Княжеская Н.П., Осипова Г.Л. Новый препарат Сальмекорт в базисной терапии бронхиальной астмы // Русский медицинский журнал. 2015. № 4. С. 3–6.
20. Отчет клинического исследования. Протокол: GL-SF/2012-1. Исследуемый препарат Сальмекорт (25/250 мкг) в форме аэрозоля для ингаляций дозированного.
Источник

