Сколько эозинофилов при астме

Эозинофильная астма: симптомы, диагностика и лечение
Что такое эозинофильная астма?
Эозинофилы являются частью иммунной системы и помогают организму бороться с инфекцией. Однако при высоком содержании (более 300 клеток/мкл) эозинофилы провоцируют воспаления в дыхательных путях.
По мере повышения уровня эозинофилов воспаления и другие симптомы астмы становятся более серьезными. По статистическим данным, среди всех пациентов с тяжелой бронхиальной астмой более 55% всех случаев характеризуются эозинофильным типом заболевания.
Типичные симптомы эозинофильной астмы выражаются в хроническом воспалении бронхов и ограничении свободного дыхания, возникают патологии верхних дыхательных путей – постоянный насморк, полипы в носу, пониженная чувствительность к запахам.
У больных наблюдается частые приступы астмы и общий неблагоприятный прогноз течения заболевания при отсутствии адекватного врачебного контроля.Эозинофильная бронхиальная астма чаще всего развивается с так называемым поздним дебютом — то есть у людей старше 18 лет.
Как определить эозинофильную астму:
Существуют критерии для определения эозинофильной бронхиальной астмы. Они делятся на 2 группы – большие и малые.
Большие критерии:
Диагноз – бронхиальная астма.
Частые приступы астмы.
Зависимость от применения стероидных препаратов для контроля бронхиальной астмы.
Хроническое повышенное содержание эозинофилов в крови – более 300 клеток/мкл.
Малые критерии:
Хронический насморк. Полипы в носу.
Затрудненность дыхания. Плохая проходимость бронхов.
Слизистые пробки, воздушные ловушки в легких.
Позднее начало развития бронхиальной астмы.
Когда обратиться к врачу.
При обнаружении у себя 1-2 симптомов указанных выше необходимо срочно обратиться к врачу для точной диагностики.
Важное значение имеет быстрое определение и последовательное лечение эозинофильной астмы. Хроническое воспаление дыхательных путей приводит к переходу болезни в тяжелую форму с плохо контролируемой формой течения.
Лечение
Целью лечения эозинофильной бронхиальной астмы является контроль течения заболевания. В качестве начального средства применяются ингаляционные глюкокортикостероиды (ИГКС). Они эффективно работают, так как эозинофилы являются стероидо-чувствительными клетками.
В случае если при средних и высоких дозах ИГКС не достигается должный контроль заболевания, к терапии добавляются бета-агонисты, антилейкотриеновые препараты и теофиллины медленного высвобождения.
При недостаточности комбинированного лечения применяются системные кортикостероиды в минимально возможных дозах. Так-же при эозинофильной бронхиальной астме используются современные биологические препараты моноклональных антител, которые недавно были одобрены для клинического применения в России.
Для контроля лечения эозинофильной астмы нужно использовать специальные опросники, которые позволяют врачу оценивать степень контроля при подобранном лечении и прогнозировать будущие риски развития заболевания. Крайне важно контролировать уровень эозинофилов в крови или мокроте – в случае повышения уровня эозинофилов в 2 раза при отсутствии увеличения доз ингаляционных кортикостероидов – риск приступа астмы увеличивается до 80-90% .
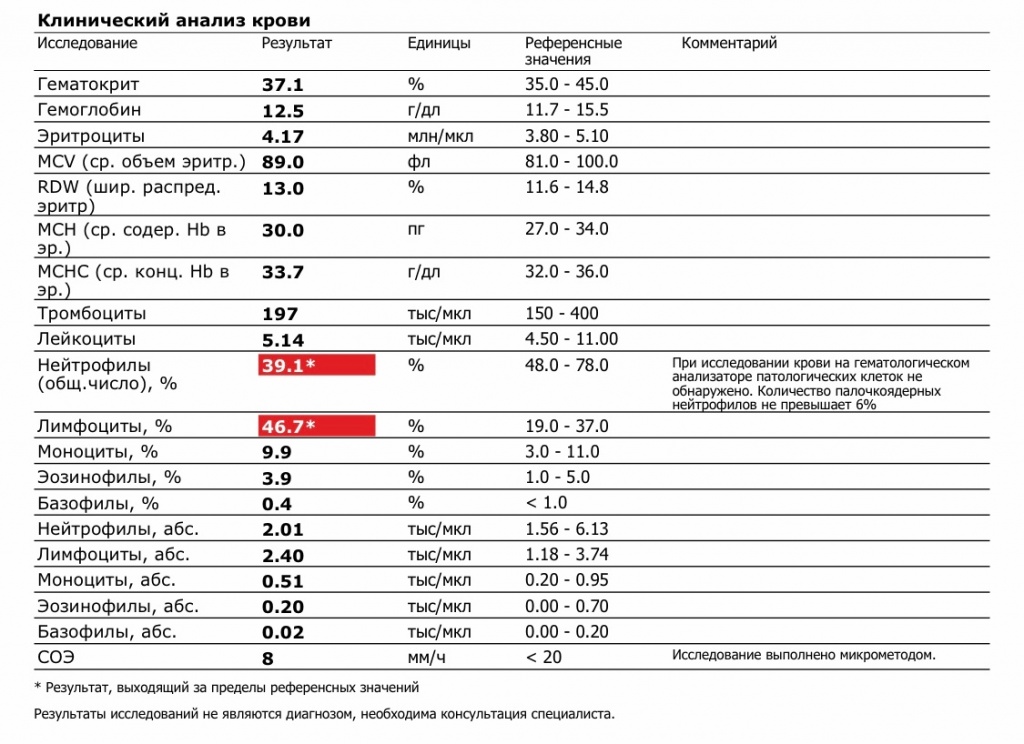
Доза ИГКС должна быть увеличена, если эозинофилов в крови больше 0.3%.
Доза ИГКС остаётся на прежнем уровне, если эозинофилов от 0.1 до 0.3%.
Доза ИГКС должна быть уменьшена при уровне эозинофилов менее 0.1%.
Выводы
Эозинофильная астма требует особого внимания в связи с воспалительными эффектами в дыхательных путях, которые без должной терапии ведут к осложнениям и сопутствующим болезням, существенно ухудшающим качество жизни.
Эозинофильная астма это более 50% всех случаев тяжелой бронхиальной астмы. Именно поэтому она требует особого контроля со стороны самого больного и лечащего его врача. Современные препараты и методы лечения позволяют успешно контролировать течение болезни при условии соблюдения дисциплины со стороны пациента, контроля и правильно подобранной лечащим врачом терапии.
Основные шаги к контролю эозинофильной бронхиальной астмы:
Выбор квалифицированного специалиста практикующего современные методы лечения бронхиальной астмы
Своевременная диагностика эозинофильного типа астмы по критериям приведённым выше.
Дисциплина в принятии лекарств и их дозировок.
Ведение опросников и регулярный контроль уровня эозинофилов в крови
Соблюдение общих рекомендаций для профилактики бронхиальной астмы.
Важно помнить, что бронхиальная астма в ее эозинофильной форме – это очень опасное заболевание с высокими рисками. К счастью, современная терапия позволяет успешно ее контролировать с помощью стероидных препаратов, а недавно разработанные биологические препараты позволяют снизить дозы стероидов без потери контроля заболевания.
Несмотря на это очень важно помнить — несоблюдение правил, дисциплины лечения и предписаний врача в конечном итоге может привести к потере контроля над заболеванием и далее к астматическому статусу – состоянию потенциально угрожающему вашей жизни.
Будьте здоровы и помните — лечение эозинофильной бронхиальной астмы должно проходить ТОЛЬКО под наблюдением высококвалифицированного врача!
Источник
В разных странах мира бронхиальная астма (БА) занимает лидирующие позиции среди аллергических заболеваний органов дыхания, как среди взрослого населения, так и у детей. При данной патологии наблюдается развитие синдрома гиперчувствительности и гиперреактивности на аллергены и неспецифические агенты, ирританты. Хроническое воспаление обуславливает возникновение повторяющихся приступов обструкции бронхов, обратимых спонтанно либо в результате лечения.
В результате различных исследований становится понятным, что существуют различные фенотипы бронхиальной астмы, имеющие определенные клинические и биологические характеристики. Актуальность выделения определенных фенотипов этого заболевания объясняется тем, что именно эти данные должны являться основой для лечения и разработки индивидуальных схем терапии.
Фенотипирование бронхиальной астмы основывается на выявлении доминирующего подтипа воспаления и биологических маркеров, которые присутствуют либо в моноварианте, либо дополняют друг друга. С атопической формой бронхиальной астмы связывают эозинофильный фенотип, при котором наблюдается эозинофильная клеточная инфильтрация. В основе патогенеза при этом лежит активация эозинофилов в очаге воспаления и выброс агрессивных медиаторов, которые являются биологическими маркерами данного воспалительного процесса.
Известно, что уровень эозинофилов в крови при аллергии увеличивается до 10-20%, что получило название «эозинофилия». В гранулах эозинофилов содержатся белки, основными являются цитотоксин и нейроцитотоксин. Эти белки способны повреждать собственные клетки организма. В результате активации эозинофилов из гранул высвобождаются медиаторы аллергических реакций, а также цитокины: ИЛ-4, ИЛ-5, ИЛ-10, ИЛ-12, ИЛ-13, ГМ-КСФ и ФНОα.
Помимо этого эти клетки несут на своей поверхности рецепторы для С4, С3, С3b компонентов комплемента, а также для Fc-фрагментов IgG, IgE. CD23 является низкоаффинным рецептором для IgE. Большая часть IgE связана с рецепторами, несвязанная — циркулирует в сыворотке крови, где и определяют уровень общего IgE. Экспрессия рецепторов на клетках, как и концентрация иммуноглобулинов в крови при аллергическом процессе меняется. Взаимоотношение «Fc-рецептор-иммуноглобулин» определяет их уровень в крови и на клетках, и от этого зависит развитие патологического процесса.
Несмотря на имеющиеся в литературе данные, четких клинических и иммунологических критериев определенных фенотипов не разработано, что является необходимым для дифференцированного подхода к выбору терапии и профилактики бронхиальной астмы. Цель работы — характеристика эозинофильного фенотипа бронхиальной астмы у детей.
Показатели эозинофилов в крови
В обследование включено 160 детей в возрасте от 5 до 18 лет. 130 пациентов наблюдались по поводу атопической бронхиальной астмы. Диагноз установлен на основании международных рекомендаций, подтвержден данными анамнеза, клинической картиной заболевания, результатами аллергологических и инструментальных исследований. Контрольную группу составили 30 здоровых детей обоих полов 5-18 лет, не имеющих аллергических заболеваний. В ходе работы определяли следующие показатели: относительный и абсолютный уровень эозинофилов, уровень эозинофилов, несущих FcεRI+ и CD23+IgE+ рецепторы, уровень общего IgE.
Фенотипирование клеток проводили на проточном цитометре Cytomics FC 500 (Beckman Coulter Inc., США) с использованием моноклональных антител производства ОДО «НИКП РЕСАН», Беларусь. Для лизиса эритроцитов использовали лизирующий раствор OptiLyse С.

У детей с бронхиальной астмой, имеющих высокий уровень эозинофилов, изучали анамнез жизни и заболевания, наследственность, особенности клинической картины бронхиальной астмы, оценивали результаты аллергологического исследования. Аллергологическое обследование включало проведение кожных скарификационных проб (КСП), а также определение специфических IgE-антител в сыворотке крови к бытовым (клещ постельный Dermatophagoides pteronyssinus) и эпидермальным (шерсть кошки, шерсть собаки) аллергенам.
Статистическую обработку данных проводили с использованием стандартного пакета прикладных программ «Statistica 6.0». Критерий Шапиро-Уилка применяли для принятия решения о виде распределения количественного признака. Для описания признака распределение, которого отличается от нормального использовали медиану и интерквартильный интервал. Использовались непараметрические методы статистического исследования: критерий Манна-Уитни (для анализа различий в двух независимых группах по количественному признаку). Различия считали достоверными при р<0,05.
Уровень эозинофилов крови
В норме абсолютный уровень эозинофилов в периферической крови составляет 0,055-0,550×109 (55,0-550,0 кл/мкл), относительное содержание — 1-5%. Относительный уровень эозинофилов у детей обследуемой группы составил 6% [3,0; 8,0%], абсолютный показатель — 417,0 кл/мкл [232,0; 636,0 кл/мкл], что достоверно выше уровня детей контрольной группы, где относительный уровень равен 2,5% [1,0; 3,0%], абсолютное значение — 166,5 кл/мкл [86,0; 213,0 л/мкл] (р<0,001).
При определении уровня эозинофилов, несущих FcεRI+ рецептор, который является высокоаффинным рецептором для IgE, показатель составил 420,0 кл/мкл [250,0; 660,0 кл/мкл], что достоверно выше уровня контрольной группы, где этот показатель равен 200,0 кл/мкл [140,0; 240,0 кл/мкл] (р<0,001).
Уровень, превышающий референтные значения (<440,0 кл/мкл), установлен у 61 (46,92%) пациентов с бронхиальной астмой. В этой группе детей этот показатель равен 660,0 кл/мкл [580,0; 840,0 кл/мкл]. У 58 пациентов высокий уровень эозинофилов сочетался с высоким уровнем эозинофилов, несущих FcεRI+ рецептор.
Количество эозинофилов, несущих на своей поверхности CD23+IgE+ рецептор, составило 62,2% [35,4; 76,6%], абсолютный показатель равен 223,371 кл/мкл [105,30; 375,24 кл/мкл]. Полученные результаты достоверно выше показателей детей контрольной группы, где относительный уровень равен 25,45% [14,30; 30,60%] (р<0,001), а абсолютный — 30,88 кл/мкл [25,63; 42,84 кл/мкл] (р<0,0001) (таблица 1).

Относительный уровень эозинофилов, несущих CD23+IgE+ рецептор, превышал референтные значения (<40%) у 92 (70,77%) детей, в этой группе относительный показатель равен 70,6% [58,25; 80,30%], абсолютный уровень составил 289,80 кл/мкл [172,36; 405,31 кл/мкл]. При этом 56 детей с эозинофилией имели высокий уровень этого показателя.
У детей с бронхиальной астмой определяли уровень общего IgE в сыворотке крови, как маркер аллергического процесса. Этот показатель составил 430,0 МЕ/мл [220,0; 760,0 МЕ/мл]. У 14 (10,77%) пациентов установлен уровень общего IgE менее 100 МЕ/мл. При сопоставлении показателей, изучаемых в ходе работы, установлены корреляционные взаимоотношения между уровнем общего IgE и абсолютным уровнем эозинофилов (r=+0,367; p<0,01), соответственно уровень общего IgE коррелировал с уровнем эозинофилов, несущих FcεRI+ рецептор (r=+0,389; p<0,01). Высокий уровень корреляции также установлен между уровнем эозинофилов, несущих FcεRI+ рецептор и абсолютным уровнем эозинофилов, несущих CD23+IgE+ рецептор (r=+0,677; p<0,0001).
В ходе работы эозинофилия выявлена у 71 (54,62%) ребенка с бронхиальной астмой. При изучении семейного анамнеза, установлено, что у детей с эозинофилией в большинстве случаев прослеживается наследственный характер заболевания. 56 (78,87%) детей имели близких родственников, страдающих аллергическими заболеваниями. Наибольший процент приходился на долю бронхиальной астмы — 24 (33,80%) и атопического дерматита — 17 (23,94%).
Первые проявления аллергии наблюдались у 45 (63,38%) детей на первом году жизни. Чаще всего в клинической картине выявлялись кожные проявления непереносимости пищевых продуктов, причем у 19 (26,76%) пациентов кожные высыпания появились в возрасте до трех месяцев, у 12 (16,90%) — в возрасте до полугода, 14 (19,72%) пациентов отметили появление первых кожных проявлений после 6 месяцев. У большинства детей наблюдалась сыпь в области щек, за ушами, на ягодицах и голенях. Родители отмечали, что сыпь сопровождалась выраженным зудом.

У 43 (60,56%) детей с бронхиальной астмой, имеющих повышенный уровень эозинофилов в общем анализе крови, выявлена сопутствующая патология аллергической природы. Наиболее часто у пациентов наблюдался аллергический ринит, эта патология установлена у 21 (29,58%) ребенка. 9 (12,68%) детей имели атопический дерматит, у 3 (4,23%) детей в анамнезе была лекарственная аллергия, 1 (1,41%) ребенок страдал хронической крапивницей.
Наиболее часто первые эпизоды бронхообструкции у детей с бронхиальной астмой с эозинофилией наблюдались в возрасте двух-трех лет. Это было характерно для 41 (57,75%) ребенка. Однако у 8 (11,27%) детей первые эпизоды бронхообструкции наблюдались уже на первом году жизни. Для 17 (23,94%) пациентов впервые бронхообструктивный синдром наблюдался в возрасте 4-6 лет. В школьном возрасте, после 6 лет, впервые одышка наблюдалась только у 9 (12,68%) пациентов. Учитывая данные анамнеза, диагноз бронхиальная астма в возрасте до 3-х лет установлен у 45 (63,38%) детей, у 26 (36,62%) пациентов диагноз установлен в преддошкольном или школьном возрасте.
Для купирования бронхообструкции 62 (87,32%) ребенка использовали β2-агонисты короткого действия, применение которых позволяло быстро улучшить состояние пациентов и устранить явления обструкции. В качестве базисной терапии для пациентов с бронхиальной астмой с эозинофилией наилучший терапевтический эффект наблюдался после применения ингаляционных глюкокортикостероидов. Эти лекарственные средства в качестве базисной терапии использовали 66 (92,96%) детей.

При проведении аллергологического обследования у детей с эозинофилией наблюдались следующие особенности. Положительные кожные пробы к Dermatophagoides pteronyssinus выявлены у 49 (69,01%) детей: реакцию на ++++ и +++ имели 15 ребенка, на ++ — 22, и на + — 12. Сенсибилизация к аллергену шерсть кошки по результатам кожных проб выявлялась у 23 (32,39%) детей: сенсибилизацию на ++++ и +++ имели 10 детей, на ++ – 8, и на +- 5. Положительные результаты к аллергену шерсть собаки наблюдались у 14 (19,72%) детей, результаты распределились следующим образом: ++++ и +++ — у 5 детей, ++ — у 6 пациентов, + — у 3 детей. Одновременно к двум аллергенам сенсибилизация установлена у 18 детей, у 9 пациентов — к трем аллергенам.
При определении уровня IgE-антител к Dermatophagoides pteronyssinus у 67 (94,37%) пациентов с эозинофилией установлен показатель выше референтных значений (<0,35 МЕ/мл), составил 28,54 МЕ/мл [7,93; 47,54 МЕ/мл]. У 58 (81,69%) детей установлен высокий уровень IgE-антител к аллергену шерсть кошки, составил 3,41 МЕ/мл [0,70; 16,06 МЕ/мл]. К аллергену шерсть собаки этот показатель находился на уровне 0,69 МЕ/мл [0,38; 2,04 МЕ/мл], высокий уровень установлен у 39 (54,93%) детей.
Все дети, имеющие положительные результаты КСП, имели высокий уровень IgE-антител к этому аллергену в сыворотке крови, однако в ряде случаев IgE-антитела в сыворотке крови выявлялись, при этом результаты КСП были отрицательными. Полученные результаты свидетельствуют о более высокой информативности лабораторных тестов, что может быть обусловлено низкой чувствительностью кожных покровов в детском возрасте.
Эозинофильный фенотип бронхиальной астмы
Для пациентов с бронхиальной астмой, имеющих определенный фенотип характерно наличие общих клинических и биологических признаков заболевания, формирование которых происходит на основе генотипа пациента с участием факторов окружающей среды. С целью выявления клинического фенотипа бронхиальной астмы оценивают клинические и анамнестические характеристики, которые позволяют распределить пациентов по подгруппам (фенотипировать). Основные характеристики и сопутствующие состояния, которые учитываются при разделении на клинические фенотипы, включают определение времени дебюта заболевания, возрастных особенностей, наличие или отсутствие атопии и т.д.
В ходе нашего исследования при изучении анамнеза и клинической картины заболевания установлено, что у детей с эозинофилией в большинстве случаев наблюдается наследственный характер заболевания, появление первых проявлений аллергии уже на первом году жизни, у 60,56% детей этой группы установлена сопутствующая аллергопатология. Диагноз бронхиальной астмы у большинства пациентов с эозинофилией установлен в возрасте до трех лет. Оптимальный эффект при лечении пациентов этой группы получен при назначении в качестве базисной терапии ингаляционных глюкокортикостероидов, а также β2-агонистов короткого действия для купирования эпизодов бронхообструкции.
В тоже время клиническое фенотипирование не предусматривает описание этиологических и патофизиологических механизмов и их взаимосвязей. С точки зрения патогенеза бронхиальной астмы следует изучать эндотипы заболевания, которые лежат в основе формирования определенного клинического фенотипа. В основе биологического эндотипирования лежит выявление доминирующего подтипа воспаления и его биологических маркеров (индикаторах), которые присутствуют либо в моноварианте, либо дополняют друг друга.

У детей с атопической бронхиальной астмой при выявлении эозинофильного фенотипа наблюдались следующие особенности аллергоиммунологического обследования. У большинства пациентов этой группы в сыворотке крови выявляется повышенный уровень IgE антител к бытовым и эпидермальным аллергенам, а также наблюдаются положительные кожные скарификационные пробы с этими аллергенами.
При иммунологическом обследование у пациентов с эозинофильным фенотипом установлено статистически значимое увеличение количества эозинофилов, несущих несущих FcεRI+ рецептор, а также эозинофилов, экспрессирующих CD23+IgE+ рецептор, а также установлена корреляция между этими показателями (r=+0,677; p<0,0001). Так, в группе детей с эозинофилией 58 (81,69%) пациентов имели высокий уровень эозинофилов, несущих FcεRI+ рецептор, и 56 (78,87%) детей — высокий уровень эозинофилов, несущих CD23+IgE+ рецептор.
Таким образом, дальнейшее изучение взаимосвязей между клинической картиной и результатами аллергологических и иммунологических исследований, изучение взаимосвязи фенотипа и механизма развития заболевания поможет провести более четкое выделение подгрупп с общими характеристиками и будет способствовать правильному подбору лекарственных средств в зависимости от варианта течения бронхиальной астмы.
Выводы
- У детей с атопической бронхиальной астмой относительное и абсолютное содержание эозинофилов, а также эозинофилов несущих FcεRI+ и CD23+IgE+ рецепторы, статистически значимо выше, чем в контрольной группе. В группе детей с эозинофилией 58 (81,69%) пациентов имели высокий уровень эозинофилов, несущих FcεRI+ рецептор, и 56 (78,87%) детей — высокий уровень эозинофилов, несущих CD23+IgE+ рецептор.
- В группе детей с бронхиальной астмой установлена корреляция между уровнем общего IgE и уровнем эозинофилов, несущих FcεRI+ (r=+0,389; p<0,01) и CD23+IgE+ рецепторы (r=+0,677; p<0,0001).
- У детей с эозинофилией в большинстве случаев наблюдается наследственный характер заболевания, первые проявления аллергии присутствуют уже на первом году жизни, установлена сопутствующая аллергопатология.
- У большинства пациентов с бронхиальной астмой, имеющих эозинофилию, в сыворотке крови выявляется повышенный уровень IgE антител к бытовым и эпидермальным аллергенам, а также наблюдаются положительные кожные скарификационные пробы с этими аллергенами.
- Оптимальный эффект при лечении пациентов с эозинофилией получен при назначении, в качестве базисной терапии, ингаляционных глюкокортикостероидов, а также β2-агонистов короткого действия для купирования эпизодов бронхообструкции.
© Е.Г. Асирян, Н.Д. Титова
Источник


