Тяжелая астма клиника диагностика
Общие сведения
Тяжёлое обострение астмы (ТОА) — это приступ бронхиальной астмы (БА), отличающийся необычной тяжестью и резистентностью к стандартной или повседневной бронхорасширяющей терапии, который при отсутствии адекватной помощи может закончиться смертельным исходом.
Помимо необычной тяжести и резистентности к бронхоспазмолитикам, для такого приступа характерны неэффективный, непродуктивный кашель, практически не сопровождающийся отделением мокроты, и быстро нарастающая острая дыхательная недостаточность, сопровождающаяся неуклонным усилением одышки и цианоза.
Ещё несколько лет назад тяжёлые приступы БА, резистентные к бронхоспазмолитикам, именовались астматическим статусом (АС).
Многие авторы и в настоящее время выделяют из ТОА астматический статус, считая термин тяжёлое обострение астмы более широким понятием по сравнению с АС. К АС эти авторы относят лишь те случаи ТОА, при которых ингаляционное применение высоких доз а2-агонистов быстрого действия не приводит к заметному улучшению состояния.
Именно такое представление о ТОА приводится в международном документе по бронхиальной астме — ДЖИНА-2002. Согласно рекомендациям международных экспертов, к тяжёлому обострению астмы относят лишь такие случаи тяжёлых приступов астмы, когда после 3-х кратного через каждые 20 минут ингаляционного применения а2-агониста быстрого действия в больших дозах (в том числе через небулайзер) у больного не наступает улучшения, а пиковая скорость выдоха (ПСВ) составляет
Таким образом, термины АС и ТОА в интерпретации ДЖИНА-2002 можно считать равнозначными. С учётом последних рекомендаций Международного консенсуса по БА и Всероссийского научного общества пульмонологов, мы будем пользоваться термином ТОА.
Тяжёлое обострение астмы развивается примерно у 30% больных бронхиальной астмой, которой в нашей стране страдает около 7 млн человек. Летальность при этом наиболее тяжёлом осложнении БА, по данным различных авторов, составляет от 1 до 10%. Развитие ТОА и летальность при ней не являются неизбежными: в подавляющем большинстве случаев их можно было предотвратить.
Различают две формы ТОА. В одних случаях прогрессирующее ухудшение состояния пациента и нарастание дыхательной недостаточности, несмотря на увеличение кратности приёма бронхолитиков (чаще а2-агонистов), наблюдается в течение нескольких дней, после чего больной поступает в стационар.
Такую форму называют тяжёлое обострение астмы с медленным темпом развития. В более редких случаях (примерно в 10-15 раз реже) наблюдается быстрое и молниеносное развитие заболевания. Остановка дыхания и смертельный исход могут наступить уже в первые 1-3 часа от появления первых симптомов (иногда в первые 5-10 минут), до поступления больного в стационар и даже — до прибытия врача скорой медицинской помощи. Такую форму называют ТОА с внезапным началом.
Разберём вначале ТОА с медленным темпом развития.
Этиология и патогенез
Довольно частыми причинами тяжёлого обострения астмы с медленным темпом развития являются инфекции трахеобронхиального дерева (бактериальные и особенно вирусные) и различные дефекты лечения.
К дефектам лечения относятся:
1) внезапная отмена или необоснованное снижение дозировки глюкокортикостероидов (ГКС) у гормонально-зависимых больных (или просто сохранение прежней дозы при развитии пневмонии и других тяжёлых заболеваний, когда требуется повышение дозировки);
2) применение седативных (седуксен и другие транквилизаторы) препаратов, угнетающих дыхательный центр и затрудняющих вентиляцию, а также противогистаминных средств, «подсушивающих» слизистую оболочку бронхов и затрудняющих отделение мокроты, что способствует формированию бронхообструктивного синдрома;
3) приём нестероидных противовоспалительных средств при «аспириновой» астме (при этом может развиться не только ТОА с медленным темпом развития, но и ТОА с внезапным началом) или препаратов, которые вообще противопоказаны при бронхиальной астме (например, а2-адреноблокаторов).
Однако наиболее частой причиной развития тяжёлого обострения астмы является неадекватное тяжести заболевания лечение пациента, недостаточное использование базисных препаратов, прежде всего ингаляционных ГКС. Развитие ТОА с медленным темпом развития можно считать следствием прогрессирования бронхиальной астмы из-за утраты контроля за течением заболевания, а нередко и в связи с явными дефектами лечения. Поэтому в подавляющем большинстве случаев развитие ТОА следует рассматривать как неудачу лечащего врача и должно служить основанием для пересмотра им своих представлений о лечении бронхиальной астмы.
Нередко причиной тяжёлого обострения астмы является плохая информированность больного о методах контроля своего состояния и оценки эффективности лечения, о принимаемых препаратах и их побочных действиях. Недостаточное обучение больного является также недоработкой лечащего врача.
К числу основных дефектов лечения, приводящих к развитию ТОА, ещё недавно относили чрезмерное применение а2-агонистов. Считалось, что в этих условиях в организме накапливаются продукты распада а2-агонистов, которые вызывают рикошетную бронхоконстрикцию и отёк слизистой оболочки бронхов (синдром «запирания легкого»). В настоящее время объяснять развитие ТОА с позиций передозировки а2-агонистов считается неправомочным.
Частое применение ингаляционных а2-агонистов в этих условиях не является непосредственной причиной бронхообструкции (она прогрессирует в основном по своим механизмам): в используемых дозировках и при несоответствующей технике ингаляции оно оказывается просто неэффективным. Вместе с тем злоупотребление а2-агонистами всё же вносит свою лепту в генез бронхообструкции.
Оно оказывает повреждающее действие на слизистую оболочку бронхов за счёт газа фреона, используемого в дозируемых ингаляторах, и в связи с этим затрудняет отделение мокроты, а также снижает чувствительность а2-рецепторов бронхов к а2-агонистам. Поэтому избыточное употребление ингаляционных а2-агонистов быстрого действия (более одной упаковки сальбутамола или его эквивалента в месяц) остаётся фактором риска развития тяжёлого обострения астмы.
ТОА с медленным темпом развития значительно чаще (примерно в 80-85% случаев) развивается у больных с неатопической (эндогенной) формой БА.
Важным звеном патогенеза считается снижение чувствительности к а2-агонистам вследствие десенситизации а2-адренорецепторов. Об этом свидетельствует гиперкатехоламинемия, установленная при ТОА, наличие тахикардии и повышение системного артериального давления, а также положительный бронхолитический эффект лишь на повышенные дозы ингаляционных а2-агонистов.
Наряду с этим, в патогенезе тяжёлого обострения астмы существенную роль играет нарушение бронхиального дренажа и отделения мокроты. При этом если вначале ТОА нарушение бронхиальной проходимости, более ощутимое в мелких бронхах, связано в основном с бронхоспазмом, то в дальнейшем основное значение приобретает скопление в просвете бронхов вязкой мокроты из-за гиперсекреции бронхиальных желез, отёк слизистой оболочки бронхиального дерева и экспираторный коллапс мелких и средних бронхов, который резко увеличивается при ТОА в результате нарастания внутригрудного давления на выдохе.
Особенно большое значение в генезе обструкции имеет гиперпродукция вязкой мокроты, которая буквально перекрывает воздухоносные пути. Это необходимо учитывать при лечении: назначением только бронхолитиков не удается восстановить бронхиальную проходимость.
Прогрессирующая бронхиальная обструкция приводит к нарушению газообмена и кислотно-основного состояния. Развивающиеся гипоксия, гиперкапния и декомпенсированный ацидоз определяют не только клинику и прогноз заболевания, но и являются важнейшими факторами патогенеза.
Наряду с этим увеличение аэродинамического сопротивления является причиной гипервентиляции и чрезмерного возрастания работы дыхательных мышц с последующим их утомлением. Резко выраженные альвеолярная гипоксия и гиперкапния вызывают рефлекторный спазм легочных капилляров; дополнительное значение для развития легочной гипертензии имеет гиперкатехоламинемия. В результате может развиться острое легочное сердце или манифестировать декомпенсация хронического легочного сердца.
К факторам патогенеза тяжёлого обострения астмы относится также нарушение водно-электролитного обмена. Нарастающая гипервентиляция с увеличением работы дыхательной мускулатуры, обильное потоотделение и ограничение приёма жидкости из-за тяжёлого общего состояния приводят к дегидратации с увеличением вязкости мокроты. Уменьшается объём циркулирующей крови (иногда на 20-25%) и объём внеклеточной жидкости, нередко развивается циркуляторная гипотония.
Клиника и диагностика
Исходя из представленных выше данных, критериями диагностики ТОА являются:
1) развитие тяжёлого приступа БА;
2) отсутствие улучшения после 3-х кратного (через каждые 20 минут) ингаляционного применения а2-агонистов в больших дозах;
3) неэффективный, непродуктивный кашель;
4) пиковая скорость выдоха (ПСВ)
5) прогрессирующая острая дыхательная недостаточность.
Клиническая картина ТОА во многом соответствует таковой при тяжёлом приступе БА. У больного имеется удушье с преимущественным затруднением выдоха, как правило, по типу умеренного тахипноэ (т.е. с несколько увеличенной частотой дыхания), цианоз вначале умеренный.
При физикальном обследовании легких определяются: шумное, свистящее дыхание, слышимое на расстоянии, перкуторно-коробочный звук, при аускультации — жёсткое дыхание с удлинённым выдохом, сухие рассеянные, преимущественно свистящие хрипы на выдохе. Классическими признаками тяжёлого обострения астмы являются: вынужденное положение (ортопноэ), профузная потливость, затруднение при разговоре из-за одышки, участие в дыхании вспомогательной мускулатуры шеи, втяжение над- и подключичных промежутков.
Частота дыхания обычно более 25, а частота сердечных сокращений — более 110 в мин. Важное значение для оценки тяжести ТОА и ответа на терапию является определение величины парадоксального пульса (уменьшение пульсовых волн во время вдоха): неблагоприятным признаком является его величина более 12 мм рт.ст. Однако следует иметь в виду, что уменьшение величины парадоксального пульса может быть следствием не только улучшения состояния больного, но и утомления мышц вдоха.
При отсутствии адекватного лечения состояние больного ухудшается. Нарастает цианоз. Дыхание становится поверхностным, иногда аритмичным, частота дыхания увеличивается до 35-40 в мин, экскурсии грудной клетки почти незаметны. Аускультативно количество хрипов в лёгких уменьшается, а на некоторых участках, вначале в нижних отделах, дыхание резко ослаблено и хрипы не выслушиваются (зоны «немого» легкого). В дальнейшем зоны «немого» легкого могут увеличиваться; в наиболее тяжёлых случаях дыхательные шумы сохраняются лишь на ограниченных участках легких, обычно в области верхушек или над областью корней легких.
Возникновение участков «немого» легкого связано в основном с закупоркой бронхов вязкой мокротой и с набухлостью слизистой оболочки бронхов. В этих условиях резко нарушается газообмен, нарастают и достигают критического уровня гипоксемия, гиперкапния и нарушение кислотно-основного состояния (КОС). Это приводит к дальнейшим нарушениям со стороны сердечно-сосудистой системы и изменениям психики. У больных нарастает тахикардия (до 140 в минуту), величина парадоксального пульса, появляются аритмии, артериальное давление снижается вплоть до развития коллапса. У некоторых больных в критическом состоянии развивается брадикардия.
Нарушения со стороны центральной нервной системы вначале проявляются периодическими возбуждениями или, наоборот, апатией и депрессией; контакт с больным может быть затруднён из-за раздражительности больного и амнезии. В дальнейшем появляются формальные расстройства психики: дезориентация во времени и пространстве, развиваются галлюцинации и бредовое состояние, сменяющиеся глубокой заторможенностью и потерей сознания с развитием комы.
Врач должен хорошо ориентироваться в динамике патологического процесса при ТОА, поскольку больной может поступить на любом этапе течения этого тяжелого осложнения.
Для объективной оценки тяжести состояния необходим мониторинг ПСВ иSatO2 (сатурации или насыщения гемоглобина крови кислородом), которая определяется неинвазивно с помощью пульсоксиметра. Снижение ПСВ 2, РаСО2, КОС, включая рН), а при SatO2
Совокупное определение SatO2, РаО2, РаСО2 и КОС позволяет дать точную оценку газообмена больного. При прогрессировании тяжёлого обострения астмы наблюдается следующая последовательная динамика газового состава и КОС крови: умеренное снижение РаО2, гипокапния, дыхательный алкалоз — выраженная гипоксемия (снижение РаО2), гиперкапния, дыхательный (иногда и метаболический) ацидоз.
Между снижением SatO2 и РаО2 наблюдается параллелизм, а при снижении ПСВ 2 составляет около 100 %, РаО2 — более 80 мм рт.ст., РаСО2 — 35-45 мм рт.ст. Гипокапния (РаСО2
Для более глубокой характеристики патологического процесса и оптимизации лечения, помимо ПСВ и газов крови, крайне желательно определять центральное венозное давление,электролиты крови (калий, натрий, магний, фосфор), гематокрит, объём циркулирующей крови и внеклеточной жидкости, следить за динамикой эмиссионной компьютерной томографии (ЭКГ).
При подозрении на пневмонию, ателектаз,пневмоторакс, легочную эмболию, а также во всех случаях, когда пациенты не отвечают на терапию, проводят рентгенографию легких.
Саперов В.Н., Андреева И.И., Мусалимова Г.Г.
Опубликовал Константин Моканов
Источник

Бронхиальная астма – это хроническое неинфекционное заболевание дыхательных путей воспалительного характера. Приступ бронхиальной астмы часто развивается после предвестников и характеризуется коротким резким вдохом и шумным длительным выдохом. Обычно он сопровождается кашлем с вязкой мокротой и громкими свистящими хрипами. Методы диагностики включают оценку данных спирометрии, пикфлоуметрии, аллергопроб, клинических и иммунологических анализов крови. В лечении используются аэрозольные бета-адреномиметики, м-холинолитики, АСИТ, при тяжелых формах заболевания применяются глюкокортикостероиды.
Общие сведения
За последние два десятка лет заболеваемость бронхиальной астмой (БА) выросла, и на сегодняшний день в мире около 300 миллионов астматиков. Это одно из самых распространенных хронических заболеваний, которому подверженные все люди, вне зависимости от пола и возраста. Смертность среди больных бронхиальной астмой достаточно высока. Тот факт, что в последние двадцать лет заболеваемость бронхиальной астмой у детей постоянно растет, делает бронхиальную астму не просто болезнью, а социальной проблемой, на борьбу с которой направляется максимум сил. Несмотря на сложность, бронхиальная астма хорошо поддается лечению, благодаря которому можно добиться стойкой и длительной ремиссии. Постоянный контроль над своим состоянием позволяет пациентам полностью предотвратить наступление приступов удушья, снизить или исключить прием препаратов для купирования приступов, а так же вести активный образ жизни. Это помогает поддержать функции легких и полностью исключить риск осложнений.

Бронхиальная астма
Причины
Наиболее опасными провоцирующими факторами для развития бронхиальной астмы являются экзогенные аллергены, лабораторные тесты на которые подтверждают высокий уровень чувствительности у больных БА и у лиц, которые входят в группу риска. Самыми распространенными аллергенами являются бытовые аллергены – это домашняя и книжная пыль, корм для аквариумных рыбок и перхоть животных, аллергены растительного происхождения и пищевые аллергены, которые еще называют нутритивными. У 20-40% больных бронхиальной астмой выявляется сходная реакция на лекарственные препараты, а у 2% болезнь получена вследствие работы на вредном производстве или же, например, в парфюмерных магазинах.
Инфекционные факторы тоже являются важным звеном в этиопатогенезе бронхиальной астмы, так как микроорганизмы, продукты их жизнедеятельности могут выступать в качестве аллергенов, вызывая сенсибилизацию организма. Кроме того, постоянный контакт с инфекцией поддерживает воспалительный процесс бронхиального дерева в активной фазе, что повышает чувствительность организма к экзогенным аллергенам. Так называемые гаптенные аллергены, то есть аллергены небелковой структуры, попадая в организм человека и связываясь его белками так же провоцируют аллергические приступы и увеличивают вероятность возникновения БА. Такие факторы, как переохлаждение, отягощенная наследственность и стрессовые состояния тоже занимают одно из важных мест в этиологии бронхиальной астмы.
Патогенез
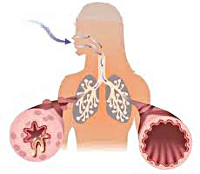
Хронические воспалительные процессы в органах дыхания ведут к их гиперактивности, в результате которой при контакте с аллергенами или раздражителями, мгновенно развивается обструкция бронхов, что ограничивает скорость потока воздуха и вызывает удушье. Приступы удушья наблюдаются с разной периодичностью, но даже в стадии ремиссии воспалительный процесс в дыхательных путях сохраняется. В основе нарушения проходимости потока воздуха, при бронхиальной астме лежат следующие компоненты: обструкция дыхательных путей из-за спазмов гладкой мускулатуры бронхов или вследствие отека их слизистой оболочки; закупорка бронхов секретом подслизистых желез дыхательных путей из-за их гиперфункции; замещение мышечной ткани бронхов на соединительную при длительном течении заболевания, из-за чего возникают склеротические изменения в стенке бронхов.
В основе изменений бронхов лежит сенсибилизация организма, когда при аллергических реакциях немедленного типа, протекающих в виде анафилаксий, вырабатываются антитела, а при повторной встрече с аллергеном происходит мгновенное высвобождение гистамина, что и приводит к отеку слизистой бронхов и к гиперсекреции желез. Иммунокомплексные аллергические реакции и реакции замедленной чувствительности протекают аналогично, но с менее выраженными симптомами. Повышенное количество ионов кальция в крови человека в последнее время тоже рассматривается как предрасполагающий фактор, так как избыток кальция может провоцировать спазмы, в том числе и спазмы мускулатуры бронхов.
При патологоанатомическом исследовании умерших во время приступа удушья отмечается полная или частичная закупорка бронхов вязкой густой слизью и эмфизематозное расширение легких из-за затрудненного выдоха. Микроскопия тканей чаще всего имеет сходную картину – это утолщенный мышечный слой, гипертрофированные бронхиальные железы, инфильтративные стенки бронхов с десквамацией эпителия.
Классификация
БА подразделяется по этиологии, тяжести течения, уровню контроля и другим параметрам. По происхождению выделяют аллергическую (в т. ч. профессиональную БА), неаллергическую (в т. ч. аспириновую БА), неуточненную, смешанную бронхиальную астму. По степени тяжести различают следующие формы БА:
- Интермиттирующая (эпизодическая). Симптомы возникают реже одного раза в неделю, обострения редкие и короткие.
- Персистирующая (постоянного течения). Делится на 3 степени:
- легкая — симптомы возникают от 1 раза в неделю до 1 раза в месяц
- средняя — частота приступов ежедневная
- тяжелая — симптомы сохраняются практически постоянно.
В течении астмы выделяют обострения и ремиссию (нестабильную или стабильную). По возможности контроля над пристпуами БА может быть контролируемой, частично контролируемой и неконтролируемой. Полный диагноз пациента с бронхиальной астмой включает в себя все вышеперечисленные характеристики. Например, «Бронхиальная астма неаллергического происхождения, интермиттирующая, контролируемая, в стадии стабильной ремиссии».
Симптомы бронхиальной астмы
Приступ удушья при бронхиальной астме делится на три периода: период предвестников, период разгара и период обратного развития. Период предвестников наиболее выражен у пациентов с инфекционно-аллергической природой БА, он проявляется вазомоторными реакциями со стороны органов носоглотки (обильные водянистые выделения, непрекращающееся чихание). Второй период (он может начаться внезапно) характеризуется ощущением стесненности в грудной клетке, которое не позволяет дышать свободно. Вдох становится резким и коротким, а выдох наоборот продолжительным и шумным. Дыхание сопровождается громкими свистящими хрипами, появляется кашель с вязкой, трудно отхаркиваемой мокротой, что делает дыхание аритмичным.
Во время приступа положение пациента вынужденное, обычно он старается принять сидячее положение с наклоненным вперед корпусом, и найти точку опоры или опирается локтями в колени. Лицо становится одутловатым, а во время выдоха шейные вены набухают. В зависимости от тяжести приступа можно наблюдать участие мышц, которые помогают преодолеть сопротивление на выдохе. В периоде обратного развития начинается постепенное отхождение мокроты, количество хрипов уменьшается, и приступ удушья постепенно угасает.
Проявления, при которых можно заподозрить наличие бронхиальной астмы.
- высокотональные свистящие хрипы при выдохе, особенно у детей.
- повторяющиеся эпизоды свистящих хрипов, затрудненного дыхания, чувства стеснения в грудной клетке и кашель, усиливающийся в ночной время.
- сезонность ухудшений самочувствия со стороны органов дыхания
- наличие экземы, аллергических заболеваний в анамнезе.
- ухудшение или возникновение симптоматики при контакте с аллергенами, приеме препаратов, при контакте с дымом, при резких изменениях температуры окружающей среды, ОРЗ, физических нагрузках и эмоциональных напряжениях.
- частые простудные заболевания «спускающиеся» в нижние отделы дыхательных путей.
- улучшение состояние после приема антигистаминных и противоастматических препаратов.
Осложнения
В зависимости от тяжести и интенсивности приступов удушья бронхиальная астма может осложняться эмфиземой легких и последующим присоединением вторичной сердечно-легочной недостаточности. Передозировка бета-адреностимуляторов или быстрое снижение дозировки глюкокортикостероидов, а так же контакт с массивной дозой аллергена могут привести к возникновению астматического статуса, когда приступы удушья идут один за другим и их практически невозможно купировать. Астматический статус может закончиться летальным исходом.
Диагностика
Диагноз обычно ставится клиницистом-пульмонологом на основании жалоб и наличия характерной симптоматики. Все остальные методы исследования направлены на установление степени тяжести и этиологии заболевания. При перкуссии звук ясный коробочный из-за гипервоздушности легких, подвижность легких резко ограничена, а их границы смещены вниз. При аускультации над легкими прослушивается везикулярное дыхание, ослабленное с удлиненным выдохом и с большим количеством сухих свистящих хрипов. Из-за увеличения легких в объеме, точка абсолютной тупости сердца уменьшается, тоны сердца приглушенные с акцентом второго тона над легочной артерией. Из инструментальных исследований проводится:
- Спирометрия. Спирография помогает оценить степень обструкции бронхов, выяснить вариабельность и обратимость обструкции, а так же подтвердить диагноз. При БА форсированный выдох после ингаляции бронхолитиком за 1 секунду увеличивается на 12% (200мл) и более. Но для получения более точной информации спирометрию следует проводить несколько раз.
- Пикфлоуметрия. Измерение пиковой активности выдоха (ПСВ) позволяет проводить мониторинг состояния пациента, сравнивая показатели с полученными ранее. Увеличение ПСВ после ингаляции бронхолитика на 20% и более от ПСВ до ингаляции четко свидетельствует о наличии бронхиальной астмы.
Дополнительная диагностика включает в себя проведение тестов с аллергенами, ЭКГ, бронхоскопию и рентгенографию легких. Лабораторные исследования крови имеют большое значение в подтверждении аллергической природы бронхиальной астмы, а так же для мониторинга эффективности лечения.
- Анализа крови. Изменения в ОАК — эозинофилия и незначительное повышение СОЭ — определяются только в период обострения. Оценка газового состава крови необходима во время приступа для оценки тяжести ДН. Биохимический анализ крови не является основным методом диагностики, так как изменения носят общий характер и подобные исследования назначаются для мониторинга состояния пациента в период обострения.
- Общий анализ мокроты. При микроскопии в мокроте можно обнаружить большое количество эозинофилов, кристаллы Шарко-Лейдена (блестящие прозрачные кристаллы, образующиеся после разрушения эозинофилов и имеющие форму ромбов или октаэдров), спирали Куршмана (образуются из-за мелких спастических сокращений бронхов и выглядят как слепки прозрачной слизи в форме спиралей). Нейтральные лейкоциты можно обнаружить у пациентов с инфекционно-зависимой бронхиальной астмой в стадии активного воспалительного процесса. Так же отмечено выделение телец Креола во время приступа – это округлые образования, состоящие из эпителиальных клеток.
- Исследование иммунного статуса. При бронхиальной астме количество и активность Т-супрессоров резко снижается, а количество иммуноглобулинов в крови увеличивается. Использование тестов для определения количества иммуноглобулинов Е важно в том случае, если нет возможности провести аллергологические тесты.
Лечение бронхиальной астмы
Поскольку бронхиальная астма является хроническим заболеванием вне зависимости от частоты приступов, то основополагающим моментом в терапии является исключение контакта с возможными аллергенами, соблюдение элиминационных диет и рациональное трудоустройство. Если же удается выявить аллерген, то специфическая гипосенсибилизирующая терапия помогает снизить реакцию организма на него.
Для купирования приступов удушья применяют бета-адреномиметики в форме аэрозоля, для того чтобы быстро увеличить просвет бронхов и улучшить отток мокроты. Это фенотерола гидробромид, сальбутамол, орципреналин. Доза в каждом случае подбирается индивидуально. Так же хорошо купируют приступы препараты группы м-холинолитиков – аэрозоли ипратропия бромида и его комбинации с фенотеролом.
Ксантиновые производные пользуются среди больных бронхиальной астмой большой популярностью. Они назначаются для предотвращения приступов удушья в виде таблетированных форм пролонгированного действия. В последние несколько лет препараты, которые препятствуют дегрануляции тучных клеток, дают положительный эффект при лечении бронхиальной астмы. Это кетотифен, кромогликат натрия и антагонисты ионов кальция.
При лечении тяжелых форм БА подключают гормональную терапию, в глюкокортикостероидах нуждается почти четверть пациентов, 15-20 мг Преднизолона принимают в утренние часы вместе с антацидными препаратами, которые защищают слизистую желудка. В условиях стационара гормональные препараты могут быть назначены в виде инъекций. Особенность лечения бронхиальной астмы в том, что нужно использовать лекарственные препараты в минимальной эффективной дозе и добиваться еще большего снижения дозировок. Для лучшего отхождения мокроты показаны отхаркивающие и муколитические препараты.
Прогноз и профилактика
Течение бронхиальной астмы состоит из череды обострений и ремиссий, при своевременном выявлении можно добиться устойчивой и длительной ремиссии, прогноз же зависит в большей степени от того, насколько внимательно пациент относится к своему здоровью и соблюдает предписания врача. Большое значение имеет профилактика бронхиальной астмы, которая заключается в санации очагов хронической инфекции, борьбе с курением, а так же в минимизации контактов с аллергенами. Это особенно важно для людей, которые входят в группу риска или имеют отягощенную наследственность.
Источник


