Тучные клетки при бронхиальной астме
Не следует путать с адипоцитами — «клетками жировой ткани».
Тучные клетки (также известные как мастоциты или лаброциты) — это один из типов белых клеток крови, а именно, один из типов гранулоцитов, которые в зрелом состоянии встраиваются в соединительные ткани, являются частью и нейроиммунной иммунной системы. Происходят из миелоидных стволовых клеток. Содержат большое количество гранул, содержащих медиаторы и модуляторы воспаления, пролиферации и миграции клеток (гистамин, нейтральные протеазы — химаза и триптаза, кислые гидролазы, катепсин G, карбоксипептидаза, гепарин- и хондроитин-сульфат протеогликаны), а также медиаторы воспаления, которые синтезируются при активации клетки PAR , простагландин D2, лейкотриен С4, цитокины IL-4 , IL-5, IL-6, IL-8, IL-13, TNF-aльфа, MIP-laльфа (воспалительный белок la макрофагов), bFGF, гепарин. Несмотря на то, что лучше всего изучена их роль в аллергических реакциях, в частности, при анафилаксии, известно также, что мастоциты играют важную защитную роль, будучи тесно связанными с залечиванием ран, ангиогенезом, аутотолерантностью, противостоянием патогенам и с функциями гемато-энцефалического барьера.
Мастоциты по внешнему виду и функциям сильно схожи с базофилами, другим типом белых клеток крови. Несмотря на то, что мастоциты изначально считали тканевой разновидностью базофилов, было доказано, что эти клетки развиваются не из базофилов (хотя и из общих с ними гемоцитобластов [1]), поэтому не являются одним типом клеток.
Происхождение и классификация[править | править код]
Мастоциты были впервые описаны в 1878 г. Паулем Эрлихом в его докторской диссертации. Наличие гранул привело Эрлиха к неправильному мнению, что эти клетки существуют для питания окружающих тканей, поэтому он назвал их Mastzellen (от немецкого глагола Mast, означающего «откармливать»). Сейчас мастоциты рассматриваются как клетки иммунной системы.
Иллюстрация активации мастоцитов и анафилаксии
Мастоциты сильно схожи с базофильными гранулоцитами (класс белых клеток крови). Оба типа являются гранулоцитами, содержащими антикоагулянты гистамин и гепарин. Fc-фрагмент иммуноглобулина Е (IgE) связывается с мастоцитами и базофилами, когда активный центр иммуноглобулина E связывается с антигеном. Это приводит к высвобождению путем дегрануляции гистамина и других медиаторов воспаления. Эти сходства позволили многим ученым считать, что мастоциты относятся к базофильной ткани, кроме того, мастоциты и базофилы имеют общего предка в красном костном мозге, выделяющего белок CD34. Базофилы покидают костный мозг в зрелом состоянии, тогда как мастоциты циркулируют в незрелой форме, созревая лишь после выхода в ткани. Место, на котором обосновывается незрелая клетка, вероятно, зависит от характеристик отдельных клеток. Первая выращенная и дифференцированная in vitro чистая популяция мышиных мастоцитов была получена благодаря использованию кондиционированной среды, полученной с применением конквалин А-стимулированных спленоцитов. Позже было показано, что интерлейкин-3 являлся необходимым компонентом для дифференциации и роста мастоцитов. Мастоциты грызунов принято подразделять на 2 подтипа: мастоциты соединительной ткани и мастоциты слизистой. Активность последних зависит от Т-клеток. Мастоциты представлены во многих тканях, в том числе вокруг кровеносными сосудов и нервов, а особенно многочисленны они рядом с границей между внешней и внутренней средой — в коже, слизистой легких, тканях пищеварительного тракта, в тканях ротовой полости, в конъюнктиве и др.
Физиология[править | править код]
Мастоциты играют ключевую роль в воспалительных процессах. При активации мастоциты могут постепенно выделять (частичная дегрануляция) или мгновенно выделять (анафилактическая дегрануляция) «медиаторы воспаления», или соединения, приводящие к воспалению, хранящиеся в гранулах, в микросреду. Дегрануляцию могут вызывать:
- аллергены через кросс-связывание с рецепторами иммуноглобулинов Е (к примеру FcεRI)
- физическая травма, через рецепторы молекулярных фрагментов, ассоциированных с повреждениями (DAMP)
- бактериальные патогены через толл-подобные рецепторы (рецепторы ПАМП)
- различные соединения через их связанные с G-белком рецепторы (к примеру, морфий, через опиоидный рецептор) или через лиганд-зависимые ионные каналы.
- некоторые мембранные белки на поверхности мастоцитов, влияя на их функционирование.
Мастоциты экспрессируют высокоаффинный рецептор (FcεRI) для Fc-фрагмента IgЕ. Этот рецептор имеет столь большое сродство с IgЕ, что их связывание по сути необратимо. В результате мастоциты оказываются облепленными IgЕ, которые производятся плазматическими клетками (антителообразующие клетки иммунной системы). Молекулы IgE, как и все антитела, специализируются на одном конкретном антигене.
При аллергических реакциях мастоциты остаются неактивными до связывания аллергена с IgE, которые уже облепили клетку. Как правило, аллергенами являются белки или полисахариды. Антигены связываются с антигенсвязывающими участками, расположенными на вариабельных участках молекул IgE, связанных с поверхностью мастоцита. Оказывается, что связь двух и более молекул IgE (путем кросс-сопряжения, то есть образования поперечных межмолекулярных связей) обязательна для активации мастоцита. Кластеризация внутриклеточных доменов Fc рецепторов, соединенных с кросс-связанными молекулами IgE, вызывает сложную последовательность реакций внутри мастоцитов, которая приводит к их активации (и последующей дегрануляции). Несмотря на то, что данные реакции обычно рассматриваются как причина аллергии, они появились и развивались как защитная реакция против бактерий и паразитов.
За активацией мембранных рецепторов мастоцита следует высвобождение путем дегрануляции уникального, стимул-специфического набора медиаторов мастоцита. Примеры медиаторов, выделяющихся в внеклеточное пространство во время дегрануляции мастоцитов:
- преформированные (образованные предварительно) медиаторы (из гранул)
- сериновые протеазы, к примеру, триптаза и химаза
- гистамин
- серотонин
- протеогликаны, в основном гепарин (действует как антикоагулянт)
- некоторые хондроитинсульфаты
- аденозинтрифосфат (АТФ)
- лизосомальные ферменты
- β-гексозаминидаза
- β-глюкуронидаза
- арилсульфаты
- синтезируемые при стимуляции липидные медиаторы (эйкозаноиды)
- тромбоксан
- простагландин D2
- лейкотриен С4
- тромбоцит-активирующий фактор
- цитокины
- фактор некроза опухоли-α (TNF-α)
- основной фактор роста фибробластов
- интерлейкин-4
- фактор стволовых клеток
- хемокины, к примеру хемотаксический фактор эозинофилов
- реактивные формы кислорода
Гистамин расширяет посткапиллярные венулы, влияет на эндотелий, увеличивая проницаемость кровеносных сосудов. Это приводит к местному отеку, повышению температуры, покраснению и активации других близлежащих (местных) воспалительных клеток. Также приводит к деполяризации нервных окончаний, что приводит к появлению зуда или боли. Признаки выделения гистамина на коже проявляются в виде вздутостей и красных пятен, подобных тем, которые незамедлительно следуют за комариным укусом. Симптомы такой реакции появляются в считанные секунды после контакта аллергена с мастоцитом.
Некоторые данные указывают на то, что мастоциты играют важную роль в врожденном иммунитете. Они способны вырабатывать в огромных количествах важные цитокины и другие воспалительные медиаторы, такие как TNF-α; также они в больших количествах экспрессируют толл-подобные рецепторы (рецепторы ПАМП), которые вовлечены в распознавание широких классов патогенов; мыши, не имеющие мастоцитов, гораздо более восприимчивы к большинству инфекций, нежели мыши с мастоцитами. Гранулы мастоцитов содержат множество биологически активных веществ. Эти гранулы через псевдоподии мастоцитов могут передаваться в соседние клетки иммунной системы и нейроны.
Ссылки[править | править код]
- Тучные клетки: общие сведения. База знаний по боплогии человека. Дата обращения 12 июня 2019.
- Тучные клетки. Гипермаркет-здоровья.рф. Дата обращения 12 июня 2019.
Примечания[править | править код]
Источник

Бронхиальная астма – это хроническое неинфекционное заболевание дыхательных путей воспалительного характера. Приступ бронхиальной астмы часто развивается после предвестников и характеризуется коротким резким вдохом и шумным длительным выдохом. Обычно он сопровождается кашлем с вязкой мокротой и громкими свистящими хрипами. Методы диагностики включают оценку данных спирометрии, пикфлоуметрии, аллергопроб, клинических и иммунологических анализов крови. В лечении используются аэрозольные бета-адреномиметики, м-холинолитики, АСИТ, при тяжелых формах заболевания применяются глюкокортикостероиды.
Общие сведения
За последние два десятка лет заболеваемость бронхиальной астмой (БА) выросла, и на сегодняшний день в мире около 300 миллионов астматиков. Это одно из самых распространенных хронических заболеваний, которому подверженные все люди, вне зависимости от пола и возраста. Смертность среди больных бронхиальной астмой достаточно высока. Тот факт, что в последние двадцать лет заболеваемость бронхиальной астмой у детей постоянно растет, делает бронхиальную астму не просто болезнью, а социальной проблемой, на борьбу с которой направляется максимум сил. Несмотря на сложность, бронхиальная астма хорошо поддается лечению, благодаря которому можно добиться стойкой и длительной ремиссии. Постоянный контроль над своим состоянием позволяет пациентам полностью предотвратить наступление приступов удушья, снизить или исключить прием препаратов для купирования приступов, а так же вести активный образ жизни. Это помогает поддержать функции легких и полностью исключить риск осложнений.

Бронхиальная астма
Причины
Наиболее опасными провоцирующими факторами для развития бронхиальной астмы являются экзогенные аллергены, лабораторные тесты на которые подтверждают высокий уровень чувствительности у больных БА и у лиц, которые входят в группу риска. Самыми распространенными аллергенами являются бытовые аллергены – это домашняя и книжная пыль, корм для аквариумных рыбок и перхоть животных, аллергены растительного происхождения и пищевые аллергены, которые еще называют нутритивными. У 20-40% больных бронхиальной астмой выявляется сходная реакция на лекарственные препараты, а у 2% болезнь получена вследствие работы на вредном производстве или же, например, в парфюмерных магазинах.
Инфекционные факторы тоже являются важным звеном в этиопатогенезе бронхиальной астмы, так как микроорганизмы, продукты их жизнедеятельности могут выступать в качестве аллергенов, вызывая сенсибилизацию организма. Кроме того, постоянный контакт с инфекцией поддерживает воспалительный процесс бронхиального дерева в активной фазе, что повышает чувствительность организма к экзогенным аллергенам. Так называемые гаптенные аллергены, то есть аллергены небелковой структуры, попадая в организм человека и связываясь его белками так же провоцируют аллергические приступы и увеличивают вероятность возникновения БА. Такие факторы, как переохлаждение, отягощенная наследственность и стрессовые состояния тоже занимают одно из важных мест в этиологии бронхиальной астмы.
Патогенез
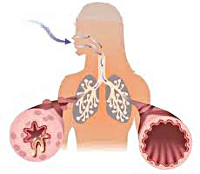
Хронические воспалительные процессы в органах дыхания ведут к их гиперактивности, в результате которой при контакте с аллергенами или раздражителями, мгновенно развивается обструкция бронхов, что ограничивает скорость потока воздуха и вызывает удушье. Приступы удушья наблюдаются с разной периодичностью, но даже в стадии ремиссии воспалительный процесс в дыхательных путях сохраняется. В основе нарушения проходимости потока воздуха, при бронхиальной астме лежат следующие компоненты: обструкция дыхательных путей из-за спазмов гладкой мускулатуры бронхов или вследствие отека их слизистой оболочки; закупорка бронхов секретом подслизистых желез дыхательных путей из-за их гиперфункции; замещение мышечной ткани бронхов на соединительную при длительном течении заболевания, из-за чего возникают склеротические изменения в стенке бронхов.
В основе изменений бронхов лежит сенсибилизация организма, когда при аллергических реакциях немедленного типа, протекающих в виде анафилаксий, вырабатываются антитела, а при повторной встрече с аллергеном происходит мгновенное высвобождение гистамина, что и приводит к отеку слизистой бронхов и к гиперсекреции желез. Иммунокомплексные аллергические реакции и реакции замедленной чувствительности протекают аналогично, но с менее выраженными симптомами. Повышенное количество ионов кальция в крови человека в последнее время тоже рассматривается как предрасполагающий фактор, так как избыток кальция может провоцировать спазмы, в том числе и спазмы мускулатуры бронхов.
При патологоанатомическом исследовании умерших во время приступа удушья отмечается полная или частичная закупорка бронхов вязкой густой слизью и эмфизематозное расширение легких из-за затрудненного выдоха. Микроскопия тканей чаще всего имеет сходную картину – это утолщенный мышечный слой, гипертрофированные бронхиальные железы, инфильтративные стенки бронхов с десквамацией эпителия.
Классификация
БА подразделяется по этиологии, тяжести течения, уровню контроля и другим параметрам. По происхождению выделяют аллергическую (в т. ч. профессиональную БА), неаллергическую (в т. ч. аспириновую БА), неуточненную, смешанную бронхиальную астму. По степени тяжести различают следующие формы БА:
- Интермиттирующая (эпизодическая). Симптомы возникают реже одного раза в неделю, обострения редкие и короткие.
- Персистирующая (постоянного течения). Делится на 3 степени:
- легкая — симптомы возникают от 1 раза в неделю до 1 раза в месяц
- средняя — частота приступов ежедневная
- тяжелая — симптомы сохраняются практически постоянно.
В течении астмы выделяют обострения и ремиссию (нестабильную или стабильную). По возможности контроля над пристпуами БА может быть контролируемой, частично контролируемой и неконтролируемой. Полный диагноз пациента с бронхиальной астмой включает в себя все вышеперечисленные характеристики. Например, «Бронхиальная астма неаллергического происхождения, интермиттирующая, контролируемая, в стадии стабильной ремиссии».
Симптомы бронхиальной астмы
Приступ удушья при бронхиальной астме делится на три периода: период предвестников, период разгара и период обратного развития. Период предвестников наиболее выражен у пациентов с инфекционно-аллергической природой БА, он проявляется вазомоторными реакциями со стороны органов носоглотки (обильные водянистые выделения, непрекращающееся чихание). Второй период (он может начаться внезапно) характеризуется ощущением стесненности в грудной клетке, которое не позволяет дышать свободно. Вдох становится резким и коротким, а выдох наоборот продолжительным и шумным. Дыхание сопровождается громкими свистящими хрипами, появляется кашель с вязкой, трудно отхаркиваемой мокротой, что делает дыхание аритмичным.
Во время приступа положение пациента вынужденное, обычно он старается принять сидячее положение с наклоненным вперед корпусом, и найти точку опоры или опирается локтями в колени. Лицо становится одутловатым, а во время выдоха шейные вены набухают. В зависимости от тяжести приступа можно наблюдать участие мышц, которые помогают преодолеть сопротивление на выдохе. В периоде обратного развития начинается постепенное отхождение мокроты, количество хрипов уменьшается, и приступ удушья постепенно угасает.
Проявления, при которых можно заподозрить наличие бронхиальной астмы.
- высокотональные свистящие хрипы при выдохе, особенно у детей.
- повторяющиеся эпизоды свистящих хрипов, затрудненного дыхания, чувства стеснения в грудной клетке и кашель, усиливающийся в ночной время.
- сезонность ухудшений самочувствия со стороны органов дыхания
- наличие экземы, аллергических заболеваний в анамнезе.
- ухудшение или возникновение симптоматики при контакте с аллергенами, приеме препаратов, при контакте с дымом, при резких изменениях температуры окружающей среды, ОРЗ, физических нагрузках и эмоциональных напряжениях.
- частые простудные заболевания «спускающиеся» в нижние отделы дыхательных путей.
- улучшение состояние после приема антигистаминных и противоастматических препаратов.
Осложнения
В зависимости от тяжести и интенсивности приступов удушья бронхиальная астма может осложняться эмфиземой легких и последующим присоединением вторичной сердечно-легочной недостаточности. Передозировка бета-адреностимуляторов или быстрое снижение дозировки глюкокортикостероидов, а так же контакт с массивной дозой аллергена могут привести к возникновению астматического статуса, когда приступы удушья идут один за другим и их практически невозможно купировать. Астматический статус может закончиться летальным исходом.
Диагностика
Диагноз обычно ставится клиницистом-пульмонологом на основании жалоб и наличия характерной симптоматики. Все остальные методы исследования направлены на установление степени тяжести и этиологии заболевания. При перкуссии звук ясный коробочный из-за гипервоздушности легких, подвижность легких резко ограничена, а их границы смещены вниз. При аускультации над легкими прослушивается везикулярное дыхание, ослабленное с удлиненным выдохом и с большим количеством сухих свистящих хрипов. Из-за увеличения легких в объеме, точка абсолютной тупости сердца уменьшается, тоны сердца приглушенные с акцентом второго тона над легочной артерией. Из инструментальных исследований проводится:
- Спирометрия. Спирография помогает оценить степень обструкции бронхов, выяснить вариабельность и обратимость обструкции, а так же подтвердить диагноз. При БА форсированный выдох после ингаляции бронхолитиком за 1 секунду увеличивается на 12% (200мл) и более. Но для получения более точной информации спирометрию следует проводить несколько раз.
- Пикфлоуметрия. Измерение пиковой активности выдоха (ПСВ) позволяет проводить мониторинг состояния пациента, сравнивая показатели с полученными ранее. Увеличение ПСВ после ингаляции бронхолитика на 20% и более от ПСВ до ингаляции четко свидетельствует о наличии бронхиальной астмы.
Дополнительная диагностика включает в себя проведение тестов с аллергенами, ЭКГ, бронхоскопию и рентгенографию легких. Лабораторные исследования крови имеют большое значение в подтверждении аллергической природы бронхиальной астмы, а так же для мониторинга эффективности лечения.
- Анализа крови. Изменения в ОАК — эозинофилия и незначительное повышение СОЭ — определяются только в период обострения. Оценка газового состава крови необходима во время приступа для оценки тяжести ДН. Биохимический анализ крови не является основным методом диагностики, так как изменения носят общий характер и подобные исследования назначаются для мониторинга состояния пациента в период обострения.
- Общий анализ мокроты. При микроскопии в мокроте можно обнаружить большое количество эозинофилов, кристаллы Шарко-Лейдена (блестящие прозрачные кристаллы, образующиеся после разрушения эозинофилов и имеющие форму ромбов или октаэдров), спирали Куршмана (образуются из-за мелких спастических сокращений бронхов и выглядят как слепки прозрачной слизи в форме спиралей). Нейтральные лейкоциты можно обнаружить у пациентов с инфекционно-зависимой бронхиальной астмой в стадии активного воспалительного процесса. Так же отмечено выделение телец Креола во время приступа – это округлые образования, состоящие из эпителиальных клеток.
- Исследование иммунного статуса. При бронхиальной астме количество и активность Т-супрессоров резко снижается, а количество иммуноглобулинов в крови увеличивается. Использование тестов для определения количества иммуноглобулинов Е важно в том случае, если нет возможности провести аллергологические тесты.
Лечение бронхиальной астмы
Поскольку бронхиальная астма является хроническим заболеванием вне зависимости от частоты приступов, то основополагающим моментом в терапии является исключение контакта с возможными аллергенами, соблюдение элиминационных диет и рациональное трудоустройство. Если же удается выявить аллерген, то специфическая гипосенсибилизирующая терапия помогает снизить реакцию организма на него.
Для купирования приступов удушья применяют бета-адреномиметики в форме аэрозоля, для того чтобы быстро увеличить просвет бронхов и улучшить отток мокроты. Это фенотерола гидробромид, сальбутамол, орципреналин. Доза в каждом случае подбирается индивидуально. Так же хорошо купируют приступы препараты группы м-холинолитиков – аэрозоли ипратропия бромида и его комбинации с фенотеролом.
Ксантиновые производные пользуются среди больных бронхиальной астмой большой популярностью. Они назначаются для предотвращения приступов удушья в виде таблетированных форм пролонгированного действия. В последние несколько лет препараты, которые препятствуют дегрануляции тучных клеток, дают положительный эффект при лечении бронхиальной астмы. Это кетотифен, кромогликат натрия и антагонисты ионов кальция.
При лечении тяжелых форм БА подключают гормональную терапию, в глюкокортикостероидах нуждается почти четверть пациентов, 15-20 мг Преднизолона принимают в утренние часы вместе с антацидными препаратами, которые защищают слизистую желудка. В условиях стационара гормональные препараты могут быть назначены в виде инъекций. Особенность лечения бронхиальной астмы в том, что нужно использовать лекарственные препараты в минимальной эффективной дозе и добиваться еще большего снижения дозировок. Для лучшего отхождения мокроты показаны отхаркивающие и муколитические препараты.
Прогноз и профилактика
Течение бронхиальной астмы состоит из череды обострений и ремиссий, при своевременном выявлении можно добиться устойчивой и длительной ремиссии, прогноз же зависит в большей степени от того, насколько внимательно пациент относится к своему здоровью и соблюдает предписания врача. Большое значение имеет профилактика бронхиальной астмы, которая заключается в санации очагов хронической инфекции, борьбе с курением, а так же в минимизации контактов с аллергенами. Это особенно важно для людей, которые входят в группу риска или имеют отягощенную наследственность.
Источник


