Вентиляция легких при астме
Показания
Показания к ИВЛ у больного бронхиальной астмой возникают в случаях, когда он не в состоянии самостоятельно обеспечить адекватный газообмен. Для клинициста основная трудность заключается в том, чтобы решить, когда рутинные методы лечения астмы оказываются безуспешными и требуется перевод больного на ИВЛ. Поскольку большинство больных с бронхиальной астмой молоды и в остальных отношениях здоровы, они могут долгое время дышать самостоятельно, несмотря на значительно повышенную работу дыхания. Однако при развитии острой дыхательной недостаточности возникают показания к ИВЛ. Правда, эти больные оказываются способными поддерживать нормальный уровень элиминации двуокиси углерода (РаС02 < 40 мм рт. ст.) почти до полного истощения дыхательных усилий. Но с момента, когда в организме начинает накапливаться С2, быстро развиваются гиперкарбия и ацидоз.
Показания к ИВЛ у больных бронхиальной астмой
Острая дыхательная недостаточность
Угроза развития острой дыхательной недостаточности Тяжелая гипоксемия ситуации больной уже утомлен и задержка с началом И В Л приводит к еще больше гиповентиляции. Хотя некоторые специалисты являются сторонниками неинвазивной ИВЛ при остром приступе бронхиальной астмы, широкомасштабных исследований, которые убедительно подтвердили бы правильность такого подхода не проводилось.
Параметры вентиляции
Основная проблема, возникающая при ИВЛ больных с бронхиальной астмой,— это феномен ауто-ПДКВ. При проведении ИВЛ следует стремиться свести данное явление к минимуму (табл. 20-2, рис. 20-2), На ранних стадиях лечения достижение такой цели может потребовать пермиссивной гиперкапнии. При этом надо проводить интенсивную бронхорасширяющую терапию. Ингаляции бронхолитиков и внутривенное введение стероидов являются важнейшим компонентами лечения этих больных.
Хотя может применяться 11В Л как управляемая по давлению, так и управляемая по объему, у некоторых больных в качестве стартового метода предпочтительнее
выбирать ИВЛ. управляемую по объему. В крайне тяжелых случаях может потребоваться очень высокое давление вдувания, правда» при этом следует избегать чрезмерного повышения пикового альвеолярного давления. Хотя иногда возникает необходимость в повышении пикового давления в дыхательных путях до 60-70 см вод. ст., давление плато следует поддерживать на уровне ниже 30 см вод. ст. Разница между пиковым давлением и давлением плато позволяет судить о сопротивлении дыхательных путей. По мере уменьшения тяжести состояния больного можно переводить на ИВЛ, управляемую по давлению. Данный метод рекомендуют из-за того, что время вдоха не ограничивается активацией верхнего предела давле-
ния, как это нередко случается при ИВЛ, управляемой по объему. При ИВЛ, управляемой по давлению, изменение доставленного в легкие дыхательного объема при фиксированном давлении является хорошим показателем динамики сопротивления дыхательных путей и объема воздушной ловушки. По мере снижения тяжести астматического приступа дыхательный объем при ИВЛ, управляемой по давлению, возрастает. Практически всегда приходится вводить седативные препараты для предупреждения десинхронизации больного и респиратора. Некоторым больным также приходится вводить миорелаксанты, хотя их применения следует, по возможности, избегать. После окончания применения миорелаксантов у некоторых больных развивается длительный нервно-мышечный блок, особенно у тех, кто получал большие дозы кортикостероидов. Полная респираторная поддержка может быть успешно осуществлена только при адекватной седации больного.
Для того чтобы свести к минимуму величину ауто-ПДКВ, надо применять небольшие дыхательные объемы (4-8 мл/кг). Окончательно величину дыхательного объема устанавливают в зависимости от пикового альвеолярного давления. Объем следует снижать, чтобы добиться давления плато ниже 30 см вод. ст. Частоту следует устанавливать в зависимости от объема воздушной ловушки и величины ауто-ПДКВ. Теоретически, чем ниже частота вентиляции, тем меньше объем воздушной ловушки. Правда, у некоторых больных бронхиальной астмой удается увеличивать частоту дыхания до 15-20 в 1 мин без заметного возрастания ауто-ПДКВ. Реакции больных сугубо индивидуальны и могут значительно различаться. Некоторым достаточно частоты 8 в 1 мин, другим необходимо устанавливать частоту 20 в 1 мин.
Малый дыхательный объем в сочетании с низкой частотой вентиляции приводит к задержке С2 в организме. Общим правилом является поддержание рН крови на уровне не ниже 7,20. Однако у молодых, здоровых в прочих отношениях индивидов, страдающих бронхиальной астмой, приемлемым часто оказывается уровень рН 7,10. Риск баротравмы и гипотензии обычно имеет большее значение, чем риск ацидоза, возникающего вследствие малого дыхательного и минутного объемов вентиляции.
Время вдоха должно быть укорочено, так как ауто-ПДКВ снижается при уменьшении минутной Вентиляции и удлинении экспираторного времени. При увеличении инспираторного времени дыхательный объем распределяется в легких равномернее. Рекомендуется устанавливать время вдоха равным 1-1,5 с и оценивать величину ауто-ПДКВ. У многих больных при невысокой частоте вентиляции увеличение инспираторного времени с 1 до 1,5 с не оказывает значительного влияния на величину ауто-ПДКВ. Время вдоха свыше 1,5 с надо применять с осторожностью. При ИВЛ, управляемой по объему, следует выбирать нисходящую форму кривой потока, чтобы улучшить распределение дыхательного объема во время вдоха. Если же выбирается прямоугольная форма кривой, то инспираторное время должно быть значительно укорочено. Величину пикового потока настраивают таким образом, чтобы обеспечить требуемое инспираторное время; часто оказываются необходимы потоки выше 60 л/мин.
При настройке стартовых параметров Fi02 устанавливают на уровне 1,0, а затем снижают, если показатели пульсоксиметрии и газового состава крови свидетельствуют об адекватной оксигенации. Мнения относительно целесообразности применения ПДКВ при бронхиальной астме противоречивы. Ауто-ПДКВ увеличивает градиент давления, необходимый для триггерного запуска аппаратного вдоха. ПДКВ повышает давление в контуре респиратора и снижает разницу давлений, действуя в качестве противовеса для ауто-ПДКВ. В случаях, когда ауто-ПДКВ развивается вследствие ограничения потока, внешнее ПДКВ не приводит к повышению суммарного ПДКВ. Но выгодно ли для больного дополнительное ПДКВ, если проводится принудительная вентиляция? Оно способно улучшить распределение дыхательного объема, так как участки легких, не участвующие в дыхании из-за ауто-ПДКВ, могут быть рекрутированы и стабилизированы с помощью ПДКВ. Если при ИВЛ используют ПДКВ, то его величина не должна превышать уровень, при котором начи1 нает возрастать общее ПДКВ. Применение ПДКВ на фоне ИВЛ при бронхиальной
- Выявление баротравмы
- Пиковое альвеолярное давление и среднее давление в дыхательных путях
- Ауто-ПДКВ
- Пульсоксиметрия и газовый состав артериальной крови
- Частота сердечных сокращений и артериальное давление при астме требует тщательного мониторина газообмена, пикового альвеолярного давления, ауто-ПДКВ и гемодинамических показателей.
Источник
ЦЕЛИ
- Перечислить показания к ИВЛ у больных с приступом бронхиальной астмы.
- Перечислить стартовые параметры вентиляции у больных с приступом бронхиальной астмы.
- Обсудить принципы мониторинга при ИВЛ по поводу бронхиальной астмы.
- Обсудить особенности восстановления самостоятельного дыхания у больных с бронхиальной астмой.
- Рассмотреть роль гелиокса в лечении больных бронхиальной астмой.
Приступ бронхиальной астмы может сопровождаться значительной гипоксемией и гиперкапнией. Сопротивление дыхательных путей возрастает настолько, что у многих больных вдыхаемый газ не достигает периферии легких. Действительно, у некоторых больных при аускультации дыхательные шумы могут отсутствовать.
Начиная с 1960-х гг., летальность при бронхиальной астме непрерывно возрастает.
Трудно понять, является ли это следствием увеличения частоты и тяжести заболевания или результатом самоуспокоенности в отношении методов лечения данного заболевания. Пациенты с развернутой клиникой астматического приступа должны рассматриваться как больные, находящиеся в неотложном, угрожающем жизни состоянии, которым в любой момент может потребоваться интубация трахеи и искусственная вентиляция легких.
ОБЗОР
Клинические проявления
Астма проявляется наличием свистящих хрипов, ригидностью грудной клетки, кашлем и повышенной реактивностью дыхательных путей, носящими преходящий характер. Во время тяжелого приступа бронхиальной астмы больной находится в состоянии сильнейшего стресса, обусловленного затрудненным дыханием: его легкие раздуты, а при аускультации в них выслушиваются сухие свистящие хрипы. Однако в наиболее тяжелых случаях обструкция бронхов оказывается настолько выраженной, что хрипы отсутствуют и дыхательные шумы не выслушиваются. Для тяжелого астматического приступа характерны значительные колебания внутригрудного давления и амплитуды пульсовой волны (парадоксальный пульс) в фазы вдоха и выдоха. Как правило, дыхательные пути пациента заполнены вязким секретом. Развиваются спазм бронхов и отек их слизистой оболочки. При спирометрии выявляют снижение ОФВ1 и пикового экспираторного потока.
Ауто-ПДКВ
У всех больных с бронхиальной астмой в легких возникает воздушная ловушка и повышается ауто-ПДКВ. Воздушная ловушка появляется в результате отека слизистой оболочки бронхов, воспалительных изменений и секреции, вызывающих обструкцию бронхов по механизму шарового клапана. В некоторых функциональных единицах легких ловушки и обусловленное ими вздутие альвеол могут стать столь значительными, что дыхание в этом участке прекращается. Участки с раздутыми альвеолами вследствие образования воздушных ловушек и развития ауто-ПДКВ могут сдавливать соседние ацинусы. Именно преодоление ауто-ПДКВ и повышенного легочного сопротивления вызывает появление парадоксального пульса. Так, в сочетании с увеличенным вследствие гипоксемии дыхательным драйвом инспи-раторный транспульмональный градиент давления может достигать 25 см вод. ст. Во время выдоха происходит активация экспираторных мышц в попытке минимизировать функциональную остаточную емкость, ауто-ПДКВ и работу дыхания.

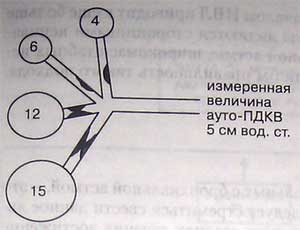
Измерение ауто-ПДКВ, выполненное традиционным способом (во время конечно-экспираторной паузы), может оказаться неточным, если имеется обструкция дыхательных путей. В приведенном на рисунке примере ауто-ПДКВ равно 5 см вод. ст., то есть среднему значению для участков лёгких, в которых значения ауто-ПДКВ равны 4 и 6 см вод. ст. Однако в некоторых участках ауто-ПДКВ намного выше измеренного (12 и 15 см вод. ст.)
Вследствие образования воздушной ловушки нарастает функциональная остаточная емкость, что сдвигает дыхательный объем в ту часть кривой давление-объем, которая соответствует области наименьшей растяжимости дыхательной системы, что, в свою очередь, еще больше увеличивает энергетические затраты на дыхание. Измеренная величина ауто-ПДКВ у некоторых больных астмой может не отражать величину объема ловушки, возникшей вследствие полной обструкции дыхательных путей (рис.). В идеале эти больные должны дышать медленно и глубоко, чтобы уменьшить воздушную ловушку, увеличить выдыхаемый объем и свести к минимуму дыхательное усилие. Однако возбуждение и психомоторное беспокойство в сочетании с повышенным дыхательным драйвом обычно препятствуют осуществлению такого идеального варианта дыхания.
Источник
Показания
Показания к ИВЛ у больного бронхиальной астмой возникают в случаях, когда он не в состоянии самостоятельно обеспечить адекватный газообмен. Для клинициста основная трудность заключается в том, чтобы решить, когда рутинные методы лечения астмы оказываются безуспешными и требуется перевод больного на ИВЛ. Поскольку большинство больных с бронхиальной астмой молоды и в остальных отношениях здоровы, они могут долгое время дышать самостоятельно, несмотря на значительно повышенную работу дыхания. Однако при развитии острой дыхательной недостаточности возникают показания к ИВЛ. Правда, эти больные оказываются способными поддерживать нормальный уровень элиминации двуокиси углерода (РаС02 < 40 мм рт. ст.) почти до полного истощения дыхательных усилий. Но с момента, когда в организме начинает накапливаться С2, быстро развиваются гиперкарбия и ацидоз.
Показания к ИВЛ у больных бронхиальной астмой
Острая дыхательная недостаточность
Угроза развития острой дыхательной недостаточности Тяжелая гипоксемия ситуации больной уже утомлен и задержка с началом И В Л приводит к еще больше гиповентиляции. Хотя некоторые специалисты являются сторонниками неинвазивной ИВЛ при остром приступе бронхиальной астмы, широкомасштабных исследований, которые убедительно подтвердили бы правильность такого подхода не проводилось.
Параметры вентиляции
Основная проблема, возникающая при ИВЛ больных с бронхиальной астмой,— это феномен ауто-ПДКВ. При проведении ИВЛ следует стремиться свести данное явление к минимуму (табл. 20-2, рис. 20-2), На ранних стадиях лечения достижение такой цели может потребовать пермиссивной гиперкапнии. При этом надо проводить интенсивную бронхорасширяющую терапию. Ингаляции бронхолитиков и внутривенное введение стероидов являются важнейшим компонентами лечения этих больных.
Хотя может применяться 11В Л как управляемая по давлению, так и управляемая по объему, у некоторых больных в качестве стартового метода предпочтительнее
выбирать ИВЛ. управляемую по объему. В крайне тяжелых случаях может потребоваться очень высокое давление вдувания, правда» при этом следует избегать чрезмерного повышения пикового альвеолярного давления. Хотя иногда возникает необходимость в повышении пикового давления в дыхательных путях до 60-70 см вод. ст., давление плато следует поддерживать на уровне ниже 30 см вод. ст. Разница между пиковым давлением и давлением плато позволяет судить о сопротивлении дыхательных путей. По мере уменьшения тяжести состояния больного можно переводить на ИВЛ, управляемую по давлению. Данный метод рекомендуют из-за того, что время вдоха не ограничивается активацией верхнего предела давле-
ния, как это нередко случается при ИВЛ, управляемой по объему. При ИВЛ, управляемой по давлению, изменение доставленного в легкие дыхательного объема при фиксированном давлении является хорошим показателем динамики сопротивления дыхательных путей и объема воздушной ловушки. По мере снижения тяжести астматического приступа дыхательный объем при ИВЛ, управляемой по давлению, возрастает. Практически всегда приходится вводить седативные препараты для предупреждения десинхронизации больного и респиратора. Некоторым больным также приходится вводить миорелаксанты, хотя их применения следует, по возможности, избегать. После окончания применения миорелаксантов у некоторых больных развивается длительный нервно-мышечный блок, особенно у тех, кто получал большие дозы кортикостероидов. Полная респираторная поддержка может быть успешно осуществлена только при адекватной седации больного.
Для того чтобы свести к минимуму величину ауто-ПДКВ, надо применять небольшие дыхательные объемы (4-8 мл/кг). Окончательно величину дыхательного объема устанавливают в зависимости от пикового альвеолярного давления. Объем следует снижать, чтобы добиться давления плато ниже 30 см вод. ст. Частоту следует устанавливать в зависимости от объема воздушной ловушки и величины ауто-ПДКВ. Теоретически, чем ниже частота вентиляции, тем меньше объем воздушной ловушки. Правда, у некоторых больных бронхиальной астмой удается увеличивать частоту дыхания до 15-20 в 1 мин без заметного возрастания ауто-ПДКВ. Реакции больных сугубо индивидуальны и могут значительно различаться. Некоторым достаточно частоты 8 в 1 мин, другим необходимо устанавливать частоту 20 в 1 мин.
Малый дыхательный объем в сочетании с низкой частотой вентиляции приводит к задержке С2 в организме. Общим правилом является поддержание рН крови на уровне не ниже 7,20. Однако у молодых, здоровых в прочих отношениях индивидов, страдающих бронхиальной астмой, приемлемым часто оказывается уровень рН 7,10. Риск баротравмы и гипотензии обычно имеет большее значение, чем риск ацидоза, возникающего вследствие малого дыхательного и минутного объемов вентиляции.
Время вдоха должно быть укорочено, так как ауто-ПДКВ снижается при уменьшении минутной Вентиляции и удлинении экспираторного времени. При увеличении инспираторного времени дыхательный объем распределяется в легких равномернее. Рекомендуется устанавливать время вдоха равным 1-1,5 с и оценивать величину ауто-ПДКВ. У многих больных при невысокой частоте вентиляции увеличение инспираторного времени с 1 до 1,5 с не оказывает значительного влияния на величину ауто-ПДКВ. Время вдоха свыше 1,5 с надо применять с осторожностью. При ИВЛ, управляемой по объему, следует выбирать нисходящую форму кривой потока, чтобы улучшить распределение дыхательного объема во время вдоха. Если же выбирается прямоугольная форма кривой, то инспираторное время должно быть значительно укорочено. Величину пикового потока настраивают таким образом, чтобы обеспечить требуемое инспираторное время; часто оказываются необходимы потоки выше 60 л/мин.
При настройке стартовых параметров Fi02 устанавливают на уровне 1,0, а затем снижают, если показатели пульсоксиметрии и газового состава крови свидетельствуют об адекватной оксигенации. Мнения относительно целесообразности применения ПДКВ при бронхиальной астме противоречивы. Ауто-ПДКВ увеличивает градиент давления, необходимый для триггерного запуска аппаратного вдоха. ПДКВ повышает давление в контуре респиратора и снижает разницу давлений, действуя в качестве противовеса для ауто-ПДКВ. В случаях, когда ауто-ПДКВ развивается вследствие ограничения потока, внешнее ПДКВ не приводит к повышению суммарного ПДКВ. Но выгодно ли для больного дополнительное ПДКВ, если проводится принудительная вентиляция? Оно способно улучшить распределение дыхательного объема, так как участки легких, не участвующие в дыхании из-за ауто-ПДКВ, могут быть рекрутированы и стабилизированы с помощью ПДКВ. Если при ИВЛ используют ПДКВ, то его величина не должна превышать уровень, при котором начи1 нает возрастать общее ПДКВ. Применение ПДКВ на фоне ИВЛ при бронхиальной
- Выявление баротравмы
- Пиковое альвеолярное давление и среднее давление в дыхательных путях
- Ауто-ПДКВ
- Пульсоксиметрия и газовый состав артериальной крови
- Частота сердечных сокращений и артериальное давление при астме требует тщательного мониторина газообмена, пикового альвеолярного давления, ауто-ПДКВ и гемодинамических показателей.
Источник


