Журналы по бронхиальной астме у детей
- Авторы
- Резюме
- Файлы
- Ключевые слова
- Литература
Миненкова Т.А.
1
Веденьева М.О.
1
Симкина А.В.
1
1 Курский государственный медицинский университет
В статье рассматриваются возможные варианты результатов исследования функции внешнего дыхания у детей в возрасте от 5 до 14 лет на фоне проводимой терапии и до нее, оценка эффективности назначенных вариантов базисной терапии для исследуемой группы детей. Также в статье отражены результаты обследования детей различных возрастов, количество обследованных — 30 человек. Бронхиальная астма является одним из самых распространенных хронических заболеваний органов дыхания у детей и подростков, что отражается на их качестве жизни и развитии [8]. За последние годы в мире отмечается тенденция к росту заболеваемости бронхиальной астмой. Так, по данным российской официальной статистики (1997–2004), число детей, страдающих бронхиальной астмой, выросло в 1,5–2,0 раза [4]. Основной целью врача является выбор таких методов терапии астмы, в результате которых образуется стойкая ремиссия заболевания вне зависимости от его тяжести. Согласно GINA (2014), основными целями терапии является достижение хорошего контроля над симптомами и поддержание нормального уровня активности ребенка [7]. Полученные результаты демонстрируют тесную взаимосвязь данных исследования функции внешнего дыхания в зависимости от клинической картины течения бронхиальной астмы у детей и проводимой терапии.
бронхиальная астма
функция внешнего дыхания
диагностика
лечение
бронхообструктивный синдром.
1. Балаболкин И. И. Современные подходы к терапии острой бронхиальной астмы у детей // Аллергология и иммунология в педиатрии. — М.: ИНФОМЕДИС. — № 3. — 2010. — С. 12-19.
2. Бронхиальная астма у детей: диагностика, лечение и профилактика. Научно-практическая программа. М. – 2017.
3. Герасимова Н.Г., Горбатов В.А., Коваленко Е.Н. и др., Эффективность применения сингуляра при лечении бронхиальной астмы у детей // Вестник РУДН. — Москва, 2010. — № 4. — С. 185-186.
4. Миненкова Т.А., Мизерницкий Ю.Л., Цыпленкова С.Э., Сорокина Е.В., Ружицкая Е.А., Окунева Т.С., Котов В.С. Клинико-иммунологические особенности бронхиальной астмы, ассоциированной с различными типами грибковой сенсибилизации у детей. // Вопросы практической педиатрии. — № 4. – 2010. – С.12-15.
5. Ненашева Н. М. Обзор некоторых основных изменений GINA – 2014. // Практическая пульмонология. — № 3.– 2014. С. 5.
6. Федеральные клинические рекомендации по диагностике и лечению бронхиальной астмы, М. – 2013г. – С. 31.
7. Akiyama K. The role of fungal allergy in bronichial asthma // Nippon Ishinkin Gakkai Zasshi.- 2009.- V.41.- N 3.- P.149-155.
8. Leon E.E., Craig T.J. Antifungals in the treatment of allergic bronchopulmonary aspergillosis. // Ann. Allergy. Asthma Immunol. — 2009.- V.82.- N 6.- P.511-516. quiz. 516-519.
9. Papadopoulos N.G., Arakawa H., Carlsen K.-H. et al. // Allergy. – 2012. – Vol.67. – P.976–997.
10. Papadopoulos N.G. Asthma in childhood // Global atlas of asthma. – Zurich, 2013. – P.57–60.
Актуальность. Бронхиальная астма (БА) — хроническое воспалительное заболевание дыхательных путей, в котором принимают участие многие клетки и клеточные элементы. Хроническое воспаление обусловливает развитие бронхиальной гиперреактивности, которая приводит к повторяющимся эпизодам свистящих хрипов, одышки, чувства заложенности в груди и кашля в особенности по ночам или ранним утром. Эти эпизоды связаны с распространенной вариабельной обструкцией дыхательных путей в легких, которая часто бывает обратима спонтанно или под влиянием лечения [1,2].
Бронхиальная астма представляет собой серьезную медицинскую и социальную проблему. Во всем мире в последнее время отмечены тенденции к росту заболеваемости во всех возрастных группах, в том числе среди детей. Наиболее подвержены болезни дети, которые впоследствии «перерастают» проблему (около половины болеющих). В последние годы во всем мире наблюдается устойчивый рост заболеваемости, потому работает огромное количество программ, и всемирных, и национальных, по борьбе с астмой.
Приступы удушья наблюдаются с разной периодичностью, но даже в стадии ремиссии воспалительный процесс в дыхательных путях сохраняется. В основе нарушения проходимости потока воздуха, при бронхиальной астме лежат следующие компоненты:
- обструкция дыхательных путей из-за спазмов гладкой мускулатуры бронхов или вследствие отека их слизистой оболочки.
- закупорка бронхов секретом подслизистых желез дыхательных путей из-за их гиперфункции.
- замещение мышечной ткани бронхов на соединительную при длительном течении заболевания, из-за чего возникают склеротические изменения в стенке бронхов.
У больных астмой снижается трудоспособность и часто наступает инвалидность, потому что хронический воспалительный процесс формирует чувствительность к аллергенам, различным химическим раздражителям, дыму, пыли и т.д. из-за чего образуется отечность и бронхоспазм, так как в момент раздражения идет повышенная выработка бронхиальной слизи.
Проблема распространенности астмы в нашей стране требует дальнейшего изучения и уточнения [3].
Остаются открытыми вопросы подбора адекватной терапии при тяжелой форме БА, что обусловлено ограниченными количеством клинических исследований в детской популяции, часто неадекватным подходом при выборе препаратов, их доз, продолжительности лечения, распространенной стероидфобией и низкой приверженностью терапии среди пациентов.
Лечение бронхиальной астмы проводится поэтапно. Каждая из стадий развития требует внесения корректив в план терапевтических мероприятий. Для оценки астмы в динамике и степени контроля заболевания следует использовать пикфлоуметрию. Базисная (основная) терапия предполагает поддерживающее лечение, направленное на уменьшение воспалительной реакции. Рациональная терапия, начатая по возможности раньше, существенно замедляет процесс развития астмы.
Цель. Оценка вариантов базисной терапии у детей, страдающих бронхиальной астмой.
Материалы и методы исследования. Данная работа проведена в дизайне простого открытого клинического проспективного рандомизированного исследования. Было обследовано 30 детей в возрасте от 5 до 14 лет, которым проводилось лечение на базе 1 педиатрического отделения ОБУЗ «ОДКБ»; средний возраст в исследованной группе составил 7,53±0,45 лет; распределение по полу: мальчики составили 60%(18), а девочки – 40%(12).
Критерием включения пациентов в исследование явилось: наличие у них бронхиальной астмы; критерием исключения пациентов из исследования явилось наличие другой патологии. Средняя продолжительность заболевания у обследованных детей составила 1,5±1,3 лет.
В соответствии с поставленными задачами, объемом и характером проводимого лечения были определены следующие варианты базисной терапии: 33,3%(10) пациентам терапия проводилась кромонами, антилейкотриеновыми препаратами (тайлед, сингуляр); монотерапия ингаляционными глюкокортикостероидами (пульмикорт) – 33,3%(10) пациентов, терапия ингаляционными глюкокортикостероидами в средних или высоких дозах в комбинации с ингаляционным ß2-агонистом длительного действия (серетид, симбикорт) – 33,3%(10).
Степень тяжести астмы и уровень контроля болезни на момент сбора информации уточняли в соответствии с Федеральными клиническими рекомендациями по диагностике и лечению бронхиальной астмы от 2013г. и GINA-2014 [5,6].
Статистическая обработка данных проводилась с помощью программ BIOSTAT и EXCEL. Для определения достоверности различий использовали t-критерий Стьюдента. Достоверными считались различия при степени вероятности безошибочного прогноза (р) 95% (р < 0,05).
Результаты и их обсуждение. 50% (15) пациентов поступили в период обострения бронхиальной астмы с менее выраженной симптоматикой, а 13,3%(4) пациентов – в период обострения с приступом удушья, оставшиеся 36,7%(11) пациентов были госпитализированы на дообследование и аллергообследование.
При клиническом обследовании исследуемой группы пациентов было определено, что астму легкой степени тяжести имели 33,3%(10), средней степени – 46,7%(14), тяжелая астма наблюдалась в 20%(6) случаев.
В ходе обследования было выявлено несколько вариантов объективной картины: вариант 1 (перкуторно – ясный легочный звук и аускультативно – везикулярное дыхание) у 26,7%(8), вариант 2 (ясный легочный звук и жесткое дыхание) у 53,3%(16), вариант 3 (коробочный легочный звук, жесткое дыхание, сухие хрипы) у 20%(6) [10].
Данные спирометрии до назначения базисной терапии (рис.1) выглядели следующим образом: ОФВ1 ≥ 80% от должного зарегистрирован у 60%(18) пациентов, ОФВ1 80 – 60% от должного – у 26,7%(8) и менее 60% от должного – у 13,3%(4) [13].
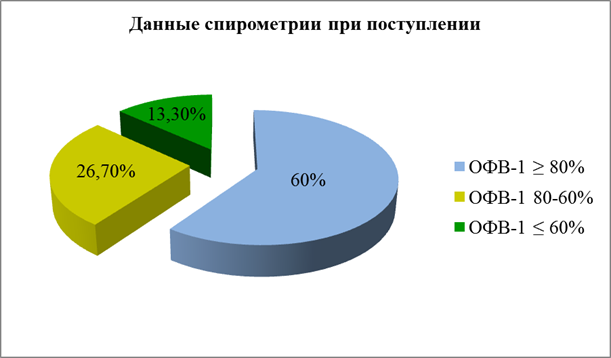
Рис. 1.
Было выявлено, что до начала базисной терапии астма контроль заболевания был достигнут у 60%(18) пациентов, частично контролировалась у 26,7%(8), вовсе не контролировалась у 13,3%(4). При повторном обследовании после проведенного 7 дневного курса базисной терапии астма хорошо поддавалась контролю у 86,6%(26) пациентов, частично контролировалась у 6,7%(2), вовсе не контролировалась у 6,7%(2) [11,12].
При повторной спирометрии после проведенного 7 дневного курса базисной терапии (рис.2) были получены следующие показатели функции внешнего дыхания: ОФВ1 ≥ 80% от должного зарегистрирован у 70%(21) пациентов, ОФВ1 80 – 60% от должного – у 23,3%(7) и менее 60% от должного – у 6,7%(2) [9].

Рис. 2.
Сравнение результатов оценки функции внешнего дыхания, по данным спирометрии, до и после проведения 7 дневного курса базисной терапии показало, что количество лиц, имевших ОФВ-1≤60%, достоверно уменьшилось (p<0,05) [17]. Также наблюдалось уменьшение числа детей, имевших ОФВ-1 80-60% (p>0,05). Соответственно увеличивается количество пациентов с ОФВ-1≥80%. Таким образом, назначенные варианты базисной терапии бронхиальной астмы способствовали улучшению функции внешнего дыхания у исследуемой группы пациентов (рис.3.) [14].
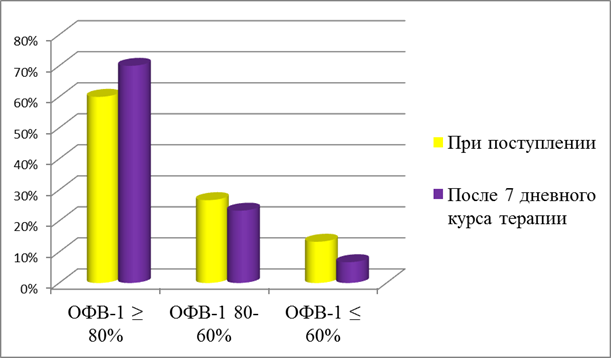
Рис.3.
При сравнении данных по астма контролю до и после проведения 7 дневного курса базисной терапии было выявлено, что количество пациентов в исследованной группе, у которых астма хорошо контролировалась выросло с 60% до 86,6% (p>0,05); также наблюдалось достоверное уменьшение числа детей с частично контролируемой и вовсе не контролируемой бронхиальной астмой (p<0,05). Таким образом, назначенные варианты базисной терапии, являются эффективными в осуществлении контроля бронхиальной астмы [15,16].
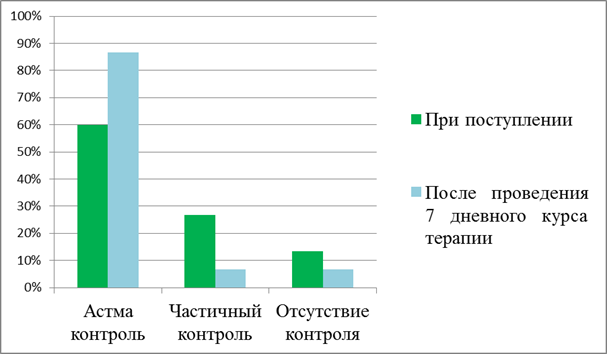
Вывод. Назначенные варианты базисной терапии бронхиальной астмы способствовали улучшению показателей функции внешнего дыхания, т.к. по результатам повторной спирометрии количество пациентов с ОФВ-1≤60% достоверно уменьшилось с 13,3 до 6,7% (p<0,05), также снизилось количество детей, имевших ОФВ-1 80-60% (p>0,05). Проведенная базисная терапия является эффективной для осуществления контроля бронхиальной астмы у исследуемой группы детей, т. к. после повторного обследования наблюдалось достоверное уменьшение числа детей с частично контролируемой (с 26,7 до 6,7%) и вовсе не контролируемой (с 13,3 до 6,7%) астмой (p<0,05) [15]. С целью оптимизации терапии пациентов с частично контролируемой и неконтролируемой астмой на стандартной базисной терапии необходимо внедрение дополнительных препаратов, относящихся к данной ступени, в том числе ИКС, отличающихся большей клинической эффективностью и безопасностью[18].
Библиографическая ссылка
Миненкова Т.А., Веденьева М.О., Симкина А.В. КЛИНИЧЕСКИЕ ОСОБЕННОСТИ БРОНХИАЛЬНОЙ АСТМЫ У ДЕТЕЙ // Международный студенческий научный вестник. – 2018. – № 6.;
URL: https://eduherald.ru/ru/article/view?id=19352 (дата обращения: 25.06.2020).
Предлагаем вашему вниманию журналы, издающиеся в издательстве «Академия Естествознания»
(Высокий импакт-фактор РИНЦ, тематика журналов охватывает все научные направления)
Источник
Определение
Бронхиальная астма (БА) у детей — заболевание, развивающееся на основе хронического аллергического воспаления бронхов, их гиперреактивности и характеризующееся периодически возникающими приступами затрудненного дыхания или удушья в результате обратимой распространенной бронхиальной обструкции, обусловленной бронхоконстрикцией, гиперсекрецией слизи, отеком стенки бронхов.
Эпидемиология
В контексте общих направлений по ведению БА основными целями эпидемиологических исследований являются:
1) определение факторов и групп риска на основе метаанализа при когортных исследованиях гетерогенных популяций;
2) разработка средств модификации и элиминации факторов риска у лиц с потенциальной возможностью развития БА;
3) оценка эффективности модифицирующих воздействий путем проведения рандомизированных исследований;
4) оценка экономической эффективности модифицирующих воздействий;
5) разработка дифференцированных рекомендаций для внедрения в государственную стратегию здравоохранения.
По данным эпидемиологических исследований, на современном этапе бронхиальной астмой страдает от 4 до 8% населения. В детской популяции данный показатель составляет 5-10%. При этом распространенность астмы у детей варьирует в различных странах и популяциях. Однако в структуре хронической патологии органов дыхания она занимает одно из первых мест.
Этиология
Бронхиальная астма является манифестным маркером экологического неблагополучия. Неуклонный рост распространенности бронхиальной астмы у детей, особенно в местностях с напряженной экологической ситуацией, обусловлен дополнительной сенсибилизацией аллергенами техногенной природы. При этом низкомолекулярные экопатогены выступают в роли промоторов аллергии, способствуя сенсибилизации к широкому спектру аллергенов.
1. Факторы, предрасполагающие к развитию бронхиальной астмы:
— наследственность;
— атопия;
— гиперреактивность бронхов.
2. Причинные (сенсибилизирующие) факторы:
1) пищевые аллергены:
— облигатные (коровье молоко, шоколад, яйца, цитрусовые, орехи, мед и др.);
— факультативные (любые пищевые продукты, приводящие к развитию сенсибилизации у конкретного индивидуума);
2) бытовые аллергены:
— домашняя, библиотечная пыль, клещи домашней пыли.
3) эпидермальные:
— шерсть, пух, перо, перхоть, экскременты, слюна животных (кошек, собак, морских свинок, хомячков и других грызунов, птиц, кроликов, лошадей, овец и т.д.) и насекомых (тараканов);
4) пыльцевые аллергены:
— деревья и кустарники (береза, ольха, лещина, или орешник, ива, дуб, каштан, тополь, ясень, вяз и т.д.), злаковые травы (тимофеевка, овсяница, мятлик, пырей, рожь, пшеница и т.д.), сорные травы (лебеда, амброзия, одуванчик, крапива, полынь);
5) грибковые аллергены:
— Candіda albіcans, Aspergіllus flavus, Aspergіllus nіger, Rhіzopus nіgrіcans, Penіcіllіum notatum, Alternarіa tenіus, Cladosporіum herbarum и др.;
6) лекарственные средства:
— антибиотики пенициллинового ряда, сульфаниламиды, витамины, нестероидные противовоспалительные препараты;
7) вирусы и вакцины:
— вирусы, тропные к структурам респираторного тракта, вакцина АКДС;
8) химические вещества:
— промышленные химические вещества, бытовые поллютанты.
3. Факторы, способствующие возникновению бронхиальной астмы:
— вирусные респираторные инфекции;
— патологическое течение беременности у матери;
— недоношенность;
— нерациональное питание;
— атопический дерматит;
— различные поллютанты;
— табачный дым.
4. Факторы, вызывающие обострение бронхиальной астмы, — триггеры:
— аллергены;
— вирусные респираторные инфекции;
— физическая и психоэмоциональная нагрузка;
— изменение метеоситуации;
— экологические воздействия (ксенобиотики, табачный дым, резкие запахи);
— непереносимые продукты, лекарства.
Механизмы формирования БА
1. Иммунное воспаление (и ммунная, патохимическая и патофизиологическая фазы):
— Th2-опосредованная иммунная реакция;
— специфический профиль цитокинов;
— продукция IgE -антител;
— воздействие на тучные клетки и эозинофилы с высвобождением медиаторов воспаления.
2. Нейровегетативный дисбаланс:
— нарушение равновесия между возбуждающими (холинергическая, нехолинергическая и адренергическая система) и ингибирующими (β-адренергическая и неадренергическая ингибирующие системы) системами.
3. Эндокринные дисфункции:
— реализация антистрессового эффекта в системах: гипоталамус — гипофиз — надпочечники; гипоталамус — гипофиз — щитовидная железа.
4. Биологические маркеры патологического процесса:
— дисфункция системы ПОЛ-АОЗ;
— уровень оксида азота;
— электролитный состав конденсата выдыхаемого воздуха.
Морфологические проявления аллергического воспаления при БА
— Наличие эозинофилов в клеточном инфильтрате слизистой оболочки бронхов и бронхиол.
— Дистрофия и деструкция покровного эпителия.
— Утолщение подэпителиального соединительнотканного базального слоя.
— Гипертрофия гладких мышц бронхов.
— Нарушение микроциркуляции.
— Отек слизистой и подслизистой оболочек.
Роль бронхиального эпителия в развитии воспаления при БА
— Прямая активация эпителиальных клеток аллергенами (IgE-зависимый механизм), поллютантами, вирусными частицами.
— Непрямая активация эпителиальных клеток гистамином (из тучных клеток) и цитокинами.
— Десквамация эпителия с обнажением нервных окончаний повышает чувствительность к действию поллютантов и других раздражителей.
— Активация эпителиальных клеток приводит к высвобождению цитокинов, провоспалительных медиаторов, фибронектина.
— Молекулы адгезии (ICAM-1) на поверхности эпителиальных клеток ведут к удержанию воспалительных клеток (эозинофилов, тучных клеток и лимфоцитов).
— Факторы роста, высвобождаемые эпителиальными клетками, в значительной степени способствуют ремоделированию экстраклеточного матрикса.
Клиническая диагностика
1. Оценка анамнестических данных:
— преморбидный фон (недоношенность, нерациональное вскармливание, атопические заболевания, частые ОРВИ).
— наследственный аллергологический анамнез.
— связь заболевания с причинными аллергенами.
— экоаллергия, табачный дым.
— повторяющиеся эпизоды бронхообструкции и эффективность бронхолитической терапии.
2. Клиническая симптоматика:
— экспираторная одышка;
— свистящие хрипы;
— чувство дыхательного дискомфорта;
— приступообразный кашель.
3. Оценка функции внешнего дыхания:
— спирография с оценкой степени выраженности и обратимости бронхообструкции по показателям (FEV1 — объем форсированного выдоха за 1 секунду, FVC — форсированная жизненная емкость легких, соотношение FEV1/ FVC;
— анализ спирографии с применением нагрузочных и медикаментозных тестов;
— пикфлоуметрия — мониторирование суточной вариабельности пиковой скорости выдоха
4. Иммунологическое исследование:
— оценка показателей системной иммунологической защиты (клеточных, гуморальных и макрофагальных) и факторов местного иммунитета с учетом количественных показателей и функционального состояния различных звеньев иммунной системы.
5. Аллерготестирование для выявления причинно-значимых аллергенов:
— методы in vitro (определение причинно значимых аллергенов с использованием ИФА, ИТМ и т.д.);
— методы in vivo (скарификационные и уколочные тесты).
Критерии тяжести приступа БА
— Частота дыхания.
— Участие вспомогательной мускулатуры в акте дыхания.
— Интенсивность свистящего дыхания.
— Вздутие грудной клетки.
— Характер и проведение дыхания в легких (при аускультации).
— Частота сердечных сокращений.
— Вынужденное положение тела.
— Изменение поведения.
— Степень ограничения физической активности.
— Объем терапии (препараты и способы их введения), используемый для купирования пр иступа.
2006/85/1_20.png)
Дифференциальная диагностика
Бронхообструктивный синдром (БОС) — это симптомокомплекс, связанный с нарушением бронхиальной проходимости функционального или органического происхождения.
Термим «бронхообструктивный синдром» не может быть использован как самостоятельный диагноз.
Классификация БОС
1. Заболевания органов дыхания.
1.1. Инфекционно-воспалительные заболевания (бронхит, бронхиолит, пневмония).
1.2. Бронхиальная астма.
1.3. Аспирация инородных тел.
1.4. Бронхолегочная дисплазия.
1.5. Пороки развития бронхолегочной системы.
1.6. Облитерирующий бронхиолит.
1.7. Туберкулез.
2. Заболевания желудочно-кишечного тракта (халазия и ахалазия пищевода, гастроэзофагальный рефлюкс, трахеопищеводный свищ, диафрагмальная грыжа)
3. Наследственные заболевания (муковисцидоз, дефицит α-1-антитрипсина, мукополисахаридозы, рахитоподобные заболевания)
4. Паразитарные инфекции (токсокароз)
5. Заболевания сердечно-сосудистой системы
6. Заболевания центральной и периферической нервной системы (родовая травма, миопатии и др.)
7. Врожденные и приобретенные иммунодефицитные состояния
8. Воздействия различных физических и химических факторов внешней среды
9. Другие причины (эндокринные заболевания, системные васкулиты, тимомегалия и др.)
Критерии оценки степени тяжести
Критерии тяжести БА:
1. Количество дневных симптомов в день и в неделю.
2. Количество ночных проявлений симптомов в неделю.
3. Выраженность нарушений физической активности и сна.
4. Величина пиковой скорости выдоха (ПСВ) и процентное соотношение к норме или наибольшей величине.
5. Суточные колебания ПСВ.
6. Частота использования β-2-агонистов короткого действия (беротек, сальбутамол).
7. Состояние больного во внеприступный период.
Оценка степени тяжести БА согласно клиническим симптомам
1. Интермитирующая астма:
— кратковременные эпизодические симптомы 1 раз в неделю;
— короткие приступы;
— ночные симптомы реже 2 раз в месяц;
— отсутствие симптомов и нормальная функция легких между обострениями;
— ПСВ более 80% от нормы;
— колебания ПСВ менее 20%.
2. Легкая персистирующая астма:
— обострения 1-2 раза в неделю.
— ночные проявления возникают чаще 2 раз в месяц.
— нарушение физической активности и сна.
— ПСВ более 80% от нормы.
— колебания ПСВ 20-30%.
3. Среднетяжелая персистирующая астма:
— ежедневные проявления заболевания.
— ночные приступы чаще 1 раза в неделю.
— обострения могут приводить к нарушению физической активности и сна.
— ПСВ от 60 до 80% от нормы.
— колебания ПСВ 30%.
— потребность в ежедневном применении β-2-агонистов короткого действия.
4. Тяжелая персистирующая астма:
— частые обострения.
— постоянное присутствие симптомов.
— частые ночные приступы.
— ограничение физической активности.
— ПСВ менее 60% от нормы.
— колебания ПСВ более 30%.
2006/85/2_20.png)
Таким образом, своевременная корректная диагностика бронхиальной астмы, идентификация факторов риска, определение степени тяжести заболевания являются первостепенными для адекватного лечения и полного контроля над заболеванием.
Источник


